Bibliothek
- Biologie
- Q1 - Genetik
- Von der DNA zum Protein
- Watson-Crick-Modell Die DNA (Desoxyribonukleinsäure) ist für das Leben jeder Zelle essenziell und enthält die Informationen (den Bauplan) jeder Zelle und jedes Proteins. Auf der DNA sind diese Informationen in Form von Genen codiert. Proteine und somit auch die DNA sind für den Stoffwechsel und damit für jedes Leb...
- Semikonservative ReplikationDurch das Messelson-Stahl-Experiment wurde die semikonservative Replikation als Replikationsvorgang nachgewiesen. Dieser Vorgang dient der Verdopplung der DNA im Zuge der Mitose oder Meiose. Bei der Replikation werden immer alle Genabschnitte verdoppelt. Durch Replikationsfehler kann es zu Mutatione...
- GeneDer Genbegriff und die Genexpression werden gerne als Definition abgefragt. Deshalb sollten die Schlüsselwörter in jedem Fall auswendig gelernt werden: Genbegriff: Ein Gen ist ein DNA-Bereich, der exprimiert werden kann und dabei zur Herstellung eines Polypeptids oder eines RNA-Moleköls mit eine...
- Proteinbiosynthese - TranskriptionDie Proteinbiosynthese ist das beliebteste Abiturthema der Genetik. Die Proteinbiosynthese beschreibt den Prozess, der in einer Zelle abläuft, um die Informationen eines Gens in ein fertiges Protein zu übersetzen. Dabei muss die im Zellkern vorliegende DNA bei Eukaryoten erst umgeschrieben und kop...
- Proteinbiosynthese - TranslationFunktion: Die tRNA (transfer-RNA) spielt eine wichtige Rolle bei der Translation, da sie eine bestimmte Aminosäure aufnimmt und diese zu den Ribosomen transportiert. An den Ribosomen angekommen, kann sich die tRNA an die passende mRNA-Stelle heften. So werden zu jedem Codon exakt die zugehörigen A...
- CodesonneWichtig: Nur eine mRNA-Sequenz kann mit der Codesonne übersetzt werden. Ist keine mRNA-Sequenz gegeben, muss die gegebene Basensequenz in eine mRNA übersetzt werden. Dabei gibt es zwei Möglichkeiten: Der codogene Strang (3' → 5') ist gegeben: Er muss in eine mRNA-Sequenz übersetzt werden. D...
- Proteinbiosynthese bei EukaryotenDie Proteinbiosynthese findet bei Eukaryoten räumlich und zeitlich getrennt statt. Dies liegt daran, dass die Prä-mRNA erst reifen muss, um anschließend aus dem Zellkern zu den Ribosomen transportiert zu werden. Als Prä-mRNA bezeichnet man die mRNA, die direkt durch Transkription entsteht und an...
- Raumstruktur von ProteinenNach der Proteinbiosynthese liegt eine Polypeptidkette frei im Cytoplasma vor. Eine Polypeptidkette ist eine Kette aus vielen (griech.: poly = viel) Aminosäuren, die über Peptidbindungen verbunden sind. Bevor die Polypeptidkette jedoch als Protein funktionsbereit ist, müssen sogenannte Faltstrukt...
- GenmutationDurch äußere- und innere Einflüsse oder Replikationsfehler können Mutationen der DNA entstehen. Befinden sich diese Mutationen auf einem codierenden Bereich der DNA kann es zur Veränderung der Proteinstruktur bzw. -funktion kommen. Dadurch können Krankheiten entstehen, da beispielsweise bestim...
- Evolutionsaspekt von Mutationen Mutationen spielen eine entscheidende Rolle in der Evolution. Nur durch spontane Mutationen in den Zellen der Keimbahn (Spermien und Eizellen) ist es möglich, dass völlig neue Merkmale in der folgenden Generation auftreten. Da Mutationen aber immer spontan auftreten, ist die Wahrscheinlichkeit, da...
- Regulation der Gentätigkeit
- Regulation bei Bakterien nach dem Jacob-Monod-Modell Das Jacob-Monod-Modell oder auch Operon-Modell beschreibt das einfachste Prinzip der Genregulation und läuft in Prokaryoten ab. Es basiert darauf, dass es zu jedem Genabschnitt, der für ein Protein codiert, ein sogenanntes Operon gibt. Dieses Operon besitzt verschiedene Abschnitte zur Regulation d...
- Substratinduktion Lactose-OperonDas Lactose-Operon befindet sich in einem Bakterium, welches dazu in der Lage ist, Lactose mit Hilfe des Strukturgens lacZ abzubauen. Da es zu energieaufwändig wäre, dieses Strukturgen ständig zu transkribieren und translatieren, soll dies nur geschehen, wenn auch Lactose gegenwärtig ist. Dazu ...
- Endproduktrepression Tryptophan-Operon Bei der Endproduktrepression ist das Ziel die Herstellung eines Stoffes, der in der Zelle in einer bestimmten Konzentration vorliegen soll. Im Folgenden wird der Mechanismus der Endproduktrepression anhand der namensgebenden Aminosäure Tryptophan erklärt. Diese ist ein Baustein von Peptiden und so...
- Genregulation bei EukaryotenDie oben beschriebenen Vorgänge sind die einfachsten Regulationsvorgänge, die in Lebewesen stattfinden. Daher sind sie fast ausschließlich in Einzellern zu finden. Menschen sind wie alle Eukaryoten komplexere Organismen. Daher müssen mehrere Umstände in die Genregulation einbezogen werden. Die ...
- Epigenetische ModifizierungDie Epigenetik befasst sich mit Faktoren, die die Aktivität bestimmter Gene beeinflussen, ohne deren Basensequenz zu verändern. Diese werden teilweise vererbt, können aber auch durch Umweltfaktoren beeinflusst werden. Die Aktivität der Gene kann durch das Binden oder Entfernen bestimmter Molekü...
- Bakterien
- Bau und Vermehrung von BakterienBakterien bilden die einfachste Lebensform dieser Erde. Sie sind Einzeller und besitzen keinen Zellkern. Daher zählen sie zu den Prokaryoten. Die DNA „schwimmt“ vielmehr als Bakterienchromosom und in Form kleinerer Plasmidringe frei im Cytoplasma umher und wird nicht von einer Membran umgeben (...
- Transformation und KonjugationDa die Vermehrung von Bakterien durch Zellteilung stattfindet, kann es bei diesem Prozess zu keinem Austausch genetischer Informationen kommen, so wie es bei der geschlechtlichen Fortpflanzung anderer Lebewesen der Fall ist. Da ein Austausch und eine Rekombination genetischer Informationen aus evolu...
- Antibiotika und Antibiotikaresistenzen Antibiotika sind die meisten natürlichen Stoffe, die Pilze oder andere Lebewesen entwickelt haben, um sich in der Natur gegen Bakterien durchzusetzen. Es sind Stoffe, die sich so stark auf den Stoffwechsel von Bakterien, dass entweder das Wachstum und die Teilung des Bakteriums verhindert (bak...
- Viren/Phagen
- Bau von PhagenPhagen ist der Begriff für Viren, die auf Bakterien als Wirtszellen spezialisiert sind. Sie sind somit ebenso wie andere Viren keine Lebewesen und sind auf eine Wirtszelle angewiesen. Grob gesagt sind sie nur aus DNA und Hüllproteinen aufgebaut. Zur Erklärung des Aufbaus wird gerne der T2-Bakteri...
- Vermehrung von PhagenBei der Vermehrung von Phagen unterscheidet man zwischen dem lytischen und dem lysogenen Zyklus. Während der lytische Zyklus die aktive Vermehrung darstellt, ist der lysogene für die passive zuständig. Der lytische Zyklus ist für den lysogenen Zyklus die Voraussetzung. Man unterscheidet beim lyt...
- TransduktionTransduktion ist eine Variante des Genaustausches zwischen Bakterien mit Hilfe von Phagen. Während der Latenzphase können Teile der Bakterien-DNA mit in den Kopf von Phagen eingeschlossen werden. Dies kann sogar so weit gehen, dass sich nur Bakterien-DNA in den Phagen befindet und somit keine viru...
- Methoden der Gentechnik
- RestriktionsenzymeRestriktionsenzyme arbeiten nach einem einfachen Prinzip: Sie schneiden DNA an ganz bestimmten Sequenzen in zwei Teile. Diese Sequenzen sind typischerweise Palindrome (Ein Palindrom liest sich vorwärts wie rückwärts gleich. Also zum Beispiel GAATTC, dessen Tochterstrang CTTAAG wäre). Die Enzyme ...
- Polymerase-KettenreaktionDie Polymerase-Kettenreaktion (PCR) wurde entwickelt, um das System der DNA-Replikation zu imitieren. Allerdings soll dabei meistens nur ein bestimmter Abschnitt repliziert werden. Das Ziel ist also die Vervielfältigung eines bestimmten DNA-Abschnittes. Die Voraussetzung dafür ist, dass dieser Abs...
- Gelelektrophorese Das Ziel der Gelelektrophorese ist es, DNA-Fragmente aufgrund ihrer Größe bzw. Länge voneinander zu trennen . Dies kann zum Beispiel zum Nachweis einer Genvariante oder für einen Vaterschaftstest verwendet werden. Der Einsatz dieser Methode ist sehr umfangreich und aus Forschungslaboren nicht m...
- Genetischer FingerabdruckSicherlich hast du den Begriff des genetischen Fingerabdrucks schon einmal gehört. Hierbei handelt es sich um eine Technik der Molekularbiologie, welche es erlaubt, genetisches Material mit anderem genetischen Material auf Übereinstimmungen zu überprüfen. Ohne eine Vergleichsprobe sagt ein genet...
- Exkurs: Diagnose der Erkrankung Chorea HuntingtonChorea Huntington war in den vergangenen Abiturdurchgängen ein beliebtes Thema, da anhand der Erkrankung sowohl Methoden der Gentechnik wie auch Themen der Neurologie abgefragt werden konnten. Häufig wurden die jeweiligen Aufgaben mit entsprechendem Material kombiniert....
- Gentransfer durch VektorenBeim Gentransfer durch Vektoren werden Plasmidringe verwendet, um ein bestimmtes Gen in ein Bakterium einzubringen. Ein bekanntes Beispiel ist das Einbringen des Insulin-Gens. Hiermit wird angestrebt, dass das Bakterium Insulin produziert, um es anschließend Personen verabreichen zu können, die ke...
- Biomedizinische Aspekte der Genetik
- Krebs - Bösartige GewebeneubildungBei dem Begriff "Krebs" hat vermutlich jeder direkt eine Assoziation im Kopf, die durch die Schwere dieser Erkrankungsform meist sehr negativ ist. Laut statistischem Bundesamt war im Jahr 2019 Krebs zusammengenommen die zweithäufigste Todesursache in Deutschland1. Bei dieser Gruppe von Erkrankungen...
- Exkurs: Beispiele für das Entstehen von Krebserkrankungen Das Retinoblastom-Gen codiert für das Retinoblastom-Protein (Rb). Dieses ist ein Tumorsuppressorprotein, welches eine wichtige Rolle bei der Regulation des Zellzyklus spielt. Während der G1-Phase befindet sich das Retinoblastom-Protein im nicht-phosphorylierten, aktiven Zustand. In diesem Z...
- StammzellenStammzellen sind Körperzellen, welche sich zu bestimmten Zelltypen und Gewebearten ausdifferenzieren können. Sie besitzen noch keine oder eine nur geringe Differenzierung und daher noch keine festgelegte Funktion im Organismus. Aus ihnen können zum einen durch mitotische Teilung weitere Stammäze...
- Stammbaumanalyse
- StammbaumanalyseEine Stammbaumanalyse kann die perfekte Aufgabe sein, um in einem kurzen Zeitraum die volle Punktzahl zu holen, da die Aufgabenstellung meist klar definiert ist. Nach dem unten angegebenen System kann jeder Stammbaum bearbeitet und analysiert werden. Bevor auf die Analyse von Stammbäumen näher ein...
- Stammbaumanalyse - AlgorithmusNun hast du alle wichtigen Informationen zur Stammbaumanalyse gelernt. Da eine vollständige Analyse jedoch manchmal kompliziert und verwirrend sein kann, haben wir dir zusätzlich einen Algorithmus erstellt. ...
- Von der DNA zum Protein
- Q2 - Ökologie und Stoffwechselphysiologie
- Strukturierung von Ökosystemen
- Toleranzkurve & ökologische PotenzDie Ansprüche eines Lebewesens oder einer Population an einen bestimmten Umweltfaktor lassen sich in einer Toleranzkurve darstellen. Sie stellt dabei die Intensität der Lebensvorgänge in Abhängigkeit von der Intensität des Umweltfaktors dar. Die Kurve reicht dabei vom Minimum bis zum Maximum di...
- Ökologische Nische und KonvergenzDie Gesamtheit aller Ansprüche eines Lebewesens an seine Umwelt – alle biotischen und abiotischen Faktoren – werden gemeinsam als ökologische Nische bezeichnet. Unter Einnischung versteht man das Ausbilden einer bzw. das Spezialisieren auf eine ökologische Nische. Dies kann evolutionär oder ...
- Biotop und BiozönoseAls Biotop bezeichnet man den unbelebten Lebensraum einer Lebensgemeinschaft und damit im Allgemeinen die Gesamtheit aller abiotischen Faktoren. Das Biotop stellt die Lebensgrundlage für alle Lebewesen dieses Gebietes dar. Man muss ein Biotop aber getrennt von allen es bewohnenden Lebewesen betrach...
- Abiotische FaktorenAbiotische Faktoren umfassen alle Faktoren der unbelebten Natur. Sie sind die nicht belebten Bestandteile eines Ökosystems. Die vier wichtigsten abiotische Faktoren sind dabei: LichtWasserTemperaturMineralien...
- Wasser als abiotischer FaktorWasser ist die Grundlage allen Lebens und damit für alle Lebewesen von größter Bedeutung. Im Folgenden werden Diffusion und Osmose erklärt, da dies wichtige Grundlagen für das Abitur sind....
- Hydroregulation bei PflanzenDie Hydroregulation der Pflanzen besteht aus drei wichtigen Teilen: Der Wasseraufnahme, dem Wassertransport und der Abgabe des Wassers. Diese sind notwendig, um einen ständigen Fluss in der Pflanze aufrechtzuerhalten und somit Mineralien und Nährstoffe zu transportieren und ausreichend Wasser für...
- Temperatur als abiotischer FaktorAnhand des Faktors Temperatur lassen sich Unterschiede hinsichtlich der Körpertemperatur und -produktion von Tieren sowie der Abhängigkeit des Phänotypen von abiotischen Faktoren erklären. Hierbei gilt es drei Regeln, die RGT-Regel, Allensche und Bergmannsche Regel, zu verinnerlichen und reprodu...
- ThermoregulationEs kann zwischen verschiedenen Thermoregulationsmechanismen bei Tieren unterschieden werden. Die wichtigste Unterscheidung ist dabei die zwischen endotherm und ektotherm: Endotherme Tiere produzieren selbst Körperwärme, sie kommt also von innen (endo). Ektotherme Tiere beziehen ihre Körperwär...
- RegelkreislaufmodellFür das Abitur gilt es, Regelkreisläufe beschreiben und interpretieren zu können. Dazu werden im Folgenden die grundlegenden Bestandteile eines Regelkreises besprochen. Demonstriert werden diese Bausteine nun exemplarisch im Zusammenhang der Thermoregulation endothermer Tiere. ...
- Biotische FaktorenBiotische Faktoren sind die Faktoren, die von anderen Lebewesen ausgehen und die Population einer Art beeinflussen. Zu nennen sind hier die vier wichtigsten: Konkurrenz Parasitismus Symbiose Räuber-Beute-Beziehung...
- Ökofaktoren als SelektionsfaktorenEin Selektionsfaktor ist ein Umweltfaktor bzw. eine Umweltbedingung, die sich auf den Fortpflanzungserfolg eines Individuums auswirkt. Selektionsfaktoren wirken permanent auf Individuen einer Population und führen letztendlich dazu, dass diejenigen Individuen, die am besten angepasst sind, die meis...
- Stoffkreisläufe im ÖkosystemIn einem ausgewogenen Ökosystem findet man immer Produzenten, Konsumenten und Destruenten: Produzenten nutzen die Energie der Sonne, um durch die Photosynthese energiereiche organische Verbindungen wie zum Beispiel Glukose aufzubauen. Somit kann die Sonnenenergie chemisch fixiert werden. Neben der ...
- NahrungsnetzEin Nahrungsnetz beschreibt die trophischen Beziehungen eines Habitats. Das Nahrungsnetz ist wie eine Nahrungspyramide zu verstehen. Der einzige Unterschied besteht darin, dass die Nahrungsbeziehungen in einem Nahrungsnetz deutlich komplexer dargestellt sind. Dadurch kann aus einem Nahrungsnetz entn...
- SukzessionSukzession beschreibt in der Ökologie die zeitliche Abfolge von Vergesellschaftungen verschiedener Pflanzen-, Tier-, Bakterien- und Pilzarten nach einem veränderten Ausgangszustand an einem Standort. Dabei kann es sich im Extremfall um einen vegetationsfreien Boden handeln, der sukzessiv und phase...
- Nachhaltigkeit am Beispiel eines ausgewählten ÖkosystemsDer Begriff der Nachhaltigkeit wird in den verschiedensten Bereichen des Lebens verwendet. Was aber bedeutet Nachhaltigkeit und wie kann sie auf Ökosysteme angewandt werden? Eine häufig verwendete Definition für Nachhaltigkeit stammt von Gro Harlem Brundtland. Dieser sagt, dass durch nachhaltiges...
- Ökosystem FließgewässerLaut dem Erlass für das anstehende Abitur sollen verschiedene Themen anhand des Ökosystems „Fließgewässer“ erklärt werden. Der Aufbau sowie biotische und abiotische Faktoren dieses Ökosystems werden im Folgenden aufgeführt....
- Grundlegende Stoffwechselprozesse
- BlattaufbauIst in den Handreichungen nach dem Blattaufbau gefragt, so soll der Blattaufbau von mesophyten C3-Pflanzen reproduktiv wiedergegeben werden. Der Begriff mesophyt kommt aus dem altgriechischen (mesos = mittig; phyton = Pflanze) und bedeutet, dass diese unter mittel feuchten, gemäßigten Klimabedin...
- Photosynthese - GrundlagenDie Photosynthese stellt die Grundlage unseres Lebens dar, da sie von fast allen Produzenten genutzt wird, um durch die Energie der Sonnenstrahlung energiereiche organische Verbindungen wie zum Beispiel Glukose aufzubauen. Die Photosynthese findet in den Chloroplasten der Pflanzen statt. Unterschied...
- Lichtabhängige Reaktion (Lichtreaktion)Die lichtabhängige Reaktion benötigt – wie der Name schon sagt – Licht, welches als Energiequelle fungieren, um die energiereichen Verbindungen ATP und NADPH + H+ herzustellen. Die Lichtreaktion findet in der Membran der Thylakoide in den Lichtsammelkomplexen statt. Dabei bilden zwei hinterein...
- Lichtunabhängige Reaktion (Dunkelreaktion)Die Dunkelreaktion wird nicht etwa Dunkelreaktion genannt, weil sie im Dunklen abläuft, sondern weil für ihren Ablauf kein Licht benötigt wird. Das Ziel der Dunkelreaktion ist der Aufbau einer energiereichen Kohlenstoffverbindung (Glukose) unter Verbrauch von Kohlendioxid und Wasser. Die dazu nö...
- Exkurs: CAM-Stoffwechselweg Der CAM-Stoffwechselweg der lichtunabhängigen Reaktion ist laut Erlass zwar nicht abiturrelevant, war in der Vergangenheit aber ein beliebtes Abiturthema, das häufig mit Material und dem Calvin-Zyklus als Reproduktionsaufgabe abgefragt wurde. Um das Wissen der vorherigen Kapitel zu festigen und ei...
- ZellatmungMitochondrien stehen im Mittelpunkt des zellulären Energiestoffwechsels und werden daher auch als „Kraftwerke der Zelle“ bezeichnet. Mitochondrien zeichnen sich dadurch aus, dass sie im Gegensatz zu anderen Organellen gleich durch zwei Membranen vom Cytoplasma abgegrenzt sind. Die äußere Memb...
- Strukturierung von Ökosystemen
- Q3 - Neurobiologie und Verhaltensbiologie
- Neurobiologie
- Bau und Funktion einer NervenzelleDer Aufbau einer Nervenzelle ist von ihrer Funktion abhängig und daher sehr variabel. Im Folgenden wird dieser beispielhaft anhand einer peripheren Nervenzelle beschrieben. Wie fast alle anderen Zellen unseres Körpers besitzt eine Nervenzelle ein Soma (Zellkörper) mit Zellkern und den übrigen Ze...
- RuhepotentialDas Ruhepotential beschreibt das im Grundzustand vorliegende Membranpotential einer erregbaren Nervenzelle. Dieses ist essenziell für die Funktionalität der Nervenzelle, da es das schnelle Ablaufen eines Aktionspotenzials überhaupt erst ermöglicht. Im Ruhepotential beträgt die Potentialdifferen...
- AktionspotentialEin Aktionspotential (AP) ist eine schlagartige Veränderung des Membranpotentials in den positiven Bereich. Diese Änderung des Membranpotenzials hält nur für einen sehr kurzen Moment an, bevor sich wieder das Ruhepotenzial einstellt. Ein Aktionspotential läuft charakteristischerweise immer glei...
- ErregungsweiterleitungDie Erregungsleitung im Nervensystem ist für uns von großem Interesse. Wir besitzen ein somatisches und ein vegetatives Nervensystem. Das somatische Nervensystem ist für die Aufnahme von Reizen und Ausführung von Bewegungen zuständig, während das vegetative Nervensystem die Organfunktionen reg...
- SynapseLaut Erlass sollen der Bau und die Funktion einer Synapse anhand einer Acetylcholin führenden Synapse erklärt werden können. Hierbei handelt es sich um eine der beliebtesten Abituraufgaben der letzten Jahre. Im Folgenden wird zuerst der Aufbau einer Synapse dargestellt, um anschließend den Ablau...
- Wirkung von SynapsengiftenDie Wirkungsweise von Synapsengiften war in der Vergangenheit eine sehr beliebte Abituraufgabe. Daher werden wir im Folgenden verschiedene Wirkmechanismen mit einzelnen Beispielen darstellen. Diese müssen nicht auswendig gelernt werden, können aber das Verständnis des Themenkomplexes verbessern. ...
- Neuromuskuläre Synapse - Motorische EndplatteBei der neuromuskulären Synapse handelt es sich um eine Acetycholin führende Synapse mit einer Muskelzelle als Zielzelle. Doch bevor der Ablauf erklärt werden kann, müssen einige Besonderheiten und Begriffe geklärt werden. Viele Zellorganellen der Muskelzelle haben andere Namen. Sie beginnen me...
- Verrechnung postsynaptischer PotentialeHinter den Abkürzungen EPSP und IPSP stecken zwei Wirkprinzipien an der Synapse. Entweder wird an der postsynaptischen Membran durch den Einstrom positiv geladener Ionen ein positiveres Membranpotential ausgelöst, das zur Auslösung eines Aktionspotentials am Axonhügel beitragen kann, oder das Me...
- SignalumwandlungZum allgemeinen Verständnis wird nun einmal der Weg eines Reizes von seinem Ursprung bis zum 2. Neuron beschrieben. Dabei wird der Vergleich zwischen einem starken und einem schwachen Reiz angestellt. Ein Reiz führt zur Erregung einer Rezeptorzelle (z.B. Messfühler in der Haut). Die Erregung der...
- Prinzip von Second-messenger-VorgängenIm Folgenden wird das Prinzip eines sekundären Botenstoffes erklärt. Zur besseren Darstellung wird dafür das Beispiel der olfaktorischen (den Geruchssinn betreffenden) Signaltransduktion gewählt. Das Prinzip eines Second-messenger-Vorgangs sollte im Abitur erkannt und auf andere Beispiele übert...
- RezeptorenInformationen der Umwelt können von unserem Gehirn registriert werden. Dazu besitzen wir Rezeptor- bzw. Sinneszellen. Jede Sinneszelle ist dabei auf das Registrieren eines bestimmten Reizes spezialisiert. Man spricht dabei von dem adäquaten Reiz. Aber auch Reize, die zu dem Rezeptor gar nicht pass...
- Bau und Funktion der Netzhaut - RetinaDie Netzhaut (Retina) ist der Ort des Auges, an welchem die Lichtsignale der Umgebung in elektrische Impulse umgewandelt werden (Phototransduktion). Sie ist nahezu durchsichtig und kleidet den Augapfel von Innen aus. Sie besitzt mehrere Schichten mit unterschiedlichen Zelltypen, welche bei der Photo...
- PhototransduktionOrt der Phototransduktion sind die Stäbchen und Zapfen. Diese sind vom Prinzip her beide ähnlich aufgebaut. Sie besitzen einen Zellkörper mit einer Synapse und einem Außensegment. Die Synapse reicht bis zur Bipolarzelle und das Außensegment ist zur Pigmentschicht gerichtet. Das Außensegment en...
- Sensorische und motorische NervenEin Nerv ist nicht gleich ein Nerv. Je nach Aufgabe und Lokalisation haben Nerven unterschiedliche Gestalten, Leitungsgeschwindigkeiten und Neurotransmitter in den synaptischen Endknöpfchen. Da für das Abitur wichtig, schauen wir uns nun sensorische und motorische Neurone an. ...
- InterneuroneFür das Abitur ist es wichtig die Komplexität des Nervensystems zu verstehen. Dabei kommt es fast immer auf Verschaltungen zwischen sehr vielen verschiedenen Nervenzellen an. Diese Aufgabe übernehmen sogenannte Interneurone. Da Interneurone so unterschiedliche Funktionen haben können möchten wi...
- Physiologie des LernensDie Veränderung von Synapsen (sogenannte synaptische Plastizität) bildet die Grundlage des Lernens. Hierbei führt eine Veränderung von Synapsen zu einer Veränderung der Verschaltung der Neurone. Dies kann beispielsweise dazu führen, dass auf einen Reiz künftig schneller reagiert werden kann. ...
- Verhaltensbiologie
- EthogrammDas Ethogramm steht nun seit über vielen Jahren in dem Kernkurrikulum des Fachs Biologie und wurde bisher noch nicht im Abitur behandelt. Nichtsdestotrotz wollen wir dir an dieser Stelle einen kleinen Einblick in das Thema geben. Ein Ethogramm kann auch als Verhaltenskatalog eines Tieres verstanden...
- Angeborenes VerhaltenReflexe ermöglichen durch ihre neuronale Verschaltung eine schnelle und automatisierte Reaktion auf einen bestimmten Reiz. Dabei ist die Reaktion auf diesen bestimmten Reiz immer die gleiche und unterscheidet sich nur in der Stärke der Ausprägung. Zum besseren Verständnis wird im Folgenden der m...
- Erlerntes Verhalten Reagiert ein Lebewesen auf eine gleiche Situation unterschiedlich, so ist dies auf Reaktionsunterschiede innerer Vorgänge zurückzuführen. Grund für diese Reaktionsunterschiede sind endogene oder exogene Faktoren. Endogene Faktoren finden im Körper selbst statt, während exogene Faktoren von au...
- KonditionierungUnter Konditionierung wird eine Form des Lernens verstanden, bei der ein Reiz wiederholt mit einem zweiten Reiz (klassische Konditionierung) oder einer bestimmten Reaktion (operante Konditionierung) gekoppelt wird. Entsprechend der Folgen dieser Kopplung findet eine Bewertung des initialen Reizes st...
- Überlebenswert von VerhaltensmerkmalenEine Population einer Art ist ständig äußeren und inneren Faktoren und somit einem Selektionsdruck ausgesetzt. Mutation und Genrekombination bewirken, dass die genetische Vielfalt in einer Population zunimmt. Diejenigen Individuen, die besser mit den gegebenen Umweltbedingungen zurechtkommen, kö...
- VerhaltensökologieBei einer Kosten-Nutzen-Analyse wird das Verhalten eines Tieres untersucht. Diese Untersuchung soll darüber Auskunft geben, ob sich ein bestimmtes Verhalten positiv oder negativ auf das Einbringen von Genen in den Genpool auswirkt. Dabei wird alles, was zum Überleben des Nachwuchses beiträgt und ...
- Neurologische Erkrankungen
- Neurologische Erkrankungen - GrundlagenSo wie jedes andere Organsystem des Menschen, kann auch das Nervensystem erkranken. Die dadurch entstehenden neurologischen Erkrankungen sind meist sehr komplex und häufig schwer zu behandeln. Dazu kommt, dass die Ursachen verschiedenster neurologischer Erkrankungen meist höchst unterschiedlich si...
- Demenz Unter dem Begriff der Demenz werden verschiedene neurologische Krankheitsbilder zusammengefasst, die mit einer progredienten Verschlechterung kognitiver Fähigkeiten einhergehen. Je nach Form und Intensität der Erkrankung können kognitive Fähigkeiten wie die Gedächtnisleistung, das Sprachverstä...
- Morbus ParkinsonDie Parkinsonkrankheit, umgangssprachlich auch Schüttellähmung genannt, zählt zu den neurodegenerativen Erkrankungen. Sie ist durch einen Verlust dopaminerger Nervenzellen gekennzeichnet. Dieser wirkt sich vor allem auf motorische Fähigkeiten aus und führt zu den Kernsymptomen Bradykinese (Lang...
- Bildgebende Verfahren der HirnforschungEs gibt verschiedene Methoden der Hirnforschung, die es uns ermöglichen, mithilfe von bildgebenden Verfahren in innere Strukturen des Schädels zu schauen, ohne diesen zu beschädigen oder den Patienten zu gefährden. Da diese verschiedenen Methoden zur Darstellung der Strukturen oder auch der Funk...
- Neurobiologie
- Q1 - Genetik
- Chemie
- Grundlagen
- Atommodell und Periodensystem
- Bohrsches AtommodellDas Bohrsche Atommodell ist eine Weiterentwicklung des Rutherford-Atommodells. Demnach besteht ein Atom aus einem positiv geladenen Kern, der Protonen und Neutronen (ohne Ladung) enthält. Da nur Protonen und Neutronen eine für das Gesamtgewicht des Atoms relevante Masse haben, macht der Kern die ...
- Periodensystem der Elemente (PSE)Die Elemente des Periodensystems sind ungeladen, da sie die gleiche Anzahl an Protonen und Elektronen aufweisen. Die Protonen- und Elektronenzahl ist gleich der Ordnungszahl und zeigt an, um welches Element es sich handelt. Die Massenzahl steht im PSE neben der Ordnungszahl und ergibt sich aus der ...
- Chemische Wechselwirkungen und Bindungen
- Intramolekulare WechselwirkungenIn der Chemie können zwei Arten von Kräften unterschieden werden: Die intramolekularen Wechselwirkungen (von lateinisch intra = innerhalb) und die intermolekularen Wechselwirkungen (von lateinisch inter = zwischen). Die intramolekularen Wechselwirkungen herrschen somit innerhalb eines Moleküls, w...
- Intermolekulare WechselwirkungenBei Intermolekularen Wechselwirkungen handelt es sich um Wechselwirkung zwischen Molekülen. Diese Wechselwirkung sind maßgebend für verschiedene Stoffeigenschaften, wie die Siede- und Schmelztemperatur, Löslichkeit und Viskosität. Hierbei ist wichtig zu verstehen, wie diese Kräfte zustande kom...
- Reaktionsgleichung und Säure/Base-Konzepte
- Reaktionsgleichungen1. Triebkraft einer Reaktion: Triebkraft einer chemischen Reaktion ist das Erreichen der Edelgaskonfiguration. Diese Konfiguration kann durch das Auftreten chemischer Bindungen erreicht werden. Dabei werden die Elektronen formell über die Oxidationszahlen einem Bindungspartner zugewiesen. Ziel...
- Säure/Base-KonzepteDie zwei wichtigsten Modelle zum Erklären von Säure/Base-Reaktionen sind das Brønstedt-Modell sowie das Lewis-Modell. Die Brønstedt-Theorie geht davon aus, dass Säuren (S) Protonendonatoren sind. Das heißt, dass sie bei Reaktionen ein H+-Teilchen (Proton) abspalten. Basen (B) hingegen sind P...
- Orbitalmodell
- Grundlagen des OrbitalmodellsDas Orbitalmodell ist ein quantenmechanisches Atommodell. Es wurde entwickelt, da sich einige Eigenschaften oder Verhaltensweisen von Molekülen nicht mit dem Bohrschen Atommodell erklären lassen. Dazu stellt man sich die Elektronen nicht mehr als um den Kern kreisende Teilchen vor, sondern als Te...
- Molekülorbital(MO)-SchemaDie Elektronen eines Atoms weisen verschiedene Energieniveaus auf: Mit steigender Haupt- und Nebenquantenzahl steigt das Energieniveau eines Orbitals, während bei unterschiedlicher räumlicher Ausrichtung (ml) sowie bei unterschiedlichem Spin (ms) alle Orbitale energetisch gleichwertig sind. Ein b...
- Elektronenpaarbindung im OrbitalmodellNach dem Orbitalmodell kommt eine Elektronenpaarbindung zweier Atome durch das Überlappen ihrer Orbitale zustande. Je nachdem, wie viele und welche Orbitale überlappen, kommt es zu Einfach- oder Mehrfachbindungen. Damit eine Bindung zustande kommen kann, müssen drei Voraussetzungen erfüllt sein:...
- OrbitalhybridisierungDamit zwei Atome eine Bindung eingehen können, müssen die Orbitale mit den Valenzelektronen auf dieselbe Energiestufe gebracht werden. Um dies zu ermöglichen, gleichen sich s- und p-Orbitale energetisch an und hybridisieren. Im Abitur ist hierbei das Beschreiben von Hybridisierungszuständen in ...
- Beschreibung von BindungsverhältnissenIn den meisten Abituraufgaben zum Orbitalmodell sollen die Bindungsverhältnisse in einer Verbindung beschrieben werden. Gemeint ist hiermit, dass alle Hybridisierungszustände der Atome zu benennen und die Art aller Bindungen zu beschreiben sind. Am einfachsten ist es, mit der Hybridisierung der A...
- Isomerie
- Atommodell und Periodensystem
- Q1 - Stoffgruppen in der organischen Chemie
- Kohlenwasserstoffe
- Struktur und Eigenschaften von KohlenwasserstoffverbindungenKohlenwasserstoffe verdanken ihren Namen ihrem chemischen Aufbau, da die Stoffe dieser chemischen Gruppe aus Kohlenstoff und Wasserstoff bestehen. Dabei bilden die Kohlenstoffatome eine Art Rückgrat und sind gleichzeitig mit Wasserstoff assoziiert. Zu den Kohlenwasserstoffen gehören hauptsächlic...
- Reaktionen von Kohlenwasserstoffen
- Die radikalische SubstitutionAlkane sind prinzipiell eher inert (reaktionsträge) und reagieren daher nur mit sehr wenigen Elementen. Dazu gehören Sauerstoff und Halogene. Bei der Reaktion mit Sauerstoff (Verbrennung) entstehen immer Wasser und Kohlenstoffdioxid. Nur wenn nicht genug Sauerstoff vorhanden ist, können Nebenpro...
- Elektrophile AdditionBei der elektrophilen Addition wird immer eine Doppelbindung (genauer: π-Bindung) durch ein Elektrophil (elektronenliebendes Teilchen) angegriffen. Als Elektrophil kann jedes beliebige positiv polarisierte Teilchen auftreten, solange es ausreichend polarisiert ist. Man beschränkt sich jedoch meist...
- EliminierungEine Eliminierung stellt immer eine reine Abspaltung eines oder mehrerer Atome in einem Molekül dar. Ob diese Reaktion abläuft, wird von vielen Faktoren beeinflusst, wie beispielsweise dem Medium, in dem sich der Stoff befindet, der Art der Substituenten oder welche Abgangsgruppe (also welche Gru...
- Induktive EffekteDer induktive Effekt basiert, ähnlich wie die Elektronegativität, auf der Polarisierbarkeit von chemischen Bindungen. Ist ein Element eines Moleküls elektronegativer als sein Bindungspartner, so „zieht“ es die Elektronen häufiger in seine Nähe. Dadurch verschiebt sich das Gleichgewicht der ...
- Alkanole
- Struktur und Eigenschaften von AlkanolenDie Stoffklasse der Alkanole bzw. Alkohole entsteht durch gezielte Oxidation der entsprechenden Alkane. Alkanole wiederum können weiter zu Aldehyden oder Ketonen oxidiert werden. Die Aldehyde können anschließend noch weiter zu Carbonsäuren oxidiert werden. Alkanole können auch miteinander reagi...
- Reaktionen von Alkanolen
- Alkanolbildung durch nukleophile Substitution eines HalogenalkansDie nukleophile Substitution (SN) ist ein Reaktionsmechanismus, der nicht nur bei Alkanolen vorkommt und den du unbedingt für das Abitur beherrschen solltest. Bei der nukleophilen Substitution reagiert ein Nukleophil (=Stoff, der mit einem freien Elektronenpaar ein partiell positiv geladenes Atom ...
- AlkanolatbildungAlkanolate sind die Salze der Alkanole. Um diese zu erhalten, ist es notwendig, der Hydroxygruppe das Wasserstoffatom zu entziehen, wodurch ein Anion entsteht. Bei dieser Reaktion ist zu beachten, dass sie nur in wässriger Lösung, in der eine starke Base vorliegt, möglich ist. Außerdem können...
- Oxidationen von AlkanolenWer gerne kocht, weiß, dass Flüssigkeiten mit Ethanol ab einem gewissen Anteil an Ethanol in der Pfanne brennen können. Hierbei wird der Alkohol, ähnlich wie die Alkane, zu CO2 und H2O verbrannt. Hier lautet der Begriff „vollständige Verbrennung“. Wenn man ein Alkanol jedoch gezielt und ko...
- EtherbildungBei der Ethersynthese gibt es zwei hauptsächliche Ansätze: Bei dem ersten Ansatz reagiert beispielsweise ein Ethanolmolekül mit einem anderen Ethanolmolekül. Das Ganze läuft natürlich nicht einfach so ab, sonst könnte man sein Bier nach einiger Zeit nicht mehr genießen. Damit die Reaktion ...
- Carbonylverbindungen
- Struktur und Eigenschaften von CarbonylverbindungenCarbonylverbindungen spielen eine sehr wichtige Rolle im alltäglichen Leben. Sie stellen die Grundlage für viele Lösungs- und Reinigungsmittel dar. Auch in Kunststoffen und Proteinen (Eiweißen) spielen sie eine tragende Rolle, und sind für die Eigenschaften dieser mitverantwortlich....
- Reaktionen von Carbonylverbindungen
- Fehling- und Tollens-ProbeFunktion: Die Fehling-Probe wird verwendet, um zu testen, ob eine Probe weiter oxidierbar ist. Sie wird meist zum Nachweis von Aldehyden, wie beispielsweise Glukose, benutzt. Aufbau: Dazu verwendet man zwei Lösungen, die Fehling-Lösung I und II genannt werden: Die Fehling-Lösung I ist eine w...
- HydratisierungBei der Hydratisierung handelt es sich um eine nucleophile Addition von Wasser an eine Carbonylverbindungen (z.B. Keton oder Aldehyd). Diese Addition läuft in zwei Schritten ab: Das Sauerstoffatom des Wassers ist partiell negativ geladen. Durch die hohe Elektronegativität des Sauerstoffatoms der C...
- AcetalbildungBei der Acetalbildung wird ein beliebiges Alkanol an ein Aldehyd nucleophil addiert. Die Acetalbildung läuft im Gegensatz zu der Hydratisierung nicht von alleine ab. Die Reaktion muss durch eine Säure katalysiert (aktiviert) werden. Zuerst greift ein Proton (aus einer Säure) ein freies Elektrone...
- Alkansäuren und ihre Derivate
- Struktur und Nomenklatur von Carbonsäuren Wie bereits im vorherigen Kapitel angesprochen, ist die Carbonsäure eine Variante der Carbonylverbindungen. Dabei besitzt die Carbonylverbindung noch eine weitere Hydroxygruppe (OH-Gruppe), die die Eigenschaften des gesamten Moleküls beeinflusset. Die funktionelle -COOH-Gruppe der Carbonsäuren h...
- Eigenschaften von Carbonsäuren Versucht am Beispiel der Carbonsäuren euer Verständnis für die chemischen Eigenschaften selbst zu überprüfen, indem ihr euch zunächst Gedanken über die Wechselwirkungen, sowie deren Folge für die chemischen Eigenschaften macht und danach erst weiterlest.Bei den Carbonsäuren treten zusätzli...
- Derivate von CarbonsäurenEin Derivat ist grundsätzlich nichts anderes als ein Abkömmling eines Stoffes. Bereits im Unterkapitel Acidität wurden die Di- und Trisäuren erwähnt. Für diese müssen jedoch an der Alkansäure zwangsläufig weitere Hydroxidgruppen vorhanden sein, die ggf. oxidiert werden können. Besitzt ein...
- EsterbildungDie Esterbildung ist die wichtigste Reaktion der Carbonsäuren. Ihren Mechanismus sollte bekannt sein, da er oft abgefragt wird. Bei der Veresterung reagiert eine Carboxylgruppe mit einer Hydroxidgruppe unter Wasserabspaltung. Hierbei können die Reste stark variieren. Die Estergruppe sieht daher wi...
- Alkalische HydrolyseDie alkalische Hydrolyse ist der Fachbegriff für die Esterspaltung bzw. Verseifung. Anders als die saure Esterbildung ist diese Reaktion irreversibel (nicht umkehrbar): Nukleophiler Angriff des Hydroxid-Ions: Wird ein Ester in basischem Milieu gelöst bzw. gekocht, beginnt der erste Schritt der Ve...
- Kohlenwasserstoffe
- Q2 - Naturstoffe und Synthesechemie
- Peptide
- Struktur und Eigenschaften von AminosäurenAminosäuren bilden eine überlebenswichtige Stoffklasse bei nahezu allen Lebewesen. Indem die Aminosäuren als lange Ketten (Polymere) verknüpft werden, bilden sie Proteine. Diese übernehmen als Enzyme, Botenstoffe, Strukturproteine, Abwehrmoleküle und viele weitere Formen wichtige Aufgaben im...
- Peptidbindung und PolypeptideDie interessanteste Reaktion der Aminosäuren ist wohl die Reaktion zwischen der Aminogruppe der einen Aminosäure und der Carboxygruppe einer anderen Aminosäure. Diese Reaktion verläuft ähnlich wie die Veresterung, wird jedoch im Körper ausschließlich enzymatisch betrieben. Die Aminogruppe al...
- Kohlenhydrate
- Aufbau von KohlenhydratenKohlenhydrate werden auch Saccharide genannt und sind eine sehr große Naturstoffklasse. Sie sind ringförmigen Bausteinen, die hauptsächlich aus Kohlenstoffatomen und Hydroxygruppen (-OH) bestehen. Aufgrund dieser Hauptbestandteile haben sie ihren Namen „Kohlenhydrat“ erhalten. Diese Kohlenhyd...
- Projektionsformen von KohlenhydratenKohlenhydrate liegen nicht ausschließlich in ihrer ringförmigen Struktur vor. Zu einem geringen Anteil liegen sie auch als offene Kohlenstoffkette vor. Die Darstellung dieser offenen Kette erfolgt in der Fischer-Projektion. Diese hat klare Regeln zur Schreibweise der Moleküle: Die längste Kohle...
- Wiederholung und Vertiefung von IsomerieIn dem Kapitel „Isomerie“ wurden bereits verschiedene Isomerie-Arten erklärt. An dieser Stelle sollen diese nun auf Kohlenhydrate angewandt und vertieft werden. Dabei geht es vor allem um die Stereoisomerie. Stereoisomere sind Moleküle, die die gleiche Summenformel besitzen, sich jedoch hinsi...
- Glykosidische Bindung bei KohlenhydratenDie glykosidische Bindung ist eine Vollacetalbindung. Dabei reagieren zwei Saccharidbausteine zu einem Molekül. Bei der Reaktion wird eine glykosidische Bindung zwischen je einer Halbacetalgruppe der Zuckerbausteine aufgebaut und dabei Wasser abgespalten (Kondensationsreaktion). Da es bei dieser Re...
- Optische AktivitätDie meisten chiralen Moleküle können monochromatisches Licht um einen stoffspezifischen Winkel ablenken. Um diesen Winkel zu messen, wird linear polarisiertes Licht verwendet. Natürliches Licht besteht aus elektromagnetischen Wellen, die sich durcheinander in alle Richtungen bewegen. Bei linear p...
- MutarotationIn einer wässrigen Lösung liegen Kohlenhydrate nicht ausschließlich als Kohlenstoffringe vor. Vielmehr herrscht ein ständiges Gleichgewicht zwischen der Ringform (dargestellt in der Haworth-Projektion) und der offenkettigen Form (dargestellt in der Fisher-Projektion). Es handelt sich dabei um ei...
- Wichtige KohlenhydrateIn diesem Kapiteln wollen wir einige Kohlenhydrate vorstellen. Die wichtigsten sind hierbei Glucose und Fructose, welche man auch auswendig aufzeichnen können sollte (sowohl die Fischer-Projektion als auch Haworth-Formel). Die anderen Saccharide sind sinnvoll zu kennen und auch zu erkennen....
- Nachweise von SaccharidenEs gibt mehrere Möglichkeiten Saccharide nachzuweisen. Dabei zielt jeder der aufgeführten Nachweise speziell auf eine bestimmte Eigenschaft der Saccharide ab....
- Fette
- Struktur und Nomenklatur von FettenFette sind Derivate des dreiwertigen Alkohols Glycerol (Propan-1,2,3-triol, auch Glycerin genannt). Dieser ist mit Fettsäuren verestert. Eine Fettsäure ist eine Carbonsäure mit einem langen Alkylrest (meist bestehend aus 10-20 C-Atomen und der entsprechenden Anzahl an H-Atomen). Der Reaktionsme...
- Eigenschaften von FettenDa natürliche Fette immer Stoffgemische sind, gibt es keine klar definierten Schmelzpunkte, sondern vielmehr Schmelzbereiche. Wo genau diese liegen, hängt von der Länge der einzelnen Alkylketten des Moleküls ab. Fette bzw. Öle haben jedoch grundsätzlich keine starken intermolekularen Wechselwi...
- Verseifung und TensidwirkungWährend die saure Hydrolyse die exakte Rückreaktion der Veresterung darstellt, ist der basische Zerfall eines Fettes irreversibel. Die Fette werden also durch Laugen gespalten, wodurch Glycerin und Salze der Fettsäuren entstehen. Diese Salze wirken als Seifen, die Reaktion nennt man daher Verseif...
- Fetthärtung und Umesterung bei FettenWie bereits erwähnt, kommen natürliche ungesättigte Fette fast ausschließlich in cis-Konformation vor. Ungesättigte Fette in cis-Konformation besitzen an ihrer Doppelbindung einen „Knick“ im Molekül. Dieser entsteht aufgrund der unterschiedlichen Bindungswinkel zwischen den Kohlenstoffbind...
- Grundlagen der Kunststoffchemie
- Struktur von KunststoffenDie Kunststoffe sind eine Verbindungsklasse mit sehr unterschiedlichen Eigenschaften, was sie für die Industrie sehr interessant macht. Je nach Zusammensetzung können Kunststoffe steinhart oder flexibel sein, flüssig vorliegen oder extremen Temperaturen standhalten. Forscher versuchen Kunststoffe...
- Klassifikation von KunststoffenKunststoffe lassen sich aufgrund verschiedener chemischer Eigenschaften in 3 Klassen einteilen....
- Reaktionen von Kunststoffen
- PolymerisationBei der Polymerisation entstehen - wie der Name schon andeutet - sogenannte Polymere. Ein Beispiel eines Polymers ist im folgenden Strukturformelausschnitt zu sehen: ...
- PolykondensationDie Polykondensation ist eine Reaktion, bei der Monomere unter Wasserabspaltung in Polymere überführt werden. Die Polykondensation kann dabei in zwei Reaktionsmöglichkeiten unterteilt werden, bei denen jeweils Wasser abgespalten wird (Kondensation):1. Reaktionsmöglichkeit: Durch Veresterung von...
- PolyadditionBei der Polyaddition entstehen Kunstharze, die Polyurethane genannt werden. Diese können die folgende Strukturformel aufweisen: ...
- Recycling von KunststoffenViele Kunststoffe werden nach ihrer Nutzung entsorgt und können anschließend wieder recycelt werden, um die verwendeten Rohstoffe ganz oder teilweise zurückzugewinnen und so das Aufkommen an zu entsorgendem Material zu reduzieren.Recycling bedeutet, dass aus Abfallstoffen Rohstoffe oder Energie z...
- Peptide
- Q3 - Das chemische Gleichgewicht
- Chemische Gleichgewichte und ihre Einstellung
- Das chemische GleichgewichtReaktionen, die in einem geschlossenen System – ein System, in dem weder ein Stoff entweichen noch hinzugefügt werden kann - ablaufen, sind oftmals reversibel (können rückgängig gemacht werden). Beispielsweise läuft die Protolyse von Wasser zu OH- und H+ bei konstanten Bedingungen in beide R...
- MassenwirkungsgesetzIn diesem Kapitel wirst du das Massenwirkungsgesetz kennenlernen. Dieses ist ein wichtiges Mittel, um die Lage eines chemischen Gleichgewichtes abzuschätzen. Mithilfe des Massenwirkungsgesetzes ist es außerdem möglich viele hilfreiche chemische Größen wie den pH-Wert zu definieren. ...
- Prinzip vom kleinsten Zwang Das Prinzip vom Zwang (auch Prinzip vom kleinsten Zwang oder Prinzip von Le Chatelier) gibt Auskunft darüber, wie man ein chemisches Gleichgewicht durch äußere Bedingungen in eine bestimmte Richtung lenken kann (Produkt- oder Eduktseite). Wie bereits in den letzten Kapiteln erwähnt, hängt die ...
- Haber-Bosch-Verfahren Das Haber-Bosch-Verfahren ist ein Laborverfahren, um Ammoniak aus Stickstoff und Wasserstoff herzustellen. Das Verfahren wurde von dem Chemiker Fritz Haber und dem Ingenieur Carl Bosch entwickelt. Reaktion:N2 (g) + 3 H2 (g) ↔ 2 NH3 (g)...
- EnthalpieEnthalpie ist per Definition eine Energieangabe, die durch die Einheit Joule (Abkürzung J) angegeben wird. Genauer gesagt handelt es sich bei der Enthalpie um Wärmeenergie, die ein System bei konstantem Druck als Wärme an die Umgebung abgibt oder dieser entzieht. Manche wissen vielleicht schon, ...
- Exkurs: Innere Energie Ein wichtiger Grundsatz in der Chemie ist, dass Stoffe, die eine niedrige innere Energie besitzen, besonders stabil sind. Bei einer Verbrennung wird ein Teil dieser inneren Energie in Form von Wärme an die Umwelt abgegeben. Die innere Energie ist ein Bestandteil der Enthalpie. Allerdings wird hier...
- Exkurs: KalorimeterEin Kalorimeter ist ein Gefäß, ähnlich einer Thermoskanne, das besonders wärme- und druckkonstant ist. Daher kann der in das Kalorimeter gegebene Stoff nicht mit der Umwelt reagieren und somit keine Wärme oder Arbeit nach außen austauschen (geschlossenes System). Das Bombenkalorimeter ist ein ...
- Satz von HessNatürlich gibt es in der Chemie nicht nur einen möglichen Reaktionsweg, um ein Produkt zu erzeugen. Nach dem Satz von Hess ist die Standardbildungsenthalpie eines Stoffes immer gleich und damit unabhängig vom Weg, durch den er erzeugt wurde. Beispielsweise kann CO2 durch zwei Reaktionswege gebil...
- EntropieDie Entropie ist, genauso wie die Enthalpie, eine thermodynamische Größe und findet ihren Ursprung in der Physik. Grundsätzlich beschreibt sie eine Energieänderung pro Temperaturänderung und besitzt daher die Einheit Joule pro Kelvin (J/mol K, Formelzeichen: S). In der Chemie versteht man die ...
- Exkurs: Gibbs-Helmholtz-GleichungDie Gibbs-Helmholtz-Gleichung ist laut Kerncurriculum nicht als verbindlich vorgesehen, wurde aber bereits im Abitur als Transferaufgabe mit Material abgefragt. Daher wird sie an dieser Stelle als Exkurs behandelt. Mit ihr kannst du Aussagen darüber treffen, ob eine Reaktion spontan abläuft oder n...
- Protolysegleichgewichte
- Der pH-WertDer pH-Wert ist ein Maß dafür, wie sauer oder basisch (alkalisch) eine Lösung ist. Die Skala geht von 1 bis 14. Ein pH-Wert < 7 zeigt ein saures Medium an, eine Lösung mit einem pH-Wert > 7 bedeutet, dass sie basisch ist. Hat die Lösung einen pH-Wet von 7, ist sie neutral. ...
- Exkurs: Säure-Base-Haushalt im menschlichen Körper In unserem Körper spielt der pH-Wert und dessen Regulation eine äußerst wichtige Rolle. Dabei ist hervorzuheben, dass einzelne Organe des menschlichen Körpers aufgrund ihrer Funktion verschiedene pH-Werte ausweisen. Diese konstant zu halten, ist für die Funktionsfähigkeit und das Überleben de...
- Säurestärke Nicht alle Säuren (bzw. Basen) dissoziieren vollständig (d.h. sie geben ihre Protonen nicht immer vollständig ab), wenn man sie in Lösung gibt. Wird beispielsweise ein Mol Essigsäure in Wasser gegeben, so wird dieses mit Wasser nicht komplett zu einem Mol Ethanat-Ionen und Oxonium-Ionen (H3O+) ...
- pH-Wert BerechnungDa nicht alle Säuren vollständig dissoziiert vorliegen, kann die Formel pH= - log c(H3O+), die zur Berechnung des pH-Wertes oben aufgeführt wurden, nicht immer angewandt werden. Aus diesem Grund unterscheidet man zwischen starken und schwachen Säuren. Als Faustregel lässt sich sagen, dass alle ...
- Prinzip der TitrationDas Ziel einer Titration (auch Maßanalyse genannt) ist das Bestimmen einer Stoffmenge eines bekannten Stoffes, der in einer Lösung vorliegt. Der zu bestimmende Stoff wird Analyt genannt. Der Analyt wird bei einer Titration durch eine gezielte Reaktion mit einem anderen Stoff, dem Titrant, umgesetz...
- Redoxreaktion: GrundlagenDer Begriff „Redoxreaktion“ setzt sich aus den Worten „Reduktion“ und „Oxidation“ zusammen. Dabei können Oxidation und Reduktion jedoch nie separat stattfinden, sondern immer gleichzeitig. Daher der zusammengesetzte Begriff „Redox“. Genau wie bei der Protolyse-Reaktionen laufen die...
- Aufstellen von Redoxgleichungen Das Aufstellen vollständiger Redoxgleichungen ist ein relativ komplexer Prozess. Daher erklären wir dir diesen im Folgenden anhand mehrerer aufeinander folgender Schritte. Wichtig ist hierbei anzumerken, dass es mehrere Möglichkeiten gibt, wie du am Ende die richtige Redoxgleichung erhältst. Wir...
- Die galvanische Zelle Eine galvanische Zelle oder ein galvanisches Element ist eine Vorrichtung zur spontanen Umwandlung von chemischer in elektrische Energie. Diese Eigenschaft des galvanischen Elements wird in Batterien und Akkus genutzt. Somit kann, wortwörtlich auf Knopfdruck, die in chemischer Form gespeicherte Ene...
- Standardpotentiale und PotenzialdifferenzenDie elektrische Spannung in einer galvanischen Zelle lässt sich mit geeigneten Geräten messen und die Potentialdifferenz zwischen den Halbzellen somit bestimmen. Je nachdem welche Metalle eine galvanische Zelle bilden, liegt eine unterschiedliche Potentialdifferenz bzw. Spannung vor. Um vor der Me...
- Berechnung von PotentialdifferenzenDie Potentialdifferenz einer galvanischen Zelle berechnet sich aus der Differenz der beiden Halbzellenpotentiale. Unter Standardbedingung ist die Berechnung recht einfach, sie ergibt sich aus: ΔE = E0Kathode – E0Anode (E0 = Standardpotential einer Halbzellenreaktion. Die Standartpotentiale kön...
- Elektrochemische Korrosion am Lokalelement Unter Korrosion (von lat. corrodere zersetzen bzw. zerfressen) ist die Reaktion eines Stoffes (meist eines Metalls) mit seiner Umgebung (wie Sauerstoff, Wasser oder Säuren) zu verstehen. Durch diese Reaktion verändert sich der Stoff. Er kann aufgelöst oder stark angegriffen werden. Wie kommt es ...
- Chemische Gleichgewichte und ihre Einstellung
- Grundlagen
- Deutsch
- Halbjahresübergreifende Themen
- Operatoren
- Operatoren - EinleitungEs gibt eine einige Aufgaben, um die man in der Schule – vor allem im Deutschunterricht – nicht herumkommt, nämlich das Schreiben von Texten. Es ist also umso vorteilhafter, wenn man das Grundgerüst jeglicher Textsorten beherrscht und anwenden kann. Obwohl das Verfassen eines Textes grundsä...
- Inhaltsangabe/ZusammenfassungDas Ziel einer Zusammenfassung ist es, einen ursprünglich längeren Ausgangstext deutlich zu reduzieren (auf ca. 1/3 bis 1/4 des Originalumfangs) und in eigenen Worten wiederzugeben, ohne dabei die wesentlichen Aussagen des Textes zu vernachlässigen....
- TextanalyseHierbei gilt es, einen vorgegebenen Text tiefgehend und möglichst substanziell unter die Lupe zu nehmen, sodass ein übergeordneter Sinnhorizont oder versteckte Botschaften erschlossen und eingeordnet werden können. Unterschieden wird zwischen Sachtextanalyse und der Analyse von literarischen Text...
- CharakterisierungEine Charakterisierung versucht, eine Person so komplett wie möglich zu erfassen, indem sie die Merkmale, Beziehungen und Einstellungen einer Figur zusammenstellt und in die Gesamthandlung einordnet....
- Kommentar /Diskussion/StellungnahmeEin Kommentar, genau wie eine Diskussion, eine Stellungnahme oder eine Erörterung, dienen dazu, die eigene Meinung zu einem bestimmten Ereignis, Thema, Vorlagentext oder Ähnlichem schriftlich darzulegen und zu erläutern. Oftmals hat ein Kommentar auch die Absicht, den Leser von der Meinung des Ko...
- GedichtanalyseDa ein Gedicht an sich nichts weiter als die Sonderform eines literarischen Textes ist, orientieren sich auch ihre jeweiligen Analysen aneinander (siehe „Textanalyse“)....
- StilmittelWichtig: Gerade bei der Interpretation von Gedichten, aber auch bei der Analyse von Sachtexten und Reden, sind das Finden und Deuten von Stilmitteln von zentralem Wert. Dazu muss man jedoch erstmal wissen, was überhaupt ein Stilmittel ist und woran man es erkennt. Deshalb gibt es hier eine Zusammen...
- Epochenübersicht
- EpochenübersichtFür jede analytische Arbeit ist es wichtig, den zu analysierenden Text in den Kontext einzuordnen, um ihn in all seinen Facetten erfassen zu können. Es ist außerdem gut zu wissen, dass die Epochen nicht von einem auf den anderen Tag wechseln, sondern sich vielmehr in einem schleichenden Prozess g...
- Aufklärung (~1720-1790)Der Feudalismus löst sich allmählich auf. Die Spannung zwischen den sozialen Schichten führt zu einer Abgrenzung des Bürgertums vom Adel. Besonders beispielhaft sind die Tugend- und Moralvorstellungen des Bürgertums, durch deren strikte Einhaltung sie sich von der Verdorbenheit des Adels abgren...
- Weimarer Klassik (~1786-1805)Die Französische Revolution sowie deren Folgen (Schreckensherrschaft der Jakobiner, Scheitern der Grundforderungen nach Freiheit, Gleichheit und Brüderlichkeit, politische Instabilität in Europa) prägen Goethe und Schiller als Hauptvertreter dieser Epoche nachhaltig. Sie sind überzeugt, dass di...
- Romantik (~1795-1840)Die Romantik kann als Gegenbewegung zu einigen Phänomenen der damaligen Zeit gesehen werden. Politische Auslöser für die Entwicklung der romantischen Ideen waren unter anderem das Scheitern der französischen Revolution sowie die Restauration der absolutistischen Fürstenherrschaft. Hinzu kam die...
- Vormärz (~1830-1848)Die Epoche des Vormärz dauert etwa 30 Jahre, beginnt 1815 mit dem Wiener Kongress und endet durch die 1848 stattfindende Märzrevolution. Der Name der Epoche leitet sich von jenen Geschehnissen vor der Märzrevolution ab....
- Realismus (~1848-1890)Der Realismus löst die Epoche des Vormärz ab. Diese Ablösung ist durch das Scheitern der Märzrevolution zu erklären. Der Begriff Realismus leitet sich von dem lateinischen „realis“ (Wirklichkeit) ab. Ziel ist es daher, Dinge und Handlungen möglichst objektiv und lebensnah darzustellen....
- Expressionismus (~1910-1925)Der Begriff Expressionismus leitet sich von dem lateinischen Wort „expremere“ (deutsch: ausdrücken) ab. Der Expressionismus wird daher auch als „Kunst des gesteigerten Ausdrucks“ bezeichnet. Dieses Ausdrücken bezieht sich auf das Teilhaben der Außenwelt an innerlich gesehenen Wahrheiten u...
- Literatur nach 1945 und 1990In 200 Jahren kann es gut sein, dass die Geschichte der Literatur neue Namen für die Epoche der zweiten Hälfte des 20. Jahrhunderts entwickeln wird. Derzeit orientiert sich die Bestimmung der „Epoche“ an den historischen Einschnitten, die diese Zeit geprägt haben: Das Ende das 2. Weltkrieges...
- Audiovisuelle oder auditive MedienBei jeder Form von Sprache und Medien geht es immer um eine entscheidende Komponente: die Wirkung. Jede Form von Kommunikation, ob persönlich oder über Medien, soll eine Reaktion bzw. eine Wirkung beim Gegenüber auslösen. Diese Reaktion kann im alltäglichen Miteinander eine einfache Antwort sei...
- Sprache und ihre Wirkung in MedienAuch dieser Punkt ist im Kerncurriculum etwas ungenau formuliert. Als Beispiele für Sprache und ihre Wirkung werden Syntax, Semantik und Pragmatik genannt und diese drei Begriffe möchten wir dir hier erklären, damit du sie bei Bedarf je nach Kontext anwenden kannst....
- Realitätskonstruktion in unterschiedlichen MedienformatenAuch hier möchten wir dir die im Kerncurriculum als Beispiel angeführten Medienformate kurz erklären, damit du für den Unterricht bzw. das Abitur das nötige Hintergrundwissen hast. Bei den Medienformaten soll reflektiert werden, wie jeweils die Realität konstruiert wird und auf diese Weise den...
- Sprache und ÖffentlichkeitDie Rubrik „Sprache und Öffentlichkeit“ umfasst einige Themen, die behandelt werden können, aber nicht alle behandelt werden müssen. Dies erkennst du unter anderem daran, dass die verschiedenen Themen mit einem „oder“ getrennt werden und der Kontext, in dem die Themen jeweils behandelt we...
- Frauen- und Männerbild in der LiteraturWährend Geschlechtergrenzen sowie geschlechterspezifische Stereotypen in der heutigen Zeit mehr und mehr reflektiert oder sogar bereits aufgebrochen werden, so waren die Rollen von Mann und Frau in früheren Jahrhunderten durch gesellschaftliche Normen strikt festgelegt. Demnach ist es nicht allzu ...
- Operatoren
- Literatur
- Der Sandmann
- Inhalt - Teil 1: Die Briefe [Anm.: Der Protagonist Nathanael richtet diesen Brief zwar an seinen Freund Lothar, adressiert ihn jedoch (wohl in Gedanken versunken) fälschlicherweise an dessen Schwester Clara, Nathanaels Verlobte.] Zu Beginn dieses Briefs erzählt Nathanael von einer mehr als unliebsamen Begegnung, die ihm verd...
- Inhalt - Teil 2: Die Erzählung Hier gibt sich nun ein Erzähler zu erkennen, der sich als Freund Nathanaels bezeichnet. Er wendet sich direkt an den Lesenden, während er an die Vorgeschichte aus Nathanaels Kindheit nach des Vaters tragischem Tod anknüpft: Infolgedessen seien nämlich Clara und ihr Bruder Lothar, „Kinder eines...
- CharakterisierungenNathanael wird in seiner Kindheit mit einem für ihn äußerst traumatischen Ereignis konfrontiert, welches maßgebend für den gesamten Handlungsverlauf ist, nämlich seine Begegnung mit dem vermeintlichen Sandmann, der angeblich (Kinder-)Augen stehlen soll. Nach jener durchaus grausigen Geschichte...
- Deutungsansätze Im Folgenden werden beispielhaft bestimmte Ansätze, welche im Zuge einer interpretativen Herangehensweise näher behandelt werden könnten, kurz beleuchtet. Sie sollen lediglich als Denkanstöße dienen und demnach ebenso Platz für anderweitige Deutungen einräumen....
- Corpus Delicti
- Inhalt - Teil 1: Von "Das Vorwort" bis "Die ideale Geliebte"Das Verständnis von „Gesundheit“, welche im Handlungsverlauf eine tragende Rolle spielt, wird mithilfe eines Zitats aus einem fiktiven Standardwerk „Gesundheit als Prinzip staatlicher Legitimation“ von Heinrich Kramer, einer der Hauptfiguren, definiert.Die hier zitierte Definition von Ges...
- Inhalt - Teil 2: Von "Eine hübsche Geste" bis "Eine besondere Begabung zum Schmerz"Heinrich Kramer, den Mia als maßgeblichen Verantwortlichen für den Suizid ihrers Bruders ansieht, da er durch medialen Verruf den öffentlichen Druck auf Moritz immer größer werden ließ, besucht sie in ihrer Wohnung. Im Gespräch wird deutlich, dass Kramer weiß, dass Mia ihrem Bruder die Angel...
- Inhalt - Teil 3: Von "Bohnendose" bis "Fell und Hörner, erster Teil"Mia muss sich aufgrund der versäumten Einreichung ihrer Gesundheitswerte einer Untersuchung durch einen Amtsarzt unterziehen, der allerdings keinerlei beunruhigende Auffälligkeiten feststellt. Sie reagiert trotzig und kritisiert, dass sie keine Verbrecherin sei, nur weil sie ihre Daten nicht einge...
- Inhalt - Teil 4: Von "Rauch" bis "In der Kommandozentrale"Während sie mit der idealen Geliebten in Erinnerungen an Moritz schwelgt, zündet sich Mia eine Zigarette an, um gewissermaßen die Nähe ihres Bruders zu riechen. Driss, eine der anderen Hausbewohnerinnen, bemerkt den Rauch, vermutet ein Feuer und schlägt Alarm....
- Inhalt - Teil 5: "Recht auf Krankheit"Die ideale Geliebte schaltet den Fernseher an, in dem gerade die Talkshow „Was alle denken“ vom Journalisten Würmer mit Heinrich Kramer als Gast läuft. Er redet über die Widerstandsgruppe „Recht auf Krankheit“ (kurz R.A.K.) und deren Motivation zur Auflehnung gegen die METHODE. Dabei wird...
- Inhalt - Teil 6: Von "Das Ende vom Fisch" bis "Unzulässig"Eine weitere Rückblende zeigt Moritz und Mia, wie sie in einen als außerhalb der Hygienezone deklarierten Wald gehen. Auch hier wird die kriegsähnliche, militarisierte Umwelt charakterisiert: Die Regierung stellt es unter Strafe, die „Hygienezone“ zu verlassen, um in den Wald zu gehen. Währe...
- Inhalt - Teil 7: Von "Schnecken" bis "Bedrohung verlangt Wachsamkeit"Kramer kommt plötzlich vorbei und tritt zu Mia, Rosentreter (und der idealen Geliebten) hinzu. Er lenkt das Gespräch wieder einmal auf den Fall Moritz Holl, wobei Mia von dessen Liebe zur Natur berichtet und – zu Kramers und Rosentreters Überraschung – erwähnt, dass ihr Bruder an Leukämie l...
- Inhalt - Teil 8: Von "Die Zaunreiterin" bis "Der Härtefall"Die ideale Geliebte spricht Mia ein weiteres Mal auf ihre Unentschlossenheit bezüglich ihres Bruders an und fordert eine klare Positionierung pro Moritz. Innerhalb dieses Gesprächs macht sie deutlich, dass die Anklage Kramers gegen die Methodenfeinde eigentlich Mia direkt gelte und dass sie als Au...
- Inhalt - Teil 9: Von "Das ist die Mia" bis "Wie die Frage lautet"Driss sieht im Fernsehen ein Interview von Mia, in dem die Fehleranfälligkeit der METHODE thematisiert wird. In diesem lehnt Mia wieder eine klare Positionierung ab, als sie nach der Legitimation der METHODE gefragt wird, macht aber ihre kritische Haltung insofern deutlich, dass sie beteuert, diese...
- Inhalt - Teil 10: Von "Vertrauensfrage" bis "Geruchlos und klar"Kramer sieht in Mias Stellungnahme das Potenzial, dem Volk dadurch eine Art Vertrauensfrage stellen zu können, die das System bestärken könnte. Dies verunsichert Mia. Nachdem Kramer gegangen ist, verlässt auch die ideale Geliebte Mia, da sie ihr Ziel, Mia von Moritz' Unschuld zu überzeugen, nun...
- Inhalt - Teil 11: Von "Würmer" bis ",Es' regnet"In einer weiteren Verhandlung, die diesmal von Richter Hutschneider geleitet wird, weil Sophie wegen Befangenheit vom Fall abgezogen wurde, soll der ehemalige Fernsehmoderator Würmer als Kronzeuge verhört werden, der gesteht, Mia mehrfach in der „Kathedrale“ getroffen zu haben. Weiterhin sagt ...
- Inhalt - Teil 12: Von "Dünne Luft" bis "Zu Ende"Kramer kommt ein weiteres Mal zu Mia, findet sie in einem körperlich desolaten Zustand vor und wäscht ihr das Gesicht mit einem Essigschwamm. Obwohl Mia so geschwächt ist, dass sie kaum aus eigener Kraft sitzen kann, muss Kramer feststellen, dass sie der Folter widerstanden hat und nicht von ihre...
- Autorin: Juli ZehDie Juristin und Schriftstellerin Juli Zeh wuchs als Tochter eines Juristen und einer Übersetzerin in Bonn auf. Ihr Studium der Rechtswissenschaften zog sie dann im Jahr 1993 zunächst nach Passau, bevor sie drei Jahre später nach Leipzig umsiedelte, um dort Literatur zu studieren. Hier führte si...
- CharakterisierungenMia Holl ist eine 34-jährige Biologin, deren bisheriges Leben von den staatlichen Behörden gar als „Idealbiographie“ bezeichnet wird. Allerdings wird sie stets von der Trauer um ihren verstorbenen Bruder Moritz begleitet, dessen Selbstmord sie vor allem dem Journalisten und Methodenanhänger H...
- DeutungsansätzeEin zentraler Bestandteil des Romans ist zweifelsfrei seine politisch geprägte Ebene. Das hier dargestellte Gesellschaftssystem einer nahen Zukunft zeichnet sich vor allem durch die technologisch immer versierteren Formen von Überwachung aus, welche es sich vor allem zum Ziel gesetzt haben, die Ge...
- Woyzeck
- ÜbersichtGeorg Büchners Fragment „Woyzeck“ gehört zu den wichtigsten Dramen der deutschen Literatur. Beim ersten Lesen fragt man sich einerseits, warum ausgerechnet dieses Stück so bekannt ist, und andererseits, ob es absichtlich fürs Abitur ausgewählt wurde, um Schüler zu ärgern. Die unverständl...
- Inhaltsangabe Teil 1: "Freies Feld, die Stadt in der Ferne" bis "Die Stadt" Auch wenn es sich bei den einzelnen Szenen des Dramas um viele kleine, auf den ersten Blick unzusammenhängende Ereignisse handelt, typisch für das offene Drama, gibt es doch einen Haupthandlungsstrang, der die einzelnen Figuren und deren Erlebnisse miteinander verbindet: Die Fragen „Warum bringt...
- Inhaltsangabe Teil 2: "Buden, Lichter, Volk" bis "Kammer"Woyzeck besucht zusammen mit Marie den Jahrmarkt im Dorf. Ein alter Mann singt vom Sterben und spielt dazu die Leier, während ein Kind dazu tanzt. Es herrscht ausgelassene Stimmung und Woyzeck scheint in besserer Konstitution zu sein. Ein Ausrufer führt tierische Kuriositäten vor, wobei er die Ä...
- Inhaltsangabe Teil 3: Von "Der Hauptmann. Woyzeck" bis "Kammer"Woyzeck rasiert wortkarg den Hauptmann, während dieser philosophiert und seinen Untergebenen mit seinen Problemen belastet. Durch den Mangel an Krieg leidet der Hauptmann unter Langeweile und Beschäftigungslosigkeit, sodass er sein Leben nahezu für sinnlos hält und glaubt, man habe auf der Welt ...
- Inhaltsangabe Teil 4: Von "Auf der Gasse" bis "Beim Doktor"Marie und Woyzeck begegnen sich auf der Straße, wobei Woyzeck in einer Art fiebrigem Wahn gefangen zu sein scheint. In diesem ahnt er Maries Untreue. Statt seinen Verdacht geheimzuhalten, spricht er sie darauf an: „Adieu, Marie, du bist schön wie die Sünde. Kann die Todsünde so schön sein?“...
- Inhaltsangabe Teil 5: Von "Straße" bis "Die Wachstube"Doktor und Hauptmann gehen gemeinsam die Straße entlang, wobei das stramme Tempo des Doktors den Hauptmann ordentlich aus der Puste bringt. Dieser hält ihm den gleichen Vortrag wie Woyzeck, dass ein so gehetztes Gehen von einem schlechten Menschen zeugt. Als er den Doktor endlich zu fassen bekommt...
- Inhaltsangabe Teil 6: Von "Wirtshaus" bis "Wirtshaus"Durch das Fenster eines Wirtshauses sieht Woyzeck Marie und den Tambourmajor miteinander tanzen und sieht ein, dass Marie für ihn verloren ist: „Wie er an ihr herumtappt, an ihrem Leib, er, er hat sie wie ich zu Anfang!“In dieser Szene ist auf inhaltlicher Ebene vor allem relevant, dass Woyzeck...
- Inhaltsangabe Teil 7: Von "Kramladen" bis "Der Hof des Doktors"Woyzeck lässt seinem Mordplan Taten folgen und geht zu einem Juden, um eine Mordwaffe zu kaufen.Da ihm die Pistole zu teuer ist, kauft Woyzeck sich ein Messer, das „mehr als Brot schneide“ kann.Diese Szene hat, trotz ihrer Kürze, wieder symbolische Tragkraft: Woyzecks absolute Selbstaufgabe wi...
- Inhaltsangabe Teil 8: Von "Marie mit Mädchen vor der Haustür" bis "Abend. Die Stadt in der Ferne" Marie sitzt zusammen mit drei Kindern und der Großmutter vor der Haustür. Nachdem die Kinder zuerst gemeinsam gesungen, dann mit Marie getanzt haben, erzählt die Großmutter auf Maries Bitten ihr und den Kindern das Märchen vom Sterntaler als Anti-Märchen mit traurigem Ende: „und war ganz all...
- Inhaltsangabe Teil 9: Von "Es kommen Leute" bis "Woyzeck an einem Teich"Zwei Personen hören unheimliche Geräusche „wie ein Mensch, der stirbt“ und laufen zum Tatort....
- Inhaltsangabe Teil 10: Von "Straße" bis "Der Idiot. Das Kind. Woyzeck"Kinder erzählen einander, dass eine Leiche „in dem Wäldche, am roten Kreuz“ gefunden wurde. Die Kinder beeilen sich, um zu dem Schauplatz zu kommen, denn sie befürchten, dass die Leiche schon weggetragen worden sein könnte, bevor sie einen Blick auf sie erhaschen konnten. Hier kritisiert Bü...
- Der „wahre“ WoyzeckBüchner griff bei seinem Drama „Woyzeck“ auf einen realen Kriminalfall zurück, der zu seiner Zeit viel Aufmerksamkeit in der Öffentlichkeit erregte. Der am 3. Januar 1780 in Leipzig geborene Johann Christian Woyzeck, Sohn eines Perückenmachers, erstach am 21. Juni 1821 aus Eifersucht seine ...
- Charakterisierungen: Franz Woyzeck und Marie ZickwolfBüchners Protagonist ist ein Soldat und Vertreter des einfachen Volkes. Er ist 30 Jahre alt und lebt in einer Partnerschaft mit Marie – eine Hochzeit ist aus finanziellen Gründen nicht möglich. Die beiden haben ein uneheliches Kind namens Christian und Woyzeck zahlt von seinem geringen Sold und...
- Charakterisierungen: Andres und TambourmajorAndres ist Soldat und Woyzecks Kamerad sowie Zimmergenosse beim Militär. Er singt häufig und wirkt unbekümmert. Woyzeck scheint ihm nahezustehen, da er ihm sein Erbe anvertraut. Trotzdem nimmt Andres die Sorgen von Woyzeck nicht ernst, obwohl dieser ihm mehrmals seine Unruhe mitteilt. Dies ist ih...
- Charakterisierungen: Doktor und HauptmannDer Doktor ist ein Vertreter der gebildeten Oberschicht und führt an Woyzeck Experimente durch. Er hat kein persönliches Interesse an Woyzeck und kümmert sich nicht um dessen Gesundheit – seine Versuche haben Vorrang vor dem körperlichen Wohlergehen Woyzecks. Damit wird er als Vertreter der Wi...
- Figurenkonstellation und NamenEs gibt zwei Gruppen in Büchners Drama, die sich gegenüberstehen. Die Mächtigen werden repräsentiert von den Angehörigen der Oberschicht, dazu gehören der Hauptmann und der Doktor. Den Kontrast bilden die Angehörigen der Unterschicht, dazu zählen Woyzeck, Marie, ihr Kind Christian und Andres...
- Aufbau des TextesDas Stück Woyzeck zeigt Merkmale eines Stationendramas. Das bedeutet, dass einzelne Szenen, die meist nur lose miteinander verbunden sind, aufeinander folgen. Das Stationendrama ist eine Form des offenen Dramas, das im Gegensatz zu einem Regeldrama nicht in Akte gegliedert ist. Stattdessen stehen d...
- Stil und SpracheHierbei handelt es sich um Dialoge, bei denen die sprechenden Personen quasi aneinander vorbeireden statt ein Gespräch miteinander zu führen. Die Dialoge ähneln eher Monologen und auch die Lieder bzw. Märchen, die Büchner immer wieder einbaut, machen ein funktionierendes Zwiegespräch unmöglic...
- Zeitgeschichtlicher Hintergrund und heutige Bedeutung1813 wurde bei der Völkerschlacht bei Leipzig Napoleon I. besiegt und die europäischen Machtverhältnisse bekamen eine Neuordnung. 1815 wurden durch den Wiener Kongress die Staatsverhältnisse, die vor der Französischen Revolution 1789 herrschten, wieder eingeführt. Es gab somit keinen deu...
- InterpretationsansätzeZu guter Letzt werden wir dir einige Interpretationsansätze vorstellen. Natürlich gibt es die verschiedensten Möglichkeiten „Woyzeck“ zu deuten und deinen eigenen Ideen sind keine Grenzen gesetzt – du musst sie nur gut begründen und wenn möglich mit Zitaten aus dem Stück belegen sowie de...
- Mario und der Zauberer
- InhaltsangabeIn der Novelle „Mario und der Zauberer – Ein tragisches Reiseerlebnis“, welche von Thomas Mann verfasst und im Jahre 1929 veröffentlicht wurde, dient bereits der erste Absatz gleichsam als Zusammenfassung der gesamten Handlung, indem das besagte Reiseerlebnis vom Erzähler aus der Perspektive...
- CharakterisierungenDer Zauberkünstler Cipolla ist mit seiner Vorführung maßgeblich dafür verantwortlich, dass sich das Reiseerlebnis des Erzählers endgültig ins Tragische wendet. Cipollas Darbietung füllt den zweiten Teil der Novelle und soll eigentlich für den Erzähler sowie dessen Familie als freudige Ablen...
- Deutungsansätze Die Novelle ist zweifelsfrei durchzogen von einigen Momenten, welche man ethisch oder auch politisch lesen kann und die Handlung – sowohl im ersten als auch im zweiten Teil – in jedem Fall jedoch auf ihre Art maßgeblich prägen. Der besagte erste Teil stellt den Urlaub des Erzählers und seine...
- Faust - Der Tragödie erster Teil
- EinleitungDie Tragödie „Faust”, geschrieben von Johann Wolfgang von Goethe und veröffentlicht im Jahr 1808, ist auch heutzutage noch als das Werk eines deutschen Schriftstellers schlechthin anzusehen. Es gibt zwei Teile des Dramas („Faust I“ bzw. „Faust. Der Tragödie erster Teil“ und „Faust I...
- Inhalt - Abschnitt 1: Drei Vorspiele Die beiden ersten Szenen des Stücks haben keine funktionale Rolle für die eigentliche Rahmen- und Binnenhandlung. Allerdings bieten sie einen wichtigen Einblick in die Denkweise Goethes. Er reflektiert hier sowohl über seine Rolle als Dichter, über seine eigene Entwicklung und seine Werke als au...
- Inhalt - Abschnitt 2: Die Gelehrtentragödie IFausts unbefriedigendes Dasein als Gelehrter verleitet ihn zu drastischen Maßnahmen und macht ihn für teuflische Mächte empfänglich. Die Gelehrtentragödie beginnt bei den meisten Strukturdarstellungen mit der Nacht und endet – zumindest für den ersten Teil – mit der Hexenküche. Hierbei is...
- Inhalt - Abschnitt 2: Die Gelehrtentragödie IIFaust beschließt nach der Unterhaltung die sich bietende Gelegenheit zu nutzen und mit Wagner einen österlichen Spaziergang vor den Toren der Stadt, also in der Natur und unter den einfachen Leuten zu machen. Zu Beginn der Szene lernen wir eine große Bandbreite der mittelalterlichen Gesellschaft ...
- Inhalt - Abschnitt 2: Die Gelehrtentragödie IIIWie angekündigt, sucht Mephisto Faust erneut auf, um diesmal sein Ziel (Faust zu seinem Spielball in der Wette mit Gott zu machen) zu erreichen. Interessant ist, dass er nicht wieder als Scholastikus auftritt, sondern als „edler Junker“, also als Adeliger. Dies hat, so Mephisto, die Funktion, F...
- Inhalt - Abschnitt 2: Die Gelehrtentragödie IVAls erste Station steuern die zwei Auerbachs Keller in Leipzig an. Dort soll Faust zunächst ein paar Eindrücke von dem Leben gewinnen, das die einfachen Leute führen. In Auerbachs Keller treffen sie auf vier Studenten, die mit Wein in munterer Stimmung feiern. Allerdings kann Faust nicht wirklich...
- Inhalt - Abschnitt 3: Die Gretchentragödie IFaust und Gretchen lernen sich durch die tatkräftige Unterstützung Mephistos kennen. Ihr Verhältnis führt zu einer dramatischen Entwicklung mit drohender Hinrichtung Gretchens. Wie bereits angedeutet, ist die Gretchentragödie sowohl für sich genommen ein eigener und unter diesem Aspekt zu betr...
- Inhalt - Abschnitt 3: Die Gretchentragödie IIMephisto berichtet Faust von seinem Ärger über Gretchens Mutter. Unglücklicherweise hat Gretchens Mutter ihr den Schmuck sogleich wieder weggenommen, da er nicht zu deren bescheidenem, gottgefälligem Lebensstil passt (V. 2813ff) und sie die teuflische Herkunft erahnt hat. Darüber habe sich Gret...
- Inhalt - Abschnitt 3: Die Gretchentragödie IIIBeim erneuten Treffen fragt Margarete Faust, wie er zum Thema Religion steht (V. 3415). Sie stellt ihm die so genannte Gretchenfrage: „Nun sag, wie hast du´s mit der Religion?“ Diese Frage Gretchens an Faust ist so bekannt geworden, dass auch heute Fragen dieser Art als „Gretchenfrage“ beze...
- Inhalt - Abschnitt 3: Die Gretchentragödie IVDerweil führt Mephisto Faust ins Harzgebirge auf den Blocksberg, wo die Hexen ausgelassen und zügellos die Nacht zum ersten Mai feiern. Tatsächlich lässt sich Faust schon auf dem Weg vom Treiben faszinieren, er will sogar ganz nach oben, um das Böse tiefgehend studieren zu können. Die Walpurgi...
- Figuren - Teil 1Die folgenden Charakterisierungen beschränken sich auf die wesentlichsten Aspekte der relevantesten Figuren. Sie dienen daher nicht als vollwertige Charakterisierungen im eigentlichen Sinn, sondern stellen vielmehr eine Übersicht der wichtigsten Charaktereigenschaften dar....
- Figuren - Teil 2Gretchen, Fausts Kosename für Margarete, ist ein junges Mädchen von 14 Jahren, das sich besonders durch Frömmigkeit und Sittlichkeit auszeichnet, bis sie mit Faust und Mephisto in Berührung kommt. Ihre häuslichen Verhältnisse sind eher bescheiden, obwohl sie zumindest „einen gewissen Wohlsta...
- Formaler Aufbau „Faust”, besonders der erste Teil, ist zwar rein von seiner Entstehungszeit aus betrachtet ein Drama aus der Weimarer Klassik, hat aber strukturell mehr zu bieten als ein rein klassisches (geschlossenes) Drama nach Aristoteles und richtet sich damit eher nach der Formrevolution des Sturm und Dra...
- Epochentypische MerkmaleDa Goethe an „Faust“ über mehrere Jahrzehnte arbeitete, haben ihn zwangsläufig die Einflüsse verschiedenster Epochen geprägt. Romantische Ideale haben ihn während der Entstehungszeit von Faust beeinflusst, allerdings waren vor allem die Gedanken der Klassik und des Sturm und Drang (damit ve...
- InterpretationsansätzeDie wichtigste Deutung, nämlich dass das Werk der Versuch Goethes ist, die Frage „Was ist der Sinn der göttlichen Schöpfung, vor allem des Menschen?“ in seinem Sinne zu beantworten, ist zu umfangreich, als dass sie hier zusammenfassend dargestellt werden könnte. Die einzelnen Aspekte wurden ...
- Der Sandmann
- Halbjahresübergreifende Themen
- Englisch
- Q1 - Ideals and realities
- The USA – the formation of a nation
- Development and principles of American democracy and the Constitution - The founding of the United States of America In the context of the development and principles of American democracy and the Constitution as well as the concept of “American exceptionalism,” it is necessary to start with the beginnings of settler colonialism on the American continent and the Puritans who fled from religious persecution in E...
- Development and principles of American democracy and the Constitution - First constitutional documents and principlesOn 7thJune,Richard Henry Lee, a Virginina, asked the Continental Congress in Philadelphia to consider declaring independence from Great Britain. The Congress appointed a committee of five to write the formal declaration. Thomas Jefferson wrote the first draft of “The Declaration of Independence”...
- Landmarks of the American history - African-American history and Civil Rights MovementIn 1807, the slave trade in America was declared illegal for the first time. At the same time, tensions between anti-slavery and pro-slavery states began to rise, which were also triggered by the Missouri Compromise. The Missouri Compromise (1820) regulated the political status of newly founded stat...
- Landmarks of the American history - Industrialisation, Era of Great Depression, international conflictsAs described above, America declared its independence from Great Britain in 1776. However the countries were still connected through the Triangular Trade. The triangular trading system existed between America (known as New England), Great Britain and the African continent. The trade consisted of En...
- Recent political and social developmentsDonald John Trump – born 1946 – is an American businessman, entertainer and the 45th president of the United States. Trump is famous for posting statements on Twitter and he thrives on the attention given to him by the media. (Currently, Trump is not able to use Twitter since his account has bee...
- Living in the American society
- The American way of life and American values and beliefs The American way of life is based on the idea and principles of the American Dream, which includes individual freedom, the pursuit of happiness, hard work, striving for higher standards and fulfilling traditions. The American way of life describes the attitudes and the habits of most Americans and i...
- Migration and the American Dream - America as a country of immigrationAmerica is one of the most famous countries in terms of immigration and cultural diversity. Because America is known as the country of unlimited opportunities, migrants from all over the world have immigrated to the United States. It is important to note the historical context of people from Western...
- Migration and the American Dream - Melting pot and Salad bowlAsian Americans:In the 1950s/60s, a large crowd of Asian immigrants came to America. Asian immigration cannot be generalised because completely different groups from all over Asia have immigrated to the US. Japanese, Chinese, Korean, Filipino, Indian, Pakistani and Vietnamese immigrants do not form ...
- Manifestation of individualism
- Concepts of life in AmericaThe concepts of life in America are known as the principles of life, liberty and the pursuit of happiness. These principles have been executed in different periods of time and in different ways. Nevertheless, the concepts of life cannot be specified because in different historical situations, people...
- American Dream as a manifestation of individualism - American FrontierDefinition: The belief that anyone in the US has the chance to be successful and happy if they work hard enough in order to gain the opportunity for upwards mobility.Quote:“[The] American Dream [is] the dream of a land in which life should be better and richer and fuller for every man with opportu...
- American Dream as a manifestation of individualism - The American characterThe US became a major power at the beginning of the 20th century due to its large and rich territory, a growing population, an emerging industry strengthened by technological advances and the opportunity, as well as the political will, to assert this power. The Platt Amendment (1901) declared that t...
- Visions and nightmaresThe American Dream has been widely criticised, and is sometimes referred to as the American Nightmare. The American Nightmare stipulates that the American dream is nothing but an illusion and says that the pursuit of success, happiness and liberty is unrealistic in most circumstances and societies. ...
- Stories of InitiationInitiation means the introduction of a young person into any human society by instruction [dt. (hier): Anleitung] about its principles, rules and mysteries. It is a process of coming of age and describes the passage from childhood to maturity. Becoming a member of the adult world is a natural p...
- To kill a mockingbird
- Author and historical contextHarper Lee was born in Alabama in 1926 as the daughter of Amasa Coleman Lee and Frances Cunningham Finch. She studied law before she decided to become a writer and returned from Great Britain to New York. Lee published "To kill a Mockingbird" in 1960 when the Civil Rights Movement became effective. ...
- Summary Chapters 1-11Scout, the narrator, introduces the reader to her familial circumstances and provides an introduction to Maycomb society. Atticus Finch studied law and did not remain at the landing as his sister did. Jem, Scout and Dill are fascinated by their neighbours’ estate, especially by Boo Radley, who has...
- Summary Chapters 12-31Calpurnia takes the children with her to an African American church where they learn about Tom Robinson; the church is already collecting money for his family. Scout and Jem experience the unfairness of segregation – the separation of black and white people. They notice that nearly all African Ame...
- CharactersScout is the first-person narrator in "To kill a Mockingbird". When she is an adult, she tells the story in retrospect as a six-year- old child. She is considered to be bright for her age and she loves to read. Scout gets in trouble with her teacher, who expects Scout to learn in conventional ways. ...
- Themes and InterpretationThe story is set in the 1930s; it occurs during the Great Depression (economic crisis) and before the Civil Rights Movement. It is primarily about the social problems associated with racism and prejudice towards African Americans. The title “To kill a Mockingbird” is derived from the saying that...
- Overview of the American historyThe following aspects summarise the most important incidents in American history including the history of immigration and depicting the visions and nightmares concerning the American Dream. It is not necessary to know every date of every incident, but the thickly marked words should be known. To put...
- The USA – the formation of a nation
- Q2 - The encounter of cultures
- Great Britain – past and present: the character of a nation
- Great Britain – Tradition and Change Great Britain: Scotland, England, Wales United Kingdom: Scotland, England, Wales, Northern Ireland The UK is one country consisting of four former independent countries. England took over Wales in 1542 and in 1707, the Act of Union was signed, which united England and Scotland, too. The Irish War o...
- DevolutionDevolution describes the shift of Great Britain’s legislative power from the UK parliament to elected representations in Scotland, Northern Ireland and Wales. England does not have its own parliament. In England, policies concerning health, schools, housing, agriculture, environmental protection, ...
- Britain and the EU – BrexitDespite signing the Maastricht Treaty about the European Union in 1991, Great Britain still refused to completely attach to the EU. This can be seen in several aspects like the currency: the euro was never introduced in Great Britain. Moreover, Britain did not agree with opening the boarders as stip...
- British Empire - ImperialismDefinition: Describes a major power’s desire to extend its ideological, political, military and economic influence far beyond the state’s national borders. Expansion can be achieved by making weaker countries economically, politically and culturally dependent on the stronger country. The Briti...
- British Empire - IndustrialisationDefinition: Describes an economic and cultural shift from home-based production and traditional agriculture to a system of factory-based manufacturing including modern technologies, other energy sources and developments in transportation. First Industrial Revolution (the 1700s-1800s): production in...
- British Empire - ColonisationDefinition: Describes the domination of a country by a major power of a different culture, whereupon the colonised country and inhabitants are dependent, exploited and controlled by military subjugation and political, economic and cultural influence. From the 16th century on, the British began to ...
- British Empire - CommonwealthThe Commonwealth, founded in 1926, is an association of the UK and its former colonies. The members are not colonies anymore, but free and independent nations. The main purpose of the Commonwealth is to preserve the connection to the British Empire through strong partnership and trade. The table sum...
- Being BritishNational identity describes a set of factors that connect individuals and groups under one nation. Such factors can be communal beliefs, behaviours, mannerisms, emotional attachments, and typical ways of thinking or acting. There are multiple interpretations of what being “British” really means...
- Elizabethan England The Elizabethan Era (1558 – 1603) is the epoch in the Tudor period of the history of England during the reign of Queen Elizabeth I. It was marked by/can be characterized by threats of invasions by France and Spain, fighting Ireland and the Netherlands, the outbreaks of the plague as well as conspi...
- Ethnic diversity
- Great Britain as a multicultural societyRobin Cook, politician of the British labour party, believed that it was not possible to split Britishness and multiculturalism because being British is actually based on diverse multicultural influences. Multiculturalism: a social term that encompasses multiple ethnicities that interact with each o...
- Prejudice and the one-track mindDefinition: Prejudice Is a preconceived, non-objective opinion that is not based on reasons or own experience As it is already described in the definition, prejudices are unfair and unreasonable feelings or opinions that are often established without enough thought or knowledge. Often and especially...
- Integration versus assimilation Since it is important to distinguish between the terms ‘integration’ and ‘assimilation’ in the context of multiculturalism, you should/need to be able to define both terms. Integration: Different ethnicities share values. Minorities are accepted and protected by the law. Assimilation: D...
- Literature concerning multi-culturalism and ethnic diversity
- The Embassy of Cambodia
- Author and historical contextZadie Smith was born in Willesden, London in 1975 and grew up with parents of British and Jamaican descent. When her parents got divorced Smith concentrated her energy on writing short stories. After completing school, Smith went to Cambridge University and studied English Literature until 1997. ...
- Summary Chapter 1 - 10The Embassy of Cambodia is a miniature novel of 21 short chapters written by Zadie Smith. At first, the text was published in The New Yorker journal in 2013. Through the description of the Ivory Coast [dt.: Elfenbeinküste] immigrant Fatou who fled to London illegally, Zadie Smith illustrates the li...
- Summary Chapter 11 - 21Fatou and Andrew wait for the rain to stop in the café, but as it continues to rain, they decide to leave and go to the train station together. Until then, they shared an umbrella. When Andrew insists that Fatou takes his umbrella, she refuses and puts on her bathing cap. As they leave, they kiss e...
- CharactersFatou is an African woman from the Ivory Coast and comes to London as an economic refugee to work as domestic help for the Derawals. Fatou embodies the image of modern slavery in The Embassy of Cambodia. From the former French Ivory Coast, Fatou and her father travel to former British Ghana. They b...
- Themes & InterpretationsPrimarily, “The Embassy of Cambodia”, written by Zadie Smith, deals with lawlessness and exploitation in the context of multiculturalism at the beginning of the 21st century. The story focuses on the dysfunctionality of multiculturalism and the emergence of parallel societies. In Willesden’s ...
- My son the fanatic
- “My son the fanatic”: a story about a clash of cultureHanif Kureishi (born 1954) is a British Pakistani writer, screenwriter and director. Kureishi is the son of a British mother and a Pakistani father who came to London in 1950 to study law. Kureishi’s father belonged to the first generation of Pakistani immigrants. Later he worked for the Pakistani...
- Shooting an Elephant
- “Shooting an Elephant”: a story in times of colonialism - Author, Historical Background, SummaryGeorge Orwell is the pen name of Eric Arthur Blair, a novelist, essayist and critic. He spent his childhood in England, where he attended Eton College from 1917 to 1921. In Burma, today’s Myanmar, the 19-year-old introduced himself as a colonial police officer. The short story “Shooting an Elep...
- “Shooting an Elephant”: a story in times of colonialism - InterpretationCentral aspects of “Shooting an Elephant” are colonialism and the imperialists' exercise of power over their subjects . Above all, the coexistence of both sides play a role. The story not only addresses the role of the despots on the indigenous population, but also how the despots are viewed by ...
- The Embassy of Cambodia
- The English-speaking world: Country of reference: Ireland
- The English-speaking world - Country of reference - Ireland: Irish historyThe Island of Ireland is made up of two countries: the Republic of Ireland and Northern Ireland. The Northern part of the land, called Northern Ireland, is part of the United Kingdom. 80 percent of the landmass of the island belongs to the Republic of Ireland....
- The English-speaking world - Country of reference - Ireland: Irish history and National IdentityThe ethnologic-political conflict between the Protestant unionists (loyalists) and the Roman Catholic nationalists (republicans) reached the climax in 1968. The duration of The Troubles, known as the Northern Ireland conflict, is dated from the 1960s to 1998. It consisted of the dispute between the ...
- Overview of the British history The following table gives a short overview of the British history and is a leitmotif for the most important incidents in Britain’s history. It is not necessary to know every date of every incident, but the thickly marked words should be known. To put incidents in context, it is helpful to know th...
- Great Britain – past and present: the character of a nation
- Q3 - Challenges of our time
- Human dilemmas in fiction and real life
- Extreme situationsAn extreme situation is a special or unconventional situation. Human beings often react to extreme situations with extreme behaviours, which can then result in unwanted consequences. There are various factors which can transform a normal situation into an extreme situation. Psychological factors, su...
- Being differentHuman beings are inherently social and gregarious. They need social contacts and positive interactions. Hence, they want to be a part of a society in order to fulfil their social needs. However, most societies have their own rules and belief systems and might not be welcoming to people who are diffe...
- Modelling the future
- Power and ambitionPower and ambition are closely connected. People who have power but do not have any ambitions might lose their position to someone who is simply more ambitious. An ambitious person is someone who has a strong mindset and who will execute the necessary steps in order to achieve a desired goal. An am...
- Science and technologyDefinition science: Science can be defined as the empirical study of structural and behavioral aspects of the physical world.Definition technology: Technology refers to methods, systems, and devices which are the result of scientific knowledge being used for practical purposes.Quote: “It is the fu...
- Possibilities and responsibilitiesScientists specialise in various fields of research. Through research, scientists have developed various systems and technical instruments to make everyday life easier and more comfortable. However, each finding comes with risks and benefits and it needs to be ensured that the benefits always outwei...
- Main inventions in the last few decades Part 1General information: Many scientists contributed to the commercialisation of electricity. Thomas Edison invented the electric light bulb around 1878. However, the idea of static electricity goes back to the Ancient Greeks (600 BC).Pro – argumentContra – argumentElectricity majorly contributes t...
- Main inventions in the last few decades Part 2General information: Karl Benz filed for a patent for his “Motorwagen” in 1885. It had three wheels and was similar to what we consider to be a car. Even before the invention of a “Motorwagen” people had thought about the possibility of cars. Also, in the 19th century electric cars were alre...
- Main inventions in the last few decades Part 3General information: Computer: The first computing device was invented by Charles Babbage in 1822 and it was used for calculations. The efforts of Microsoft, Apple, and other companies resulted in what we know as computers today. Smartphone: IBM introduced the first smartphone in 1992, which had li...
- Main inventions in the last few decades Part 4General information: Genetic engineering describes the alteration of the DNA of an organism. By manipulating the DNA of an organism, it is possible to activate new genes. Genetic Engineering on humans: Decide the sex, eliminate the risk of genetic diseases and change the appearance (designer babie...
- Main inventions in the last few decades Part 5General information: Artificial Intelligence (AI) can be understood as machines and computers that imitate human intelligence. What is intelligence? Most authors define intelligence with these three traits: The ability to work with abstract concepts. The ability to solve problems. The ability to l...
- Gender issues
- Gender and identity - Gender construction For a long-time, sex and gender were used synonymously. However, nowadays, these terms are considered to be distinct terms. Sex refers to the biological differences between female and male, whereas gender is considered to be a performative act, which situates a person on a spectrum ranging from femi...
- Culture and gender – now and then - the ideal beauty of women over timeShall I compare thee to a summer’s day? Thou art more lovely and more temperate: Rough winds do shake the darling buds of May, And summer’s lease hath all too short a date: Sometime too hot the eye of heaven shines, And often is his gold complexion dimm’d; And every fair from fair sometime ...
- Nature and the environmentTwo of the biggest environmental issues the world faces today are plastic pollution and global warming. 1. Plastic Pollution: In our day and age, plastic is used in various products; however, it decomposes slowly. More and more plastic ends up in the ocean, which is unquestionably dangerous for aqua...
- Globalisation Globalisation refers to the process of the worldwide integration of economy, communication, politics and many other sectors. The world has become a global village, which means that different countries and companies can work together more easily, but it also means that regional and national problems ...
- Othello
- SummaryOthello is a play written by William Shakespeare in 1604. It is one of the four great Shakespearean tragedies, the other three being Hamlet, Macbeth, and King Lear. What sets Othello apart from the other three tragedies is the vicious villain Iago. Due to Iago’s plotting and Othello’s complexes,...
- CharactersOthello is the protagonist of the tragedy. He is a black man from Africa who has gained the position of a general in the Venetian Army due to his skills. He is very confident as he is aware of how crucial he is for the Venetian forces. “Let him do his spite: My services which I have done the signi...
- Themes and Interpretation1. Racism Othello is a black man. He is constantly called “the Moor”, which puts him into a category and gives the audience an insight into how commonly racism is practiced in their society. In the beginning, Brabantio’s hidden racist thoughts come to light. It is said that Brabantio liked Ot...
- Human dilemmas in fiction and real life
- Additional Literature
- Mother To Mother
- Author and SummaryThe Author of “Mother to Mother”, Sindiwe Magona, was born and raised with seven siblings in Gugulethu, a township near Cape Town in South Africa. She worked as a domestic aid before graduating at a correspondence school. After working as a primary school teacher for a while, she finished with a...
- CharactersMandisa is a black woman living in the township Gugulethu near Cape Town. She has three children, each of them has a different father. At the time the novel takes place, she is married to Dwadwa, the father of her daughter Siziwe. Mandisa is Mxolisi’s mother, he is the murderer of Amy Biehl. She ...
- Themes and InterpretationThe system of Apartheid was a system of racial segregation, imposed by the white government in South Africa in the 20th century. The novel “Mother to Mother“ is set in this time of oppression. The political measures and the effects they have on the society are depicted in a very pure but emotion...
- Mother To Mother
- Q1 - Ideals and realities
- Ernährung
- Stoffwechsel
- Kohlenhydrate
- Funktion von KohlenhydratenKohlenhydrate werden auch Saccharide genannt und sind eine sehr große Naturstoffklasse. Sie bestehen hauptsächlich aus Kohlenstoff-, Wasserstoff- und Sauerstoffatomen. Aufgrund dieser Hauptbestandteile haben sie ihren Namen „Kohlenhydrat“ erhalten. Mengenmäßig sind sie der wichtigste Energie...
- AufbauKohlenhydrate bestehen aus den Elementen Kohlenstoff (C), Wasserstoff (H) und Sauerstoff (O). Allgemein wird ein Stoff als Kohlenhydrat bezeichnet, wenn er wenigstens drei Kohlenstoffatome enthält, mindestens eine Aldehyd- oder Ketogruppe sowie zwei Hydroxygruppen . ...
- Vorkommen von Kohlenhydraten in LebensmittelnKohlenhydrate sind in unterschiedlicher Menge in fast allen pflanzlichen Lebensmitteln enthalten. Einen besonders hohen Anteil an Kohlenhydraten weisen Getreide (z. B. Weizen, Roggen, Gerste, Hafer, Mais, Reis) sowie Getreideprodukte (Brot, Brötchen, Teigwaren, Müsli, Gebäck) auf. Einige Pseudoge...
- Verdauung und ResorptionWie bereits im vorherigen Kapitel erwähnt, gibt es sehr viele verschiedene Arten von Kohlenhydraten. In unserer Nahrung können diese Kohlenhydrate als Mono- oder Disaccharide, aber auch als Oligo- und Polysaccharide vorkommen. Um letztendlich all diese Formen aufnehmen zu können, ist es nötig, d...
- Regulation des BlutzuckerspiegelsAls Blutzucker bezeichnet man die Konzentration von Glukose im Blut. Bei einem gesunden Menschen liegt der Blutzuckerspiegel normalerweise in einem Bereich von 60–110 mg/dl. In diesem Bereich steht dem Organismus ausreichend schnell verfügbare Glukose zur Verfügung, sodass auch bei einer akuten ...
- Stoffwechselprozesse
- Glykolyse Die Glykolyse ist der erste Abschnitt des Abbaus des Monosaccharids Glukose. Dieser Abbau wird in mehrere Schritte unterteilt, die auch ohne die Anwesenheit von Sauerstoff ablaufen. Am Ende werden aus einem Molekül Glukose zwei Moleküle Pyruvat hergestellt und es werden zwei Moleküle ATP (netto) ...
- Oxidative Decarboxylierung Die oxidative Decarboxylierung ist der zweite Schritt des Glukoseabbaus und findet in der Matrix der Mitochondrien statt. Um diesen Schritt zu ermöglichen, muss das Pyruvat aus der Glykolyse zuerst in die Mitochondrien transportiert werden. Auch bei diesem Schritt gibt der Name schon Auskunft über...
- Anaerober Weg der Energiegewinnung Wie bereits oben beschrieben, muss Pyruvat aus der Glykolyse zuerst in die Mitochondrien transportiert werden, um anschließend durch die Pyruvatdehydrogenase weiter verstoffwechselt zu werden. Liegt in der Zelle nicht ausreichend Sauerstoff vor, kann der Abbau in den Mitochondrien nicht im geeignet...
- CitratzyklusDer Citratzyklus kann als Endstrecke des Nährstoffabbaus verstanden werden. Alle Hauptenergielieferanten unseres Körpers – Eiweiße, Kohlenhydrate und Fette sowie auch Alkohol – werden abgebaut und münden in Form von Acetyl-CoA in den Citratzyklus und können dadurch vollständig zu CO2, Wass...
- AtmungsketteDie Atmungskette ist der Überbegriff für eine Kette biochemischer Reaktionen, die der Energiegewinnung dienen. Das Ziel der Reaktion ist es, unter Verbrauch der Reduktionsäquivalente NADH+H+ und FADH2, Energie in Form von ATP zu gewinnen. Bei diesem Vorgang werden Elektronen sowie Protonen (H+) a...
- Fette
- Funktion von FettenFette und Öle gehören zu den essenziellen Grundbausteinen des Körpers. Sie können von diesem nur teilweise selbst synthetisiert werden und müssen daher auch von außen mit der Nahrung zugeführt werden (sogenannte essenzielle Fettsäuren). Die im Körper vorhandenen Fette erfüllen verschiedene...
- Aufbau von Fetten Fette werden im Fachjargon als Triacylglyceride (TAG) oder Triglyceride (TG) bezeichnet. Diese Namen haben die Fette aufgrund ihres Grundgerüsts, welches aus einem Glycerin und drei Fettsäuren besteht (siehe Abbildung). Das Grundgerüst des Glycerins besteht aus drei Kohlenstoffatomen, die über ...
- Vorkommen von Fetten in LebensmittelnAuch Fette sind in einer Vielzahl von Lebensmitteln enthalten. Hierbei variiert der Gehalt von Fetten und somit auch die Kaloriendichte jedoch sehr stark. Fettreiche Lebensmittel sind vor allem Fette und Öle, die aus unterschiedlichen Nahrungsmitteln wie beispielsweise Oliven oder Raps gewonnen wer...
- Verdauung und Resorption von FettenDer Abbau von Fetten ist ein äußerst komplexer Vorgang. Der Grund dafür liegt in den Eigenschaften der Fette. Diese können nur als polare Fettsäuren, die sich mit anderen Substraten zu Mizellen zusammenlagern, die Membran der Verdauungsorgane passieren. Daher ist es nötig, dass die über die N...
- Abbau von TAGDer erste Schritt des Abbaus und der Energiefreisetzung ist das Abspalten der einzelnen Fettsäuren. Dieser Schritt wird als Lipolyse bezeichnet. Dabei werden die TAG durch Lipasen in drei Fettsäuren und ein Glycerin gespalten. Die Fettsäuren sind sehr energiereiche Verbindungen, die in der Zelle...
- EnergiebilanzBei dem Abbau von TAG zu Glycerin und Fettsäuren sowie deren Abbau wird sehr viel Energie frei, die zur Regeneration von ATP in der Atmungskette genutzt werden kann. Wie viel Energie genau frei wird, hängt von der Länge der Fettsäuren ab. Je länger eine Fettsäure ist, desto häufiger kann die ...
- Proteine
- FunktionProteine sind für den Körper von großer Wichtigkeit, da sie verschiedenste Funktionen erfüllen und als universelle Bausteine für jede Zelle dienen. Sie können aufgrund ihrer unterschiedlichen Funktionen in sieben Gruppen unterteilt werden: Strukturproteine geben unseren Zellen, Geweben und so...
- Aminosäuren und Peptide Aminosäuren sind die Grundbestandteile von Proteinen. Genauer gesagt, wird die Funktion von Proteinen durch die Reihenfolge der Aminosäuren bestimmt. Aber was sind Aminosäuren? Wie der Name schon vermuten lässt, ist eine Aminosäure ein Molekül mit einer Aminogruppe (NH3) und einer Säuregrup...
- Raumstruktur von ProteinenNach der Proteinbiosynthese liegt die Polypeptidkette im Zytoplasma vor. Bevor die Polypeptidkette jedoch als Protein funktionsbereit ist, müssen sogenannte Faltstrukturen ausgebildet werden, welche dem Protein seine dreidimensionale Struktur verleihen. Viele Proteine bilden diese Faltstrukturen vo...
- DenaturierungDie Denaturierung von Proteinen beschreibt die Zerstörung der Quartär-, Tertiär- und Sekundärstruktur eines Proteins. Dabei bleibt die Primärstruktur jedoch erhalten, da die Peptidbindung eine starke Bindung ist, die nicht so einfach aufgespalten werden kann. Es gibt verschiedene Denaturierung...
- Vorkommen von Proteinen in LebensmittelnEin geringer Anteil an Proteinen ist in fast allen Lebensmitteln enthalten. Einige pflanzliche und tierische Lebensmittel weisen jedoch einen recht hohen Proteinanteil auf. Als pflanzliche Proteinquellen dienen vor allem Hülsenfrüchte wie Linsen oder Bohnen, Tofu aus Soja, verschiedene Getreides...
- Verdauung und Resorption von Eiweißen Haben wir eine eiweißhaltige Mahlzeit zu uns genommen, müssen diese Eiweiße, die aus langen miteinander verknüpften Aminosäureketten bestehen, zuerst in kleinere Einheiten gespalten werden, bevor sie von den Schleimhautzellen des Verdauungstraktes resorbiert werden können. Diese Spaltung wird ...
- Energiegewinnungsprozesse Der Körper eines erwachsenen Menschen enthält etwa 6-12 kg Proteine. Von diesen Proteinen werden pro Tag ca. 300g zu Aminosäuren abgebaut, um anschließend für die folgenden Prozesse zur Verfügung zu stehen: Ein Großteil der Aminosäuren dient der Synthese von neuen Proteinen. Ein kleinerer...
- Harnstoff Aminosäuren können in allen Zellen des Körpers trans- oder desaminiert und zur Energiegewinnung herangezogen werden. Bei diesem Prozess wird in jedem Fall Ammoniak (NH3) frei. Dieses Ammoniak wirkt in hoher Dosis toxisch und kann nicht weiter abgebaut werden. Daher muss es an ein anderes Molekül...
- Der Stoffwechsel in Nahrungskarenz
- Der Körper in einer FastenphaseBefindet sich der Körper in einer Fastenphase, müssen zum Decken des täglichen Energiebedarfs körpereigene Energiereserven herangezogen werden. Dabei können von einem Großteil der Organe Fettsäuren als Energiequelle herangezogen werden. Die Fettsäuren werden von den Fettzellen in das Blut ab...
- GlukoneogeneseUnter Glukoneogenese wird die Synthese von Glukose aus organischen Nicht-Kohlenhydratvorstufen verstanden. Wie bereits beschrieben, ist diese Reaktion essenziell, um Erythrozyten, Zellen des Nierenmarks und des Nervensystems auch in Fastenphasen mit Glukose zu versorgen. Aufgrund der enzymatischen A...
- Ketonkörper Neben Fetten und Kohlenhydraten spielen Ketonkörper, vor allem in Phasen längeren Fastens, eine essentielle Rolle, um den Energiebedarf des Körpers zu decken. Die Synthese der Ketonkörper findet ausschließlich in den Mitochondrien der Leberzellen und nur nach längerer Nüchternheit und dem Feh...
- Alanin-Glukose-ZyklusDer Alanin-Glukose-Zyklus beschreibt den Kreislauf des Aminosäure-Auf- und -Abbaus sowie der Glukosebildung zwischen Skelettmuskulatur und Leber. Dabei werden verschiedene Stoffwechselwege, wie die Glukoneogenese, die Trans- und Desaminierung sowie Teile des Citratzyklus und des Harnstoffzyklus mit...
- Steuerung der Nahrungsaufnahme
- Appetit, Hunger und SättigungBevor wir uns mit den genauen Regulationssystemen der Nahrungsaufnahme beschäftigen, wollen wir zunächst auf die zentralen Begrifflichkeiten Appetit, Hunger und Sättigung eingehen und diese voneinander abgrenzen. Unter Appetit versteht man einen psychischen Zustand, der sich durch das lustvolle V...
- Regulation der NahrungsaufnahmeDie Gesamtheit der oben beschriebenen Zustände lässt sich als Homöostase von Hunger und Sättigung bezeichnen und ist ein sehr komplexer Vorgang, an dem zahlreiche metabolische, endokrine und neuronale Prozesse beteiligt sind. All diese Prozesse müssen miteinander verrechnet werden, um das Hunge...
- Hunger- und SättigungstheorienMan unterscheidet verschiedene Hunger- und Sättigungstheorien, die teilweise auf den oben aufgeführten Erkenntnissen aufbauen. Diese erklären entweder das kurzfristige Entstehen des Hunger- und Sättigungsgefühls (thermostatische, aminostatische und glucostatische Theorie) oder die längerfristi...
- Ernährungsabhängige Erkrankungen
- Diabetes mellitus
- HäufigkeitAktuell leiden in Deutschland etwa 6,9 Millionen Menschen an Diabetes mellitus. Der Großteil (ca. 95%) dieser Erkrankungen ist auf den Diabetes Typ 2 zurückzuführen (die Daten auf die wir uns in diesem Kapitel beziehen, stammen aus dem "Deutscher Gesundheitsbericht Diabetes 2020"). Vor 100 Jahren...
- Diabetes-Typen Beim Diabetes mellitus Typ 1 kommt es durch erbliche Veranlagung und äußere Faktoren (z. B. bestimmte Virusinfektionen) zu einer Fehlsteuerung des Immunsystems. Dieses erkennt die insulinproduzierenden β-Zellen der Bauchspeicheldrüse als fremd und greifen diese an. Durch den Untergang der β-Zel...
- DiagnostikDie Diagnose eines Diabetes mellitus ist anhand verschiedener Parameter möglich, die eine Auskunft über die Regulation des Blutzuckerspiegels ermöglichen. Anhand der Werte kann eine Unterteilung in gesund, Prädiabetes und Diabetes mellitus erfolgen. Als Prädiabetes wird die Vorstufe des Diabete...
- Folgen der DiabeteserkrankungZu Beginn der Erkrankung merken die Betroffen meist keine bis geringe Symptome. Die ersten Symptome sind häufiger Durst und ein erhöhter Harndrang. Dieser entsteht durch den zu hohen Blutzuckerspiegel, der dazu führt, dass die Glukose in der Niere nicht vollständig resorbiert werden kann und dah...
- Exkurs: Diabetische Ketoazidose und Hyper- und HypoglykämieBei einem Typ I-Diabetiker findet die Insulinsekretion zu wenig oder gar nicht mehr statt. Daher ist es kaum möglich, den aufgenommenen Zucker über insulinabhängige GLUT 4-Kanäle in die Muskel- oder Fettzellen aufzunehmen. Dadurch fehlt den Zellen trotz hohem Blutglukosespiegel die nötige Energ...
- Möglichkeiten der ErnährungstherapieDie Therapie des Diabetes mellitus ist komplex und abhängig von der vorliegenden Diabetesform. Grundsätzlich ist jedoch bei Typ-1-Diabetikern immer eine Insulintherapie erforderlich, während bei Typ-2-Diabetikern auch eine konservative Therapie in Form von Gewichtsreduktion, Ernährungsumstellung...
- Praxisbeispiel zur Diabetesprävention durch ErnährungDie oben aufgeführten Ernährungs- und Verhaltensempfehlungen wurden beispielsweise in dem Präventionsprogramm aha!2.0 („ab heute anders”) in Schleswig-Holstein umgesetzt, in dem Risikopatienten, die mit einer hohen Wahrscheinlichkeit in den nächsten 10 Jahren an Diabetes mellitus erkranken, ...
- Diabetes mellitus
- Erkrankungen der Verdauungsorgane
- Exkurs: Analyse von Erkrankungen der VerdauungsorganeErkrankungen der Verdauungsorgane sind eines der beliebtesten Abiturthemen. Ein Grund hierfür ist sicherlich, dass eine Vielzahl von Themen abgefragt werden kann: Aufbau und Funktion von Organen, Resorption und Verdauung verschiedener Nahrungsbestandteile (z.B. Eiweiße, Kohlenhydrate und Fette sow...
- Magenentfernung bei Magenkrebs (Magenkarzinom)Das Magenkarzinom stellt bei Männern sowie bei Frauen eine der häufigsten tumorbedingten Todesursachen dar. Risikofaktoren für das Entstehen eines Magenkarzinoms sind vielfältig. Darunter fallen zum Beispiel die chronische Besiedlung des Magens mit dem Bakterium Helicobacter pylori, genetische R...
- Pankreasinsuffizenz durch Mukoviszidose Bei der Mukoviszidose handelt es sich um eine angeborene, erbliche Erkrankung. Es sind viele verschiedene Mutationen des sogenannten CFTR-Gens bekannt, welche alle zu einem Defekt des gleichnamigen Proteins führen. Dieses Protein ist als Chloridkanal in zahlreichen Organen wie der Lunge, Leber, Bau...
- Kurzdarm-Syndrom durch Mesenterialinfarkt Ein Mesenterialinfarkt ist ein sehr bedrohliches Krankheitsbild, bei dem es durch einen Verschluss eines den Darm versorgenden Blutgefäßes zur Minderversorgung der Dünndarmschlingen kommt. Wird dieser Zustand nicht innerhalb weniger Stunden durch eine Operation behoben, kann es zum Absterben des ...
- Einschränkung der Sekretion von Gallenflüssigkeit durch PSCBei der primär sklerosierende Cholangitis (PSC) handelt es sich um eine Autoimmunerkrankung, bei der körpereigene Immunzellen die Gallengangzellen in der Leber schädigen und somit die Sekretion von Gallenflüssigkeit eingeschränkt ist. Zudem kommt es häufiger zu Gallensteinen, die auch die Gall...
- Auswirkung der Dickdarmentfernung nach DarmkrebsDickdarmkrebs ist bei Männern der zweithäufigste, bei Frauen der dritthäufigste Krebs. Darmkrebs kann im Rahmen einer Darmspiegelung entdeckt werden. Ein möglicher Vorbote kann Blut im Stuhl sein. Je nachdem wo der Krebs im Darm sitzt und wie weit er sich ausgebreitet hat, kann der betroffene Da...
- Kohlenhydrate
- Grundlagen
- Wasser und Mikronährstoffe
- WasserWasser ist der Ursprung allen Lebens. Daher ist es auch nicht verwunderlich, dass Wasser der mengenmäßig wichtigste anorganische Bestandteil des menschlichen Körpers ist. Die meisten lebensnotwendigen Funktionen im Körper sind nur in Anwesenheit von Wasser möglich. Dabei dient Wasser unter ande...
- Makro- und MikronährstoffeZu den Makronährstoffen zählen Kohlenhydrate, Fette und Eiweiße. Diese Gruppe zeichnet sich dadurch aus, dass durch Spaltung dieser Substanzen Energie freigesetzt werden kann. Die Makronährstoffen werden in den jeweiligen Kapiteln behandelt....
- BallaststoffeBallaststoffe sind Nahrungsbestandteile, die vorwiegend in Form von Kohlenhydraten in pflanzlichen Lebensmitteln vorkommen. Im Gegensatz zu Makronährstoffen können sie im Dünndarm nicht verdaut oder absorbiert werden. Über verschiedene Mechanismen weisen sie trotzdem positive Effekte für die Ge...
- Aufbau der Zelle
- Die ZelleDie Zelle ist die kleinste lebende Einheit. Sie ist in der Lage sich selbstständig zu vermehren (man sagt: Zellen teilen sich) und viele unterschiedliche Aufgaben zu übernehmen. Um die Überlebenswahrscheinlichkeit zu erhöhen, arbeiten Zellen häufig als mehrzellige Organismen (Tiere, Menschen, P...
- Der ZellkernDer Zellkern ist ein rundes, poriges Organell, die das Erbgut, also die DNA, beinhaltet. In ihm ist die DNA geschützt und in zweimal 23 Chromosomen organisiert. Im Zellkern wird reguliert, welche Gene in mRNA umgeschrieben (transkribiert) werden. Die Poren des Zellkerns bestimmen dabei selektiv, we...
- Die DNADie DNA (Desoxyribonukleinsäure) ist zwar eine lange Molekülstruktur und kein Organell, aber dennoch wichtig, denn sie stellt unser Erbgut dar. Sie besteht aus zwei langen Ketten, die sich gegenüberstehen und in sich gewunden sind. Man bezeichnet die DNA daher auch als DNA-Doppelstrang. Jede Kett...
- Das endoplasmatische RetikulumDas endoplasmatische Retikulum (ER) ist ein sehr großes und labyrinthartiges Organell, das aus einer Lipiddoppelmembran gebildet wird. Es liegt wie ein Schlauchsystem um den Zellkern herum und dient vor allem als Synthese- und Speicherort für Proteine (Abb. 1.4). Das ER kommt in allen kernhaltigen...
- Das RibosomDas Ribosom schreibt mRNA-Moleküle in Peptidketten um (Translation). Es besteht aus zwei Untereinheiten, der 60S- und die 40S-Untereinheit, die selbst wiederum aus ribosomaler RNA (rRNA) aufgebaut sind. Zusammen bilden sie das 80S-Ribosom der Eukaryoten. Das „S“ steht dabei für den Sedimentati...
- Der Golgi-ApparatDer Golgi-Apparat ist wie das ER auch ein Organell, das aus Lipiddoppelmembranen besteht. Er wurde nach seinem Entdecker, dem Italiener Camillo Golgi benannt und besteht im Wesentlichen aus aufeinandergestapelten Membransäcken, den sogenannten Zisternen. Der Golgi-Apparat erhält vom ER aus Protein...
- Das MitochondriumDas Mitochondrium bzw. die Mitochondrien sind die sogenannten „Kraftwerke“ der Zelle. Sie sind ganz besondere Organellen, da sie Zucker (Glukose) in Energie (ATP) umwandeln können. Wird Sauerstoff bei der ATP-Bildung gebraucht, spricht man von der Zellatmung. Das Besondere an den Mitochondrien ...
- Das ZytoskelettDas Zytoskelett ist das Grundgerüst der Zelle. Es besteht aus filamentösen Proteinen (z. B. Aktin), die der Zelle Halt und Stabilität geben. Es fixiert aber auch die Organellen in der Zelle, dient als Gerüst für den Vesikeltransport und ermöglicht die Fortbewegung. Indem das Skelett an einer S...
- Die ZellmembranDamit die Zelle nicht ausläuft und ihn Form gehalten wird, ist sie von einer sogenannten Zellmembran (auch Plasmamembran genannt) umgeben. Auch einige Organellen sind von einer Plasmamembran umgeben. Die Membran schirmt das Zellinnere aber nicht nur von der äußeren Umgebung ab, sondern dient auch...
- Wichtige Prozesse in der ZelleNeben dem Aufbau der Zelle, ist es auch wichtig zu verstehen, wie die vielen verschiedenen Prozesse ablaufen. Im Folgenden werden daher einige grundlegenden Prozesse aufgeführt....
- Enzymatik
- Grundlagen EnzymatikEnzyme gehören hinsichtlich ihres Aufbaus der Klasse der Proteine an. Sie besitzen aufgrund ihres spezifischen Aufbaus eine ganz bestimmte Funktion und können wichtige Reaktionen beschleunigen. Hast du am letzten Wochenende beispielsweise ein Bier getrunken, dann war das nur möglich, weil kleine ...
- Hemmungen der EnzymfunktionIn der Medizin sind die Wirkungen von bestimmten Stoffen auf Enzyme des Körpers höchst interessant. Je besser wir diese Vorgänge verstehen, desto gezielter können wir in unerwünschte Stoffwechselprozesse eingreifen. Ein solcher Eingriff kann beispielsweise durch die Hemmung eines bestimmten Enz...
- EnzymklassifikationEnzyme erfüllen in unserem Körper verschiedene Funktionen. Dabei können die Enzyme anhand ihrer Wirkungsweisen in sechs verschiedene Gruppen unterteilt werden: ...
- Aufbau der CosubstrateAdenosintriphosphat (ATP) ist dir vielleicht aus der Biologie als Nukleotid bekannt, das zur DNA- oder RNA-Synthese verwendet wird. Dieses Nukleotid spielt aber auch in vielen anderen Reaktionen des Körpers eine wichtige Rolle, da es als Energielieferant fungieren kann. Es stellt den häufigsten En...
- Energetische Versorgung Unser Körper ist darauf angewiesen, aus den Nahrungsbestandteilen Eiweiße, Kohlenhydrate, Fette und auch Alkohol Energie zu gewinnen, um lebenswichtige Prozesse aufrechtzuerhalten. Im Folgenden werden die Grundlagen der energetischen Versorgung des Körpers besprochen, bevor in den jeweiligen Kapi...
- Anatomie und Physiologie des Verdauungstraktes
- Histologischer Aufbau von VerdauungsorganenDie Verdauungsorgane, die in direktem Kontakt mit Nahrung stehen (Speiseröhre, Magen, Dünndarm und Dickdarm), weisen eine typische Anordnung der Gewebsschichten auf. Dieser Aufbau ermöglicht die Verdauung und Resorption von Nahrungsbestandteilen, die Sekretion von Verdauungsenzymen sowie die Peri...
- MundhöhleDie Mundhöhle ist der erste Abschnitt des menschlichen Verdauungstraktes. Sie enthält die Zähne und die Zunge zur Zerkleinerung der Nahrung sowie Speicheldrüsen. Die Speicheldrüsen produzieren Speichel, der Verdauungsenzyme und Abwehrstoffe enthält und die Speisen gleitfähig macht. Nachdem d...
- Speiseröhre (Ösophagus)Die Speiseröhre ist ein etwa 25–28 cm langes schlauchförmiges Hohlorgan, das die zerkleinerte Nahrung von dem Mundraum in den Magen befördert. Dabei befindet sich die Speiseröhre in direkter Nachbarschaft zu Luftröhre, Hauptschlagader und Herzen. Durch die Peristaltik der glatten Muskulatur k...
- MagenDer Magen ist ein schlauchförmiges Hohlorgan, das Ösophagus und Dünndarm miteinander verbindet. Er liegt unterhalb des Zwerchfells im linken Oberbauch. Durch seinen Aufbau ist der Magen dehnbar und kann sich, je nach Füllungszustand, im Bauchraum auf ein Volumen von bis zu 1,5 Litern ausdehnen. ...
- Dünndarm Der Dünndarm ist ein 5–6 m langes Hohlorgan, das vom Magenausgang bis zum Dickdarm reicht. Er dient vor allem der Nährstoffverdauung sowie der Resorption der Nährstoffe und des Wassers und hat somit eine überlebenswichtige Funktion. Von allen Verdauungsorganen ist der Dünndarm das einzige Org...
- Prinzip der OberflächenvergrößerungVielleicht hast du auch schon einmal gehört, dass die Oberfläche des Dünndarms etwa 400-500 qm2 groß ist. Wie dies bei einem 5 bis 6 m langen Hohlorgan möglich ist und welche Funktion diese Oberflächenvergrößerung hat, erklären wir im Folgenden. An der Oberfläche des Dünndarms findet die ...
- DickdarmDer Dickdarm ist der terminale Abschnitt des Verdauungstraktes und reicht vom Ende des Dünndarms bis zum Anus. Dabei weist er eine Länge von 1,5 m auf. Der Dickdarm entzieht den nicht resorbierten Speisebreiresten aus dem Dünndarm Wasser und Elektrolyte und dickt diese entsprechend ein. Zudem wir...
- Leber und GallenblaseDie Leber ist das wichtigste Stoffwechselorgan des Menschen. Sie befindet sich im rechten Oberbauch direkt unter dem Zwerchfell und erhält über Blutgefäße die Nährstoffe, die durch den Darm absorbiert wurden. Die Leber kann in acht Segmente unterteilt werden, die aufgrund ihrer Blutversorgung i...
- Bauchspeicheldrüse (Pankreas)Die Bauchspeicheldrüse ist ein 12 bis 15 cm langes Organ, das quer im Oberbauch liegt und von Magen und querverlaufendem Dickdarmabschnitt verdeckt wird. Anatomisch kann die Bauchspeicheldrüse in Kopf, Körper und Schwanz unterteilt werden. Die Bauchspeicheldrüse kann funktionell in einen endokri...
- Wasser und Mikronährstoffe
- Nahrungsempfehlung
- Ernährung gesunder Erwachsener
- ErnährungsempfehlungenErnährungsempfehlungen für gesunde Menschen sind im Abitur von besonderer Wichtigkeit und sollen z.B. in Form der vollwertigen Ernährung beziehungsweise anhand der 10 Regeln der DGE angewendet werden. Mit Hilfe dieser Ernährungsempfehlung können Ernährungsformen (wie weiter unten dargestellt) ...
- Ernährungsempfehlungen nach DGESoll in einer Aufgabe ein bestimmtes Ernährungsverhalten wie eine Atkins-Diät oder vegane Ernährung beurteilt oder bewertet werden, ist es besonders ratsam sich auf die 10 Regeln der DGE zu beziehen, da genau diese euch die Punkte einbringen. Lernt diese daher am besten sinngemäß und analysiert...
- VollwerternährungDas Konzept der Vollwerternährung wurde von Prof. Claus Leitzmann, Dr. Karl von Koerber und Thomas Männle entwickelt. Bei dieser Ernährungsform handelt es sich um eine überwiegend pflanzliche (lakto-vegetabile) Ernährungsweise. Dabei werden großteils Gemüse und Obst, Vollkornprodukte, Kartoff...
- Exogene Faktoren bei der Steuerung der NahrungsaufnahmeKritik an unserer heutigen Ernährung, der sogenannten Western-Diet, sowie neue Ernährungstrends - von vegan bis paleo - sind heutzutage in aller Munde. In der digitalen wie auch der analogen Welt sind Ernährungstipps und Werbung für neue Produkte quasi ubiquitär vorhanden. Aber wie genau hat si...
- Exkurs: Beurteilung von ErnährungsformenVegetarismus ist eine Ernährungs- und Lebensweise, bei der auf den Verzehr von Tieren und ggf. tierischen Produkten verzichtet wird. Dabei unterscheidet man verschiedene Formen, z.B.: Ovo-Lacto-Vegetarier: Verzicht auf Fleischprodukte Lacto-Vegetarier: Zusätzlicher Verzicht auf Eier Veganer: Komp...
- Ernährung und Sport
- Sport und GesundheitNeben einer ausgewogenen und gesunden Ernährung ist Sport eine wichtige Säule eines gesunden Lebensstils. Bevor wir genauer auf die Energiebereitstellung während sportlicher Belastungen oder die Ernährung von Sportlern eingehen, wollen wir uns mit den Begriffen Sport und Gesundheit sowie einem M...
- Salutogenesemodell Salutogenesemodell (lat. salus = Gesundheit, Glück und griech. génesis = Entstehung) Das Modell der Salutogenese befasst sich mit der Frage, was Gesundheit ist und wie sie entsteht. Es ist demnach ein positiver Ansatz zur Erklärung, wie die Gesundheit verbessert, aber auch durch welche Faktoren s...
- Energiebereitstellung in der Belastungsphase Bei der Muskelkontraktion ist ATP (Adenosintriphosphat) der einzig verwertbare Energielieferant. ATP löst in diesem Zusammenhang die Verbindung von Aktin und Myosin, um eine erneute Bindung möglich zu machen. Man spricht in diesem Zusammenhang auch von der „Weichmacherfunktion“. Ist zu wenig A...
- Bedeutung der Kohlenhydrate im AusdauersportWie anhand der Graphik zur Energiebereitstellung im Rahmen einer Ausdauerleistung deutlich wird, sind Kohlenhydrate besonders während der ersten Stunde der Belastung die Energiequelle Nummer 1. Das liegt unter anderem daran, dass aus Kohlenhydraten im Vergleich zu Fetten mehr ATP pro Zeiteinheit ge...
- Bewertung von speziellen Ernährungsprodukten für SportlerDas Geschäft mit spezifischen Ernährungsprodukten für Sportler boomt auch in Deutschland. Im Jahr 2017 wurden, laut Institut der deutschen Wirtschaft, derartige Produkte im Wert von 156 Millionen Euro verkauft. Die Produktpalette ist riesig und reicht von Eiweißpulvern und -riegeln bis hin zu Vi...
- Ernährung gesunder Erwachsener
- Milch & Getreide
- Milch
- MilcherzeugungIn Deutschland werden jährlich durchschnittlich 50 bis 60 Liter Kuhmilch und 25 kg Käse pro Kopf konsumiert. Auf alle Bewohner Deutschlands gerechnet ergibt sich eine enorme Menge an Milch, die produziert werden muss. Für diese Produktion sorgen ca. 4 Millionen Kühe, die pro Tag ungefähr 20 Lit...
- Zusammensetzung der KuhmilchDie Zusammensetzung von Kuhmilch zu kennen, ist entscheidend, um sie hinsichtlich ihres gesundheitlichen Nutzens bewerten zu können sowie die Verarbeitung von Milch zu anderen Produkten wie Käse und Joghurt zu verstehen. Durch die Zusammensetzung können zudem Rückschlusse auf den Gesundheitszust...
- MilchgewinnungUnter der Milchgewinnung wird ein komplexer Prozess, der vom Melken der Kühe bis zur Milchabgabe an verarbeitende Betriebe reicht, verstanden. Diesen werden wir im Folgenden kurz skizzieren: Das Melken findet in sog. Melkanlagen statt. In diesen sollen die Kühe unter möglichst schonenden und hygi...
- Kontrolle der Milch Bei der Befüllung der Sammelwagen mit Rohmilch erfolgt eine Probeentnahme zur Qualitätskontrolle der Milch. Für die Kontrolle der Qualität stehen verschiedene Untersuchungsverfahren zur Verfügung. Von diesen werden im Folgenden einige aufgeführt: Bakteriologische Beschaffenheit: Mithilfe spe...
- Trinkmilchaufbereitung Bevor die Rohmilch der Bauernhöfe an den Endverbraucher verkauft werden kann, ist die Verarbeitung der Milch zu Konsummilch nötig. Dieser Prozess beginnt mit der Reinigung der Milch. Hierbei werden Zentrifugen eingesetzt, die die Bestandteile der Milch anhand ihrer Dichte voneinander trennen. Mith...
- Joghurt-HerstellungJoghurt kann aus Milch oder Sahne hergestellt werden. Dazu erfolgt eine Zugabe von thermophilen (bei hohen Temperaturen wachsenden) Bakterien wie Lactobacillus bulgaricus oder Streptococcus thermophilus. Diese werden in der Milch oder Sahne für mehrere Stunden bei Temperaturen von etwa 40 bis 45 ...
- Ernährungsempfehlungen nach DGE Wie bereits in dem Kapitel „Ernährungsempfehlungen nach DGE“ beschrieben, empfiehlt die DGE den täglichen Konsum von 1 -3 Portionen Milch und Milchprodukten wie Joghurt und Käse. Als Grund für die Ernährungsempfehlung wird der hohe Anteil gut verfügbarer Proteine mit hoher biologischer W...
- Milch
- Stoffwechsel
- Ethik
- Q1 - Anthropologie und Bereichsethiken
- Anthropologische Grundpositionen
- Anthropologie - EinleitungDie Frage, was der Mensch ist, was ihn ausmacht und was ihn besonders macht, ist vermutlich genauso alt, wie der vernünftig denkende Mensch selbst. Die Anthropologie, die Wissenschaft vom Menschen, beschäftigt sich mit genau dieser Frage. Das folgende Kapitel wird näher auf diese Frage eingehen u...
- Der Mensch als Individuum und in der GesellschaftAristoteles (384 v. Chr. – 322 v. Chr.) gilt als einer der einflussreichsten und bedeutendsten Philosophen der Antike. Er war Schüler des Platons, doch entwickelte er viele eigene Ideen und grenzte sich von seinem Lehrmeister ab. Für Aristoteles ist der vernünftige und sprachbegabte Mensch...
- Hannah ArendtHannah Arendt (1906 – 1975) war jüdischer Herkunft und floh daher 1933 nach kurzer Gestapo-Haft nach Frankreich, wo sie 1940 im Süden des Landes in einem Konzentrationslager inhaftiert wurde. Sie emigrierte in die USA, wo viele ihrer Werke entstanden. Dort arbeitete sie auch als Professorin an v...
- Die Doppelnatur des Menschen Der österreichische Arzt Sigmund Freud (1856-1939) gilt als der Urvater der modernen Psychoanalyse. Nachdem er zuerst als Neurologe das menschliche Gehirn untersuchte, wandte er sich den psychischen Krankheiten zu. Freud entwickelte eine Form der Gesprächstherapie, die psychoanalytische Methode. B...
- Wichtige Begriffe der AnthropologieAnthropologieDie Wissenschaft vom Menschen bzw. die Frage nach dem Wesen des Menschen und seiner Stellung in der WeltLogosHier: geistiges Vermögen/ VernunftVernunftFähigkeit des Menschen zum logischen Denken, die es ihm erlaubt, Bezüge zur Realität herzustellenZoon politikonDer Mensch als sozial...
- Medizinethik
- Einführung in medizinische Prinzipien (nach Beachump/ Childress)Die beiden amerikanischen Autoren Tom L. Beauchamp und James F. Childress prägen seit 1979 mit ihrem Buch „Principles of Ethics“ die medizinethische Debatte. Sie stellten erstmalig vier ethische Prinzipien vor, die als Ausgangspunkt für die Behandlung moralischer Probleme im Bereich der Biome...
- Medizinethik am Lebensanfang - StammzellforschungWissenschaftliche Forschung muss sich immer wieder mit moralethischen Fragestellungen beschäftigen. Im Besonderen der Bereich der Stammzellforschung ist durch kontroverse Sichtweisen und komplexe Fragestellungen geprägt. Stammzellforschung wirft in der ethischen Diskussion die Frage nach der Schut...
- Medizinethik am Lebensanfang - GentechnikEin Beispiel, das dir vielleicht in den Sinn kommt, wird die gentechnische Manipulation mithilfe der Genschere Crispr-Cas sein. Dieses Verfahren wird als "Genschere" oder "molekulares Skalpell" bezeichnet. Mit dieser Methode ist es möglich, das Erbgut präzise an einer bestimmten Stelle zu durchtre...
- Medizinethik in der Lebensmitte - EnhancementOptimierung des Menschen – Verbesserung, Steigerung, Verstärkung, Erhöhung – so können wir den Begriff „Enhancement“ übersetzen. Diskutiert wird hierbei der Einsatz von Mitteln und Verfahren zur Verbesserung menschlicher Eigenschaften. Es ist kein rein medizinischer Anwendungsbereich, da...
- Medizinethik in der Lebensmitte - Präventive Gendiagnostik und Risikoabschätzung für Krankheiten Präventive Gendiagnostik könnte uns unter anderem ermöglichen, bereits vor oder direkt nach der Geburt zu bestimmen, an welchen Erkrankungen das Neugeborene im Laufe seines Lebens leiden könnte. Durch entsprechende Behandlungen könnte dann schon präventiv in die Krankheitsentstehung eingegriff...
- Medizinethik in der Lebensmitte - Organspende und OrgantransplantationDas Themenfeld Organspende kann zu mehren Lebensphasen hinzugezählt werden. Zu diesem Bereich gehören mehrere Akteure und Abläufe, die genauer erläutert werden sollen. Zunächst einmal – was ist eigentlich eine Organspende? Beschädigte oder verlorene Körperteile einfach austauschen zu könn...
- Medizinethik am Lebensende - SterbehilfeZu Beginn werden folgende Begriffe erklärt: EuthanasieVon gr. Eu=schön und hánatos = Tod; wurde im Dritten Reich ein verbrecherisches Programm zur Tötung körperlich und geistig behinderter MenschenAktive SterbehilfeGezielte Tötung eines Menschen mit dessen EinverständnisPassive SterbehilfeUnt...
- Medizinethik am Lebensende - Selbstbestimmung am LebensendeWenn es um medizinische Entscheidungen und richtungsweisende Schritte geht, kommt der Rolle des Patienten eine große Bedeutung zu. Hierbei kommt es zu Spannungsverhältnissen zwischen Autonomie und Gesundheit, Wertvorstellungen des Patienten und Wertvorstellungen des Arztes. Bei der Interaktion zw...
- Medizinethik am Lebensende - Sterben und Leben Ein zentraler Philosoph in dieser Debatte ist der US-Amerikaner Ronald Dworkin (1931-2013). Der Wert menschlichen Lebens wurde im Vorfeld schon mehrfach beleuchtet. Nach Dworkin muss eine freie Gesellschaft es jedem Einzelnen gestatten, diese zentrale Frage am Lebensende selbst entscheiden zu könne...
- Medizinethik am Lebensende - Sterbehilfekriterien Ganz allgemein meint Sterbehilfe sämtliche Handlungen oder Unterlassungen, die zum Tod anderer Menschen führen. Was spricht in dieser brisanten Debatte dafür und was dagegen? Argumente für und gegen Sterbehilfe können der Tabelle auf der folgenden Seite entnommen werden. Ob ein Leben lebenswe...
- Medizinethik am Lebensende - Sterbehilfeorganisationen Die Beihilfe zur Selbsttötung ist seit einem Urteil des Bundesverfassungsgerichts von 2020 erlaubt. 2021 halfen deutsche Sterbehilfe-Organisationen bei fast 350 Suiziden. Deutsche Organisationen sind: Deutsche Gesellschaft für Humanes Sterben Dignitas Deutschland Sterbehilfe Deutschland Doch wel...
- Medizinethik am Lebensende - ExkursWürdevolles Sterben, Autonomie bis zum Lebensende, Leben retten oder beenden – Wer darf darüber entscheiden? Das alles sind Fragen, mit denen sich der deutsche Schriftsteller und Jurist Ferdinand von Schirach in seinem Werk „Gott“ (2020 verfilmt) auseinandersetzt. Zentrales Thema ist die ...
- Medizinethik am Lebensende - Verlängerung des LebensWas versteht man unter Palliativmedizin und wann kommt sie zum Einsatz? Grundlegend hat die Palliativmedizin das Ziel dem Patienten eine möglichst hohe Lebenszufriedenheit, Lebensqualität und Selbstständigkeit zu erhalten – auch wenn keine Heilung mehr möglich ist. Die letzte Phase des Leben...
- Wichtige Begriffe der MedizinethikAutonomieWillensfreiheit als Zustand der Selbstbestimmung über meine EntscheidungenStammzellforschungMithilfe medizinischer Technik werden Versuche und Forschungen durchgeführt, welche eine gezielte Manipulation von Stammzellen zum Ziel haben. Dadurch sollen Krankheiten behandelt oder verhindert w...
- Tierethik
- TierethikStell dir vor, die Erde würde von Aliens überfallen werden. Sie sind hemmungslose Kreaturen, die uns Menschen ausnutzen und für medizinische Versuche missbrauchen. Einige sind auch sehr lieb und sorgen für uns, als seien wir ihre Haustiere. Doch dies trifft nicht auf alle zu. Die meisten versteh...
- Der Personenbegriff – Unterscheidung Mensch und TierEin Philosoph, der sich mit genau diesem Thema intensiv beschäftigt hat, ist Peter Singer (geb. 1946). Er gilt als moderner Vertreter des klassischen Utilitarismus und begründete eine neuzeitliche Art des Utilitarismus, den Präferenzutilitarismus. Anstatt wie Bentham oder Mill Handlungen nach Qu...
- Naturethische Positionen als Grundlage unserer moralischen BewertungMit seiner Ethik vertritt Peter Singer nicht wie viele andere Philosophen den Anthropozentrismus, sondern den Pathozentrismus als eine von vier naturethischen Grundpositionen. Vertreter des Anthropozentrismus sind zum Beispiel Immanuel Kant und René Descartes, welche in ihrer Philosophie den Mensc...
- Grundrechte für Menschenaffen – Great Ape ProjectGrundrechte stehen uns Menschen zu. Wir haben sie uns gegeben. Ein hart umkämpftes Ziel. Doch sollen diese menschengemachten Rechte auch unseren am nächsten stehenden Artgenossen, den Menschenaffen, zugestanden werden? Wissenschaftliche Studien zeigen unsere genetische Ähnlichkeit klar auf. Mensc...
- Darf man Tiere töten und essen?Diese Frage ist (auch aktuell) wohl die umstrittenste, wenn es um das Thema Tierethik geht. Sicherlich hast du da eine eigene Meinung zum Thema. Überlege dir doch einmal vorab, welche Argumente du für deine Position vertreten würdest – egal ob du Fleisch isst oder dich vegetarisch oder vegan er...
- Exkurs: Arthur SchopenhauerArthur Schopenhauer (1788-1860) war ein Philosoph, dessen Theorien auf den Vorstellungen der kantischen Philosophie beruhen. Er spielt im Ethikunterricht besonders beim Thema Tierethik mit seiner Gefühls- und Mitleidethik eine wichtige Rolle. Schopenhauer war selbst ein großer Tierfreund und zog T...
- Wichtige Begriffe der MedizinethikAutonomieWillensfreiheit als Zustand der Selbstbestimmung über meine EntscheidungenStammzellforschungMithilfe medizinischer Technik werden Versuche und Forschungen durchgeführt, welche eine gezielte Manipulation von Stammzellen zum Ziel haben. Dadurch sollen Krankheiten behandelt oder verhindert w...
- Anthropologische Grundpositionen
- Q2 - Grundpositionen der Ethik
- Kantische Ethik
- Kantische Ethik - EinleitungUnter Deontologie ist eine Pflichtethik zu verstehen, bei der das Richtige vor dem Guten gewählt wird. Das Gute ist in diesem Fall die Handlungsoption, die eine positive Konsequenz herbeiführt und moralisch als gut bewertet wird. Ein Beispiel für die Wahl des Guten wäre eine Notlüge, die eine P...
- Pflicht und NeigungKants Moralphilosophie (Ethik) wird von zwei zentralen Begriffen bestimmt: Pflicht und Neigung. Während die Pflicht bei richtiger Anwendung seiner Ethik einen moralischen Wert haben kann, ist die Neigung etwas Individuelles und für Kant, dessen Ethik einen allgemeingültigen Anspruch anstrebt, som...
- Der kategorische ImperativDer kategorische Imperativ: die wohl bekannteste Handlungsanweisung im Bereich der Moralphilosophie. Während andere Vertreter der deontologischen Ethik eher Vorschläge zu richtigen Handlungen bieten, ist Kant bei seiner Formulierung ganz deutlich. Er gibt eine Handlungsvorschrift, einen Imperativ ...
- Weitere Formulierungen des Kategorischen ImperativsKant entwickelte zusätzlich weitere Formen des kategorischen Imperativs, die alle dieselben Eigenschaften wie die Grundformel besitzen. Dazu gehören die Naturgesetzformel und die Menschheitszweckformel. Auch diese Imperative sind universell und absolut gültig und dürfen nicht vernachlässigt wer...
- Menschenwürde nach KantWie du zur „Grundform des kategorischen Imperativs“ erfahren hast, ist die Selbstzweckformel fundamental für die Würde des Menschen. Du kennst sicher den ersten Artikel aus dem Grundgesetz der Bundesrepublik Deutschland: Die Würde des Menschen ist unantastbar. Sie zu achten und zu schützen...
- Wichtige Begriffe der Kantischen Ethik(reine) VernunftNach Kant Grundlage aller Entscheidungen, in jedem Menschen vorhandenAutonomieEigenständiges Handeln (hier: sich selbst Gesetze aufstellen)HeteronomieFremdbestimmtes Handeln (durch Triebe oder andere Einflüsse)SelbstgesetzgebungMittels kategorischem Imperativ Regeln für moralische...
- Utilitarismus
- Utilitarismus - EinführungStell dir folgende Situation vor: Du bist Kampfjetpilot in der Bundeswehr und deine Aufgabe ist es, den Luftraum über Deutschland zu schützen. Nun tritt eines Tages tatsächlich der Ernstfall ein und ein Passagierflugzeug wird entführt. Die Entführer lassen über Funk bekannt geben, dass sie pla...
- Jeremy Bentham: Quantitativer UtilitarismusJeremy Bentham (geb. 1748 in London und 1832 verstorben) war Jurist, Sozialreformer und Philosoph. Er galt als Fortschrittsdenker seiner Zeit und setzte sich ein für das allgemeine Wahlrecht, die Abschaffung der Todesstrafe, Tierrechte und die Freiheit, zu lieben wen man möchte. 1789 erschien sein...
- Handlungs-, Regel- und PräferenzutilitarismusDen Utilitarismus kann man in zwei Arten unterteilen, und zwar in den Handlungs- und in den Regelutilitarismus. Beim Handlungsutilitarismus entscheidet man bei jeder Handlung neu und individuell, welche Handlung in der konkreten Situation die besten Folgen für alle Beteiligten hat. Wenn ich mir al...
- Kritik am UtilitarismusEinige Kritikpunkte des Utilitarismus wurden bereits angesprochen, man kann diesen jedoch noch weitere hinzufügen. Der klassische Utilitarismus würde theoretisch Versprechungen und Verträge unnütz machen, da sich immer eine Situation ergeben kann, in der es einen größeren Nutzen für alle Bete...
- Wichtige Begriffe des UtilitarismusNützlichkeitNützlich ist nach Bentham dasjenige, das Freude/Glück/Lust hervorbringt und Unheil/Unlust vermeidet.NutzenprinzipDer Maßstab der Beurteilung ist der Nutzen, den die Folgen haben.FolgenprinzipDie Moralität einer Handlung wird anhand ihrer Folgen beurteilt.Hedonistisches PrinzipEine H...
- Vergleich: Utilitarismus und DeontologieBeide Ethiken, Utilitarismus und Deontologie, sollen als Unterstützung dienen, moralisch gut zu handeln und gleichzeitig moralisch schlechte Handlungen zu charakterisieren. Im Folgenden findest du die Zusammenfassung der einzelnen Ethiken mit Beispielen. Wichtig ist dabei, dass du nicht darüber en...
- Verantwortungsethik
- Verantwortungsethik In vielen alltäglichen Situationen tragen wir nicht nur die Verantwortung für eine andere Person; oftmals haben unsere Handlungen weitreichende Konsequenzen, die beispielsweise die Natur betreffen. Durch die Verwendung von Technik sind uns neue Möglichkeiten gegeben, jedoch bringt dies auch neue ...
- Der Begriff VerantwortungSieht man im Lexikon nach, was der Begriff Verantwortung bedeutet, so findet man folgende Erklärung: Ursprünglich stammt der Begriff aus der Rechtssprache und verweist darauf, dass man vor Gericht für sein Tun Rede und Antwort stehen muss. Es geht darum, dafür zu sorgen, dass (innerhalb eines b...
- Verantwortung als mehrstellige Relation (Günther Ropohl)Gerade im Bereich der Technik wird es in der heutigen Zeit immer wichtiger, sich über die Folgen unserer Handlungen bewusst zu werden. Im Zuge dessen hat sich der Technikphilosoph Günter Ropohl (1939-2017) mit Verantwortung als mehrstellige Relation beschäftigt. Ropohl nennt die Relation, also di...
- Arten der Verantwortung (Hans Lenk)Der Begriff der Verantwortung begegnet uns immer wieder in sehr negativen Situationen – sei es eine Chemiekatastrophe, der Einsturz einen Flughafenterminals oder ein Vorfall in einem Atomkraftwerk wie in Fukushima. Der Philosophieprofessor Hans Lenk (geb. 1935) sagt, dass Verantwortung nicht glei...
- Notwendigkeit einer neuen Ethik – Hans Jonas neuer Imperativ2011 bebte in Japan die Erde. Als Folge kam es im Kernkraftwerk von Fukushima zu einem Reaktorunfall. Dabei wurde eine Unmenge von radioaktiven Emissionen freigesetzt, welche Luft, Wasser, Böden und Nahrungsmittel kontaminierte. Mehr als 100.000 Menschen mussten das Gebiet und ihr Zuhause verl...
- Wichtige Begriffe der VerantwortungsethikVerantwortungMit Verantwortung wird der Umstand bezeichnet, dass jemand gegenüber einer Instanz für sein Handeln Rechenschaft abzulegen hat.Kollektive VerantwortungKollektive Verantwortung ist die Verantwortung kollektiver Akteure für ihre Handlungen. Dies unterscheidet sie von der individuellen ...
- Kantische Ethik
- Q3 - Recht und Gerechtigkeit
- Theorien der Gerechtigkeit
- Theorien der GerechtigkeitWir alle wollen gerecht behandelt werden – der Wunsch nach Fairness ist groß. Doch wie schafft es eine Gesellschaft bzw. ein Staat, Gerechtigkeit herzustellen? Bereits der antike griechische Historiker Herodot stellte fest, dass wir Menschen Bräuche benötigen, also eine innerhalb einer Gemeinsc...
- NaturrechtDas Naturrecht wird auch als „überpositives Recht“ bezeichnet. Damit sind Normen für das menschliche Zusammenleben gemeint, deren Verbindlichkeit unabhängig von positiver Setzung (Rechte, die von Menschen erschaffen wurden) ist. Sie sollen somit als Maßstab für die Beurteilung der Güte von...
- RechtspositivismusPositives Recht ist innerhalb einer staatlichen Ordnung festgesetztes, beschlossenes und dadurch in Geltung gebrachtes Recht. Das Wort leitet sich vom lateinischen „ius positivum“ ab, das so viel bedeutet wie "gesetztes Recht" (ius = Recht, positum = gesetzt). Seit der Antike wird so das Recht b...
- Naturrecht oder Rechtspositivismus - ÜberblickNaturrechtslehreRechtspositivismusEs gibt ein ewig geltendes, positiven Gesetzen übergeordnetes Recht.Eine Rechtsordnung muss von positiven Grundnormen, unabhängig von ihrem sittlichen Gehalt, abgeleitet werden.Gefahren: Rechtsunsicherheit, Rechtfertigung despotischer Herrschaft als naturgemäßGe...
- Gustav Radbruch – Fünf Minuten Rechtsphilosophie Einer der bedeutendsten Rechtsphilosophen des 20.Jahrhunderts war Gustav Radbruch (1878-1949). In der Zeit der Weimarer Republik war er Hochschullehrer und sozialdemokratischer Justizminister. Schon früh vertrat er rechtspositivistische Positionen. Im Dritten Reich veranlasste ihn die als unerträg...
- Hans Kelsen – Absolute Gerechtigkeit, ein aussichtsloses UnterfangenEin weiterer bedeutender Rechtswissenschaftler ist der Österreicher Hans Kelsen (1881-1973). Bereits 1920 erklärte Kelsen den Respekt gegenüber Minderheiten als „höchsten Wert“ einer repräsentativen Demokratie. Er gilt als Architekt der im selben Jahr geschaffenen österreichischen Bundesve...
- Sittliche Vorstellungen und positives RechtMenschen leben in Gemeinschaft. Das bringt Vorteile mit sich, hat aber auch Nachteile. Klar ist, dass wir alle Interessen haben, die wir verfolgen. Jedoch stehen diese häufig den Interessen anderer gegenüber. Unterschiedliche Verhaltensweisen und Handlungsüberlegungen können zu Konflikten und Au...
- Gerechtigkeit als Tugend Tugendhaftes Verhalten: ein antiker Begriff in der Moderne? Der Begriff der Tugend (griechisch „arete“) ist vielschichtig gedacht. Man versteht darunter zumeist eine hervorragende Eigenschaft oder vorbildliche Haltung. Person, die tugendhaft handelt, zeigt eine Fähigkeit auf, die von der Gesell...
- Gerechtigkeitstheorien – Vertragstheorien einer gerechten GesellschaftUnser Gerechtigkeitsbedürfnis spiegelt sich in den Überlegungen der Vertragstheoretiker wider. Auf dieser Ebene wird versucht zu begründen, für welche staatliche Ordnung sich freie und gleiche Individuen in einer Art Anfangszustand (Urzustand ohne staatliche Ordnung) entscheiden würden, um eine...
- Egalitarismus Unter Egalitarismus ist ein Ideal zu verstehen, in der eine vollkommene Gleichheit in der Gesellschaft angestrebt wird. Hieraus leitet sich auf sozialer Ebene eine möglichst gleichmäßige Verteilung von Einkommen und Vermögen ab. Eine ungleiche Anhäufung von Gütern ist nur in Ausnahmen zu toler...
- Liberalismus - Teil 1Der Liberalismus ist eine im 19. Jahrhundert entstandene, im Individualismus wurzelnde Weltanschauung, die in gesellschaftlicher und politischer Hinsicht die freie Entfaltung und Autonomie des Individuums fordert und staatliche Eingriffe auf ein Minimum beschränkt sehen will....
- Liberalismus - Teil 2Robert Nozick (1938-2002) war ein amerikanischer Philosoph, der sich mit den Gerechtigkeitstheorien auseinandersetzte. In seinem Hauptwerk "Anarchy, State, and Utopia“ (1974) liefert er einen Gegenentwurf zu Rawls „Theory of Justice“ (1971). Nozick gilt als Vertreter des Neo-Liberalismus, bei...
- Menschenwürde und Menschenrechte
- MenschenwürdeDie Menschenwürde ist das Wichtigste, was wir im Leben haben. Wie auch im Grundgesetz steht, ist sie unantastbar und kann uns von niemandem genommen werden. Da dieser Begriff der Würde so entscheidend für unser Selbstbild und unser Verständnis von Gesellschaft ist und sich im Laufe der Zeit sehr...
- Menschenrechte Der Begriff der Menschenwürde ist einer der zentralsten Begriffe unseres modernen Rechtsverständnisses, der sich auf dem Hintergrund der Schrecken der Nazizeit und deren Verbrechen gegen die Menschlichkeit herausgebildet hat. Doch geht mit dem Begriff der Menschenwürde immer noch ein zweiter einh...
- Wichtige Begriffe zu MenschenrechtenNaturrechtRecht, das unabhängig von der gesetzlich fixierten Rechtsauffassung eines bestimmten Staates o.Ä. in der Vernunft des Menschen begründet ist.RechtspositivismusRecht und Moral sind streng voneinander getrennt, da in einer Gesellschaft keine einheitliche Moralvorstellung herrscht. Recht w...
- Theorien der Gerechtigkeit
- Q1 - Anthropologie und Bereichsethiken
- Geschichte
- Q1 - Nation, Kapitalismus und Expansion: Europa und die Welt im 19. Jahrhundert – Ambivalenzen des politischen und wirtschaftlichen Fortschritts
- Die deutsche Revolution von 1848/49 – Markstein auf dem Weg zu Parlamentarismus, Demokratie und Nationalstaat?
- Wichtige Begriffe des VormärzUm die Geschehnisse des Vormärz verstehen zu können, müssen wir zunächst ein paar wichtige Begriffe kennenlernen. In Q1 soll es laut Abiturerlass um die „Entstehung, Entwicklung und Unterdrückung der liberal-nationalen Bewegung“ gehen. Was aber ist liberal, was national? Schauen wir uns zun...
- Befreiungskriege Unter dem Begriff Befreiungskriege werden die Kriege zwischen 1813 und 1815 in Mitteleuropa zusammengefasst, die die Herrschaft Napoleons beendeten. Als Vormärz wird die Zeit vor der Märzrevolution von 1848/49 bezeichnet....
- Wiener Kongress und Deutscher BundNachdem Napoleon besiegt war, musste Europa neu geordnet werden. Dazu berieten sich auf dem Wiener Kongress 1815 die Siegermächte der Befreiungskriege: Österreich, Preußen, Russland, Frankreich und Großbritannien unter der Führung des österreichischen Außenministers Fürst von Metternich. Es ...
- Liberale Bewegung im Deutschen BundDer Funke der Französischen Revolution konnte bzw. wollte nicht so richtig überspringen. Während die Masse des Volkes weitgehend unpolitisch blieb, formierte sich in Deutschland dennoch eine liberale und nationale Bewegung, die nach den Befreiungskriegen stärker wurde. Dabei spaltete sich die Be...
- Ereignisse des VormärzBereits 1815 wurde die erste deutsche Burschenschaft in Jena gegründet. Dies war ein erster Zusammenschluss von liberal und national eingestellten Studenten und ein Vorbild für andere deutsche Städte. 1817 entwickelten sie Grundsätze und Ziele ihres Handelns: Forderung eines Nationalstaates und...
- Deutsche Revolution 1848/1849
- Beginn der Revolution 1848/1849In Frankreich war noch lange keine Ruhe eingekehrt. Die revolutionären Bestrebungen mündeten in der Februarrevolution, die auch auf Deutschland und andere europäische Staaten übergriff. Die Februarrevolution in Frankreich war der Anlass für die Märzrevolution in Deutschland.In Deutschland gab ...
- Politische Strömungen und Forderungen der Revolution 1848/1849 So kam am Anfang des Jahres 1848 die Frage auf, wie die Wahlen zur Nationalversammlung aussehen sollten. Deshalb traf sich im März 1848 die sog. Heidelberger Versammlung. Führende Oppositionelle einigten sich darauf Vertrauensmänner ohne direkten Auftrag vom Volk nach Frankfurt zu schicken. Ende ...
- Nationale Frage: Groß- oder Kleindeutsche Lösung?In der Nationalversammlung stellten sich viele Verfassungsfragen, unter anderem auch, wie die geforderte Nation aussehen sollte: Wo sollten ihre Grenzen verlaufen? Welche Staaten gehören dazu und welche nicht? Sicher war nur eins, man wollte keine Gebiete des Deutschen Bundes aufgeben.Diskutiert wu...
- Ende der Revolution 1848/1849An der Spitze dieses neuen Staates sollte ein Erbkaiser stehen. Friedrich Wilhelm IV wurde am 28. März 1849 von den Abgeordneten für diese Position gewählt. Allerdings lehnte er die Kaiserkrone ab, da er das Prinzip der Volkssouveränität ablehnte und nur eine Legitimation durch die Fürsten akz...
- Auslöser und Gründe der Revolution 1848/1849Jetzt weißt du bereits, wie die Revolution 1848 abgelaufen ist und was wichtige Forderungen und Positionen der Revolutionäre waren. Für ein erfolgreiches Abitur reicht dieses Wissen aber nicht aus. Du musst auch in der Lage sein, diese Geschehnisse zu interpretieren – also warum die Revolution ...
- Einfluss der Französischen Revolution auf die Revolution 1848/1849Die Französische Revolution war zwar Vorbild für die deutsche Nationalbewegung – sie stellte die Revolutionäre aber auch vor gewisse Herausforderungen: Der revolutionäre Funke sprang nicht in seiner Gesamtheit auf Deutschland über. Es fand keine grundlegende Umwälzung der Verhältnisse statt...
- Ursachen des Scheiterns der Revolution 1848/1849Das Scheitern der Revolution lässt sich auf mehreren Ebenen betrachten. Schauen wir uns zunächst einmal die Nationalversammlung an. Diese stand vor vier zentralen Problemen: Schwierigkeiten der Schaffung eines Nationalstaates (Groß- oder Kleindeutsche Lösung): Man konnte sich auf keine der vorg...
- Bleibende Errungenschaften der Revolution 1848/1849 Nicht alles an der Revolution war schlecht. Auch wenn es der deutschen Revolution nicht gelang, einen deutschen Nationalstaat zu gründen, hinterließ sie einige Errungenschaften: Zunächst ebnete sie den Weg für die spätere Parlamentarisierung. Außerdem konnte sie die Presse-, Versammlungs- und...
- Nationale Bewegungen in Europa am Beispiel Italiens oder PolensIm folgenden Kapitel wird ein Thema des Leistungskurses zu diesem Kapitel besprochen. Diese werden wir allerdings nicht mehr so ausführlich besprechen, wie die bisherigen. Das hat den einfachen Grund, dass es beim LK meistens mehr darauf ankommt, Zusammenhänge zu verstehen und die richtigen Verbin...
- Herrschaft und Gesellschaft im europäischen Vergleich – ein liberaler Nationalstaat für alle Bürger?
- Das Kaiserreich zwischen Tradition und Moderne Die Revolutionsbewegung von 1848/1849 strebte die Gründung eines Nationalstaats an, scheiterte jedoch bei dem Versuch. Mit der Gründung des deutschen Reiches am 18.01.1871, bei der sich König Wilhelm I. im Spiegelsaal von Versailles zum deutschen Kaiser proklamierte, war dieses Ziel jedoch wieder...
- Rapide Industrialisierung und moderne KlassengesellschaftDie Einleitung in ein modernes Zeitalter erfolgte maßgeblich aufgrund der beschleunigten Industrialisierung ab den 1850er Jahren. Während des deutschen Kaiserreiches ab 1871 war bereits die Phase der Hochindustrialisierung im Gange. Dank dieser gelang Deutschland der Durchbruch und Wechsel von ein...
- Politik und Gesellschaft im Kaiserreich: Inklusions- und Exklusionsstrategien Nachdem nicht nur die Revolution 1848/1849 gescheitert war und auch die Idee und Gründung eines Nationalstaates der Liberalen Kräfte im Jahr der Reichsgründung 1871 enttäuscht wurde, da es keine demokratisch-parlamentarische Ordnung gab, rückte die politische Umsetzung einer gesellschaftlich um...
- Bismarcks Verhältnis zu den ParteienBismarcks Verhältnis zu den Parteien war schwierig. Bismarck geriet gleich zu Beginn seiner Regentschaft mit der Zentrumspartei in eine scharfe Auseinandersetzung über die Stellung der Kirche, die durch eine fokussierte Säkularisierung (Loslösung des Staates von der Kirche) von Bismarck in Fra...
- Großbritannien - Tradition des parlamentarischen SystemsIm Vergleich zu Deutschland hatte sich in Großbritannien im 19. Jahrhundert bereits ein parlamentarisches System etabliert, dem ein Demokratisierungsprozess voraus gegangen war, weshalb Großbritannien auch als „Mutter der modernen Demokratie“ bezeichnet wird. War diese Art von politischer Ordn...
- Frankreich - Bonapartismus und politischer Wandel durch RevolutionUnter Napoleon Bonaparte wurde ab dem 19. Jahrhundert - im Gegensatz zum britischen Parlamentarismus - eine moderne Diktatur mit Hilfe des Militärs, der Bürokratie und von Scheinwahlen etabliert. Diese Art der Politikführung wird auch als Bonapartismus bezeichnet. Louis Bonaparte, Napoleons Neffe...
- Die Diskussion über die These vom deutschen „Sonderweg“ Mit dem Sieg Deutschlands über Frankreich und der Gründung des deutschen Reiches im Spiegelsaal von Versailles im Jahr 1871 war Otto von Bismarck an seinem politischen und persönlichen Zenit angekommen. Die Mehrheit der deutschen Historiker stand hinter Bismarck und seiner teilweise ambivalenten ...
- Der Erste Weltkrieg – Zerstörung der alten europäischen Ordnung
- Außenpolitische Wende von Bismarck zu Wilhelm II
- Ausgangslage: ReaktionsäraDer deutsche Traum von einem Nationalstaat wurde weder 1815 durch den Wiener Kongress, noch 1848/49 durch die gescheiterte Revolution erfüllt. Bevor wir erklären, wie es später doch noch zur deutschen Einheit kam, schauen wir uns die Ausgangslage an. Eine wichtige Frage nach 1848 war: Wer hat je...
- Hegemonialkriege Als Hegemonialkriege oder deutsche Einigungskriege werden drei Kriege bezeichnet, die Preußen zwischen 1864 und 1871 gegen Dänemark, Österreich und Frankreich führte und die in der Gründung des deutschen Kaiserreichs endeten. ...
- Gründung des Deutschen KaiserreichesAls Folge des Deutsch-Französischen Krieges kann die „Deutsche Reichsgründung“ gesehen werden. Natürlich sorgte nicht alleine die Kriegserklärung und der Kriegsgewinn dafür, dass das deutsche Kaiserreich gegründet wurde. Auch im Volk waren ähnlich starke Bestrebungen nach einem Nationalst...
- Bismarcks Außenpolitik - Bündnissystem Bismarck nutzte ein durchdachtes Bündnissystem, um das Deutsche Kaiserreich friedlich zur Großmacht aufzubauen. Dabei war er keinesfalls ein Pazifist – er nutzte die Friedensstrategie nur, um andere Staaten nicht zu bedrohen, also als Mittel zum Zweck. Er schloss Abkommen mit anderen europäisch...
- Bismarcks Außenpolitik - Strategien und Ziele Bismarcks Außenpolitik war zu Anfang auf ein klares Ziel ausgerichtet: Durch ein komplexes Bündnissystem sollte verhindert werden, dass andere Staaten gegen Deutschland in den Krieg ziehen. Dabei machte er sich die folgenden große Konflikte dieser Zeit zunutze: Russland und Großbritannien stri...
- Wichtige Ereignisse der Außenpolitik 1871 – 1890 Neben den innenpolitischen Veränderungen und Bismarks außenpolitischen Bündnissen gab es noch einige wichtige außenpolitische Ereignisse, die im Folgenden näher beschrieben werden....
- Wandel der Außenpolitik Bismarck und Wilhelm II strebten sehr unterschiedliche außenpolitische Ziele an. Bismarcks Strategien haben wir bereits aufgeführt. Schauen wir also, was sich unter Wilhelm II geändert hat....
- Der Weg in den ersten Weltkrieg
- MarokkokriseViele Krisen vor dem Ersten Weltkrieg fanden nicht direkt in Europa statt. Vielmehr ging es um imperialistische Machtbestrebungen und Stellvertreterkriege (= Krieg in kleineren Staaten, die unter dem Einfluss anderer, großer Staaten stehen und somit stellvertretend den Krieg für die Großmächte a...
- BalkankriegeAls Balkankriege werden zwei Kriege bezeichnet, die kurz vor dem Ersten Weltkrieg auf der Balkan-Halbinsel stattfanden. ...
- Ermordung von Erzherzog Franz FerdinandZurück zum Ausbruch des Ersten Weltkrieges. Schauen wir uns an, wo wir kurz vor dem Beginn dieses Krieges standen: In Europa herrschte eifriges Wettrüsten und jeder Staat wollte seine Macht ausweiten. Der Balkan war ein Krisenherd, auf dem viele Konflikte ausgetragen wurden. Frankreich, Russland u...
- JulikriseDas Attentat hatte weltweit Bestürzung ausgelöst. In Österreich-Ungarn wurden Stimmen laut, militärisch gegen Serbien vorzugehen. Wie bereits angekündigt kommt hier noch einmal der Balkan ins Spiel. Österreich und Serbien standen sich nämlich schon vorher gegenüber: Beide hatten Interesse an...
- Vergleich der Revolution von 1848 und der Reichsgründung 1871 Nachdem wir nun die Reichsgründung 1871 behandelt haben, müssen wir noch ein Thema "nachholen". Im Abiturerlass steht unter Q1.1 Absatz 3 das Thema „Vergleich der Revolution 1848 und der Reichsgründung 1871" in Klammern als Ergänzung zu "Ursachen des Scheiterns der Revolution und bleibende Err...
- Vertiefende Auseinandersetzung mit Interpretationen und Kontroversen zum Kriegsausbruch Bisher ging es zunächst um den Weg von Bismarck zu Wilhelm II. Hier haben wir uns mit der Reichsgründung und der Außenpolitik Bismarcks beschäftigt. Dann haben wir uns angeschaut, welche Ereignisse zum Ersten Weltkrieg geführt haben. Kleiner Hinweis: Auch hier ging es um die Folgen aggres...
- Außenpolitische Wende von Bismarck zu Wilhelm II
- Die deutsche Revolution von 1848/49 – Markstein auf dem Weg zu Parlamentarismus, Demokratie und Nationalstaat?
- Q2 - Die Welt zwischen Demokratie und Diktatur (1917–1945)
- Die Weimarer Republik als erste deutsche Demokratie
- Entstehungsbedingungen und innenpolitische Entwicklung der Weimarer Republik
- Ausgangslage nach dem Ersten WeltkriegDieses Kapitel steigt direkt nach dem Ende des Ersten Weltkrieges ein. Obwohl die Details des Verlaufes des Ersten Weltkrieges nicht abiturrelevant sind, wollen wir dir kurz erzählen, wie die Lage 1918 in Europa aussah. ...
- Die Novemberrevolution - Auslöser und Ursachen Die Novemberrevolution (oder auch Revolution von 1918/1919) brach gegen Ende des Ersten Weltkriegs in Deutschland aus und führte zur Umwandlung des Deutschen Reiches zur parlamentarischen Demokratie, der Weimarer Republik.Während des Ersten Weltkriegs hatte das Militär die Macht in Deutschland fa...
- Die Novemberrevolution - Drei unterschiedliche GruppenWährend der Novemberrevolution gab es drei wichtige Interessensgruppen, die jeweils mit einem wichtigen Namen verbunden sind: Zunächst gab es die alten Eliten, die den Erfolg einer Revolution vermeiden und die alte Ordnung so weit wie möglich aufrechterhalten wollten. Wichtigster Vertreter der ...
- Die Novemberrevolution - VerlaufWie es zur Novemberrevolution kam und welche Interessen hier vertreten wurden, haben wir oben bereits erklärt. Doch wie ist die Revolution verlaufen und zu welchem Ergebnis hat sie geführt? Diese Fragen wollen wir dir in diesem Kapitel beantworten. Am einfachsten lassen sich diese Fragen beantwor...
- Parteien der Weimarer RepublikAtme am besten nochmal tief durch, denn die nächsten zwei Kapitel zur Weimarer Republik werden leider etwas trockener. Sie sind aber leider unverzichtbar für deine Abiturvorbereitung und zumindest gut auswendig zu lernen....
- Verfassung der Weimarer Republik Ein weiteres trockenes, aber umso wichtigeres Thema der Weimarer Republik ist die Verfassung. Sie wird von vielen Historikern als ein Problem der Weimarer Republik angesehen, das die spätere nationalsozialistische Machtübernahme begünstigte. Schau dir zunächst mal in aller Ruhe das Schaubild an....
- Probleme der Weimarer Verfassung Die Weimarer Verfassung stellte in vielen Bereichen eine Neuheit für Deutschland dar: Zum ersten Mal waren die Gewaltenteilung und die Grundrechte verfassungsrechtlich verankert. Zudem ging die Staatsgewalt vom Volke aus. ...
- Krisenjahr 1923Als Krisenjahr der Weimarer Republik wird das Jahr 1923 bezeichnet. Innerhalb dieses Jahres hatte die noch junge Weimarer Republik mehrere Probleme zu bewältigen: Die Hyperinflation der deutschen Währung, die Ruhrbesetzung und den Ruhrkampf, den Deutschen Oktober, Separatisten und Aufstände im We...
- Zeiten der StabilisierungNach dem ziemlich holprigen Start der Weimarer Republik entspannte sich die Lage wieder. 1924 bis 1928 bezeichnet man deshalb als zweite Phase der Weimarer Republik, der Phase der Stabilisierung. Die Wirtschaft ging schrittweise wieder bergauf, die politische Gewalt ließ nach. Auch gesellschaftlich...
- 1929-WeltwirtschaftskriseDie Weltwirtschaftskrise begann als Krise der industriellen Überproduktion und der hemmungslosen Börsenspekulation in den USA. Am 25.10.1929 kam es zum Zusammenbruch der New Yorker Börse (Schwarzer Freitag). Die Folgen waren extreme Arbeitslosigkeit und Armut. 1930 griff die Krise durch internati...
- PräsidialregierungenIn den Jahren 1930 bis 1933 hatte die Weimarer Republik keine stabilen Regierungen mehr. Sie wurde von sogenannten Präsidialkabinetten regiert. Das waren Regierungen, die mithilfe des Reichspräsidenten und dessen Notverordnungen und ohne die Unterstützung des Parlaments regierten. In den drei Jah...
- Machtergreifung der NationalsozialistenNach einem kurzen Aufschwung in den Goldenen Zwanziger Jahren war die Weimarer Republik mit den Präsidialkabinetten wieder in eine tiefe politische Krise geschlittert. Davon profitierte die NSDAP. Bei den Wahlen 1930 zog sie bereits als zweitstärkste Kraft in den Reichstag ein, 1932 war sie die s...
- Ziele, Methoden und Ergebnisse der Weimarer Außenpolitik
- Ziele, Methoden und Ergebnisse der Weimarer Außenpolitik Bisher sind wir die Ereignisse der Weimarer Republik ziemlich chronologisch durchgegangen. In den nächsten Kapiteln legen wir den Fokus nun auf die Ziele, Methoden und Ergebnisse der Weimarer Außenpolitik. Im Kerncurriculum heißt es hierzu "Ziele, Methoden und Ergebnisse der Weimarer Außenpoliti...
- Versailler Vertrag und DolchstoßlegendeEin sehr wichtiges Thema der Weimarer Außenpolitik war der Versailler Vertrag. Am 28.06.1919 unterzeichnete die deutsche Abordnung am Ende des Ersten Weltkriegs den Friedensvertrag im Spiegelsaal von Versailles. Die Deutschen waren die klaren Kriegsverlierer und verloren die alte Großmachtstellung...
- RevisionismusZu Beginn der Weimarer Republik waren die Hauptziele der Außenpolitik: die Revision des Versailler Vertrages. Dazu zählte die Lösung bzw. Senkung der Reparationsanforderungen, Räumung der besetzten Westzonen und die Wiedergewinnung der verlorenen Gebiete. Aufhebung der außenpolitischen Isolat...
- Außenpolitik: West- und Ostorientierung und Politik StresemannsIn den Anfangsjahren war die Weimarer Republik isoliert. Sie verfolgte also zwei Ziele: Wieder in das Machtgefüge der internationalen Mächte aufgenommen zu werden und den Versailler Vertrag zu revidieren. An den Osten konnte man sich relativ schnell nach Kriegsende, 1922, annähern. Durch den Rapa...
- Vertiefende Auseinandersetzung mit Interpretationen und Kontroversen über die Beurteilung der Deutschen Revolution 1918/19In den letzten Kapiteln haben wir uns die Weimarer Republik in all ihren Facetten angeschaut. Wie ist sie entstanden, wie sah die Außenpolitik aus und wie änderte sich die Gesellschaft? Ein Thema war auch die Novemberrevolution, die zur Gründung der Weimarer Republik führte. Auf diese bezieht si...
- Entstehungsbedingungen und innenpolitische Entwicklung der Weimarer Republik
- Aushöhlung der Demokratie und Errichtung der Diktatur in Deutschland
- Entstehung und Entwicklung der NSDAP Die Nationalsozialistische Deutsche Arbeiterpartei (NSDAP) war eine Partei der Weimarer Republik und des Dritten Reichs Ihren Ursprung hatte sie in Bayern, bis 1933 stieg sie zu Massenpartei auf und herrschte von 1933 bis 1945 als einzig erlaubte Partei Deutschlands, bis sie 1945 verboten wurde. Ihr...
- Ursachen des Scheiterns der Weimarer Republik Schauen wir nochmal auf das Ende der Weimarer Republik. Dass sie scheiterte hatte verschiedene Gründe. Um alles besser nachvollziehen zu können, haben wir diese in drei Kategorien aufgeteilt: Politische, soziokulturelle und ökonomische Gründe....
- Errichtung des totalitären Staates Wir haben nun ausführlich erklärt, was zum Scheitern der Weimarer Republik führte und wie die NSDAP an die Macht kam. Zusammenfassend lässt sich sagen: Die Weimarer Republik hatte noch einige strukturelle Schwächen. Auch die Bevölkerung hatte keine Erfahrung mit der Demokratie. Sie wurden nich...
- War die Weimarer Republik zum Scheitern verurteilt? In den letzten Kapiteln haben wir uns hauptsächlich mit den Schwächen der Weimarer Republik auseinandergesetzt und überlegt, welche Gründe zu ihrem Scheitern beitrugen. Auch den Aufstieg der NSDAP und die Machtergreifung der Nationalsozialisten haben wir betrachtet. ...
- Die nationalsozialistische Diktatur – Zerstörung von Demokratie und Menschenrechten in Deutschland und Europa
- Widerstand der deutschen BevölkerungDer Widerstand gegen das NS-Regime nahm die unterschiedlichsten Formen an. Manche weigerten sich einfach, den Regeln der Nationalsozialisten zu folgen und grüßten zum Beispiel nicht mit dem Hitlergruß. Andere zeigten zwar öffentlich keinen Widerstand, aber versteckten zum Beispiel die Verfolgten...
- NS-Außenpolitik im Kontext der internationalen BeziehungenEin paar außenpolitische Prinzipien des Nationalsozialismus haben wir bereits besprochen: Arbeitsbeschaffung und Wehrhaftmachung im Inneren, Autarkiepolitik, Aufrüstung und Staatsverschuldung. Bleibt noch zu klären, welche Ziele das NS-Regime damit verfolgte. Das Gesamtziel war die Wiedergewinnu...
- Kriegsvorbereitungen und ExpansionWelche Ideologie hinter der Expansion und der Außenpolitik Hitlers stand, haben wir bereits erklärt. Schauen wir uns deshalb nochmal zwei Ereignisse der Außenpolitik an, die für Expansion und die Kriegsvorbereitungen stehen: Den „Anschluss“ Österreichs und die Münchener Konferenz. Nach dem...
- Appeasement-Politik des WestensAls Appeasement-Politik („appease“ = englisch für besänftigen, beschwichtigen) wird die Beschwichtigungspolitik Großbritanniens und der anderen Westmächte im Vorfeld des Zweiten Weltkrieges bezeichnet, die darauf abzielte einen Krieg zu vermeiden und den Frieden zu bewahren. Diese Politik wu...
- Rolle der UdSSRDie UdSSR fühlte sich von den kapitalistischen Großmächten bedroht. Ihrer Ansicht nach war ein Krieg unvermeidbar – sie wollten ihn nur lange genug herauszögern, um sich bestmöglich vorbereiten zu können. Aus dieser Motivation heraus schloss die Sowjetunion einen Nichtangriffspakt mit dem De...
- Rassenideologischer Vernichtungskrieg gegen die SowjetunionAls Vernichtungskrieg wird ein Krieg bezeichnet, der die völlige Vernichtung des Gegners zum Ziel hat. Das Deutsche Reich führte im Zweiten Weltkrieg einen Weltanschauungs- und Vernichtungskrieg gegen die Sowjetunion, den es mit rassenideologischen Argumenten begründete. ...
- Rolle von Schutzstaffel und WehrmachtBei diesem Vernichtungskrieg spielten auch die Wehrmacht und die Schutzstaffel (SS) eine große Rolle. Die Wehrmacht war maßgeblich beteiligt an der Vernichtung großer Bevölkerungsteile der „Feindstaaten“. Die Soldaten plünderten und raubten, wo auch immer sie hinkamen. Die Zivilbevölkerung...
- Holocaust und Mord an Sinti und RomaWährend der Herrschaft des NS-Regimes wurden viele Bevölkerungsgruppen aufgrund rassenideologischer Ansichten verfolgt und ermordet. Als Holocaust bezeichnet man dabei die systematische Verfolgung, Gettoisierung und Massenvernichtung der Juden in Deutschland und Europa. Auch Sinti und Roma, Homose...
- Lokal-/regionalgeschichtliche RechercheHier haben wir uns mit allen Aspekten des NS-Staates auseinandergesetzt: Dem Aufbau, die Grundsätze, Propaganda und Rassismus, Aufrüstung, Arbeitsbeschaffung, Ausschluss von „Andersartigen“, Verfolgung und Ermordung von Juden und anderen Gruppen. Außerdem haben wir uns im Rahmen der Außenpol...
- Die Weimarer Republik als erste deutsche Demokratie
- Q3 - Ost-West-Konflikt, postkoloniale Welt und Globalisierung
- Die Teilung Deutschlands – eine Nation, zwei Staaten
- Ausgangslage nach dem Zweiten WeltkriegSpulen wir kurz vor in das Jahr 1945. Deutschland hat den Krieg verloren. Am 8. Mai 1945 kam es zur Kapitulation und somit zum völligen Zusammenbruch und zur totalen Niederlage Deutschlands. USA und UdSSR hatten die Vorherrschaft in der Welt übernommen. Schauen wir uns zunächst an, wie die Lage i...
- Anti-Hitler-Koalition und BlockbildungAls Anti-Hitler-Koalition wird das Zweckbündnis von Großbritannien, USA und UdSSR bezeichnet, das 1941 gegründet wurde (nach Kriegseintritt der USA am 8.12.1941), um das nationalsozialistische Deutschland zu bekämpfen. Sie diente zudem als Ausgangspunkt zur Gründung der Vereinten Nationen. Nach...
- Konferenzen und internationale Zusammenarbeit Gegen Ende des Zweiten Weltkrieges fanden verschiedene internationale Konferenzen statt, bei denen die Staaten über das jeweilige Vorgehen und auch den Umgang mit Deutschland nach dem Krieg verhandelten. Im Folgenden stellen wir dir die Konferenzen im Einzelnen vor. ...
- Deutsche TeilungKonzentrieren wir uns nun erstmal wieder auf Deutschland. Wir haben dir in vorherigen Kapiteln bereits einige Konferenzen vorgestellt, auf denen über die Zukunft Deutschlands entschieden wurde. Denn nach Ende des Zweiten Weltkrieges war Deutschland klar geschlagen und hatte kein Mitspracherecht –...
- Anerkennung der deutschen Staaten Kurz nach Ende des Krieges, im Laufe der 50er Jahre, verhärtete sich der Konflikt zwischen Ost- und Westmächten. Die Frage zur Einheit oder Teilung Deutschlands wurde zum Thema des Kalten Krieges. Dabei hatten die USA und die Sowjetunion unterschiedliche Ansichten. Die Sowjetunion versuchte unter...
- Westintegration Die Teilung Deutschlands war ein Ergebnis des Konflikts zwischen West und Ost. Und dadurch wurden auch die Aufteilung Deutschlands und die Vorherrschaft in Europa zum Konflikt des Kalten Krieges. Die Gründung der beiden Staaten haben wir dir bereits erklärt, auch wie die beiden Großmächte UdSSR ...
- Phasen der deutschen Teilung im internationalen KontextDie Frage nach der deutschen Teilung war ein weltpolitisches Thema. Stellvertretend wurden hier die Konflikte zwischen USA und UdSSR ausgetragen. So änderte sich auch die Haltung der Besatzungsmächte im Laufe der Jahre. In den 50er-Jahren spitzten sich die Feindseligkeiten zunächst zu, die Fronte...
- EntspannungspolitikAls Entspannungspolitik wird der Zeitraum des Kalten Krieges, zwischen den 60er und 80er Jahren bezeichnet. Während diesen Jahren strebten die Siegermächte eine friedliche Koexistenz an und kamen sich politisch etwas näher. Diese Entspannung hielt nur bis in die 80er Jahre an. Wichtige Maßnahmen...
- „Neue Eiszeit“Die Entspannungs-Phase hielt nicht dauerhaft an. In den 70er und 80er Jahren bahnte sich eine sogenannte „neue Eiszeit“ an. Bevor wir hier weitererklären, müssen wir zunächst noch einen weiteren Begriff einführen: Das Gleichgewicht des Schreckens. Dieser Begriff, der auch manchmal als „wec...
- NATO-DoppelbeschlussAufgrund der Forderung, dass sich Europa im Notfall auch ohne Hilfe der USA verteidigen können müsste, kam es am 12.12.1979 deshalb zum NATO-Doppelbeschluss. Zum einen kündigte die NATO die Aufstellung neuer Atomraketen in Westeuropa an. Dies begründeten sie mit dem Ungleichgewicht der...
- Opposition und Reform im Ostblock Die Sowjetunion war die klar stärkste Macht im Ostblock. Gegen diese sowjetische Vormachtstellung lehnten sich einige Staaten des Ostblockes auf. Generell war der Ostblock nicht so geeint, wie der Westen. China und die UdSSR wollten beide den größten Einfluss im Ostblock für sich beanspruchen. ...
- Deutschland von der Teilung zur Einheit
- Deutsche Teilung und Beziehung der BRD und der DDRIn diesem Kapitel geht es um die deutsche Teilung und ihren Weg zur Einheit – allerdings nicht aus internationaler, sondern innerdeutscher Perspektive. Schauen wir uns deshalb erstmal beide Staaten (BRD und DDR) im Vergleich an. Beide deutschen Staaten wurden 1949 gegründet. In der BRD wurde das...
- Innerdeutsche Beziehungen – Zuspitzung des Kalten Krieges (bis 1969)Der Anfang der deutsch-deutschen Beziehungen war durch den Kalten Krieg und die Rivalitäten zwischen Ost und West geprägt. Die BRD wurde an den Westen angebunden, die DDR in den Ostblock integriert. So entstand kein freundschaftliches Verhältnis der beiden deutschen Staaten. Drei Begriffe solltes...
- Innerdeutsche Beziehungen – Neue Ostpolitik (bis 1989)Mit dem Machtwechsel in der BRD änderte sich auch der politische Kurs des Landes. 1969 wurde Willy Brandt von der SPD Bundeskanzler und löste somit Kurt Georg Kiesinger ab. Bis dahin waren alles Bundeskanzler CDU-Mitglieder. Unter Willy Brandt (SPD) wurde eine neue Ostpolitik verfolgt, die sich au...
- Die Letzten Jahre der DDRIm Folgenden gehen wir genauer auf die Ereignisse in den letzten Jahren der DDR ein. Im Mai 1989 begann Ungarn mit der Demontage ihres Grenzzaunes. Bisher hatte der Zaun die Außengrenze Ungarns gesichert. Das hatte zunächst praktische Gründe: Bei einer Überprüfung kam heraus, dass der Zaun rost...
- Kommunalwahlen im Mai 1989Parallel zu diesen Ereignissen fanden am 6. Mai 1989 in der DDR Kommunalwahlen statt. Wie bisher auch, waren dies keine freien Wahlen. Es waren nur Kandidaten der Einheitsliste der Nationalen Front (Zusammenschluss der Parteien und Massenorganisationen der DDR) zugelassen. Dadurch wurden freie Wahle...
- Internationaler Kontext: Glasnost und PerestroikaBevor wir weiter in der deutschen Geschichte voranschreiten, müssen wir noch einmal auf den internationalen Kontext schauen. Wir haben schon gesagt, dass die Vorkommnisse im Osten, die Revolution in der DDR begünstigten. Schauen wir uns also an, was seit dem Amtseintritt Michail Gorbatschows in de...
- Deutsche WiedervereinigungKonzentrieren wir uns wieder auf die deutsche Geschichte. Wie ging es nach dem Machtverlust der SED in der DDR weiter? Und wie kam es zur deutschen Wiedervereinigung? In der DDR hatte die Bevölkerung schon während der friedlichen Revolution eine deutsche Einheit gefordert. Bei den Treffen zum Run...
- Die Wiedervereinigung im internationalen KontextDie Wiedervereinigung Deutschlands war natürlich nicht nur innerdeutsch ein wichtiges Thema. Es beschäftigte auch die Weltpolitik, waren die deutschen Staaten doch lange Krisenpunkt zwischen Ost und West gewesen. Die internationalen Staaten trafen sich seit Anfang 1990 zu sogenannten Zwei-plus-Vi...
- Vertiefende Auseinandersetzung mit Interpretationen und Kontroversen zu den Auswirkungen der Entspannungspolitik In den Kapiteln zu "Deutschland von der Teilung zur Einheit" haben wir uns auf die innerdeutsche Beziehung konzentriert. Wir haben geschaut, wie die beiden Staaten zueinander standen und wie es nach anfänglicher Ablehnung und Feindschaft zur Wiedervereinigung der BRD und DDR kam. ...
- Die Teilung Deutschlands – eine Nation, zwei Staaten
- Q1 - Nation, Kapitalismus und Expansion: Europa und die Welt im 19. Jahrhundert – Ambivalenzen des politischen und wirtschaftlichen Fortschritts
- Gesundheit
- Grundlagen
- Die ZelleDie Zelle ist die kleinste lebende Einheit. Sie ist in der Lage sich selbstständig zu vermehren (man sagt: Zellen teilen sich) und viele unterschiedliche Aufgaben zu übernehmen. Um die Überlebenswahrscheinlichkeit zu erhöhen, arbeiten Zellen häufig als mehrzellige Organismen (Tiere, Menschen, P...
- Der ZellkernDer Zellkern ist ein rundes, poriges Organell, die das Erbgut, also die DNA, beinhaltet. In ihm ist die DNA geschützt und in zweimal 23 Chromosomen organisiert. Im Zellkern wird reguliert, welche Gene in mRNA umgeschrieben (transkribiert) werden. Die Poren des Zellkerns bestimmen dabei selektiv, we...
- Die DNADie DNA (Desoxyribonukleinsäure) ist zwar eine lange Molekülstruktur und kein Organell, aber dennoch wichtig, denn sie stellt unser Erbgut dar. Sie besteht aus zwei langen Ketten, die sich gegenüberstehen und in sich gewunden sind. Man bezeichnet die DNA daher auch als DNA-Doppelstrang. Jede Kett...
- Das endoplasmatische RetikulumDas endoplasmatische Retikulum (ER) ist ein sehr großes und labyrinthartiges Organell, das aus einer Lipiddoppelmembran gebildet wird. Es liegt wie ein Schlauchsystem um den Zellkern herum und dient vor allem als Synthese- und Speicherort für Proteine (Abb. 1.4). Das ER kommt in allen kernhaltigen...
- Das RibosomDas Ribosom schreibt mRNA-Moleküle in Peptidketten um (Translation). Es besteht aus zwei Untereinheiten, der 60S- und die 40S-Untereinheit, die selbst wiederum aus ribosomaler RNA (rRNA) aufgebaut sind. Zusammen bilden sie das 80S-Ribosom der Eukaryoten. Das „S“ steht dabei für den Sedimentati...
- Der Golgi-ApparatDer Golgi-Apparat ist wie das ER auch ein Organell, das aus Lipiddoppelmembranen besteht. Er wurde nach seinem Entdecker, dem Italiener Camillo Golgi benannt und besteht im Wesentlichen aus aufeinandergestapelten Membransäcken, den sogenannten Zisternen. Der Golgi-Apparat erhält vom ER aus Protein...
- Das MitochondriumDas Mitochondrium bzw. die Mitochondrien sind die sogenannten „Kraftwerke“ der Zelle. Sie sind ganz besondere Organellen, da sie Zucker (Glukose) in Energie (ATP) umwandeln können. Wird Sauerstoff bei der ATP-Bildung gebraucht, spricht man von der Zellatmung. Das Besondere an den Mitochondrien ...
- Das ZytoskelettDas Zytoskelett ist das Grundgerüst der Zelle. Es besteht aus filamentösen Proteinen (z. B. Aktin), die der Zelle Halt und Stabilität geben. Es fixiert aber auch die Organellen in der Zelle, dient als Gerüst für den Vesikeltransport und ermöglicht die Fortbewegung. Indem das Skelett an einer S...
- Die ZellmembranDamit die Zelle nicht ausläuft und ihn Form gehalten wird, ist sie von einer sogenannten Zellmembran (auch Plasmamembran genannt) umgeben. Auch einige Organellen sind von einer Plasmamembran umgeben. Die Membran schirmt das Zellinnere aber nicht nur von der äußeren Umgebung ab, sondern dient auch...
- Wichtige Prozesse in der ZelleNeben dem Aufbau der Zelle, ist es auch wichtig zu verstehen, wie die vielen verschiedenen Prozesse ablaufen. Im Folgenden werden daher einige grundlegenden Prozesse aufgeführt....
- Ernährung
- Grundlagen einer vollwertigen Ernährung
- Energetische Versorgung Unser Körper ist darauf angewiesen, aus den Nahrungsbestandteilen Eiweiße, Kohlenhydrate, Fette und auch Alkohol Energie zu gewinnen, um lebenswichtige Prozesse aufrechtzuerhalten. Im Folgenden werden die Grundlagen der energetischen Versorgung des Körpers besprochen, bevor in den jeweiligen Kapi...
- WasserWasser ist der Ursprung allen Lebens. Daher ist es auch nicht verwunderlich, dass Wasser der mengenmäßig wichtigste anorganische Bestandteil des menschlichen Körpers ist. Die meisten lebensnotwendigen Funktionen im Körper sind nur in Anwesenheit von Wasser möglich. Dabei dient Wasser unter ande...
- Makro- und MikronährstoffeZu den Makronährstoffen zählen Kohlenhydrate, Fette und Eiweiße. Diese Gruppe zeichnet sich dadurch aus, dass durch Spaltung dieser Substanzen Energie freigesetzt werden kann. Die Makronährstoffen werden in den jeweiligen Kapiteln behandelt....
- BallaststoffeBallaststoffe sind Nahrungsbestandteile, die vorwiegend in Form von Kohlenhydraten in pflanzlichen Lebensmitteln vorkommen. Im Gegensatz zu Makronährstoffen können sie im Dünndarm nicht verdaut oder absorbiert werden. Über verschiedene Mechanismen weisen sie trotzdem positive Effekte für die Ge...
- Anatomie und Physiologie des Verdauungstraktes
- Histologischer Aufbau von VerdauungsorganenDie Verdauungsorgane, die in direktem Kontakt mit Nahrung stehen (Speiseröhre, Magen, Dünndarm und Dickdarm), weisen eine typische Anordnung der Gewebsschichten auf. Dieser Aufbau ermöglicht die Verdauung und Resorption von Nahrungsbestandteilen, die Sekretion von Verdauungsenzymen sowie die Peri...
- MundhöhleDie Mundhöhle ist der erste Abschnitt des menschlichen Verdauungstraktes. Sie enthält die Zähne und die Zunge zur Zerkleinerung der Nahrung sowie Speicheldrüsen. Die Speicheldrüsen produzieren Speichel, der Verdauungsenzyme und Abwehrstoffe enthält und die Speisen gleitfähig macht. Nachdem d...
- Speiseröhre (Ösophagus)Die Speiseröhre ist ein etwa 25–28 cm langes schlauchförmiges Hohlorgan, das die zerkleinerte Nahrung von dem Mundraum in den Magen befördert. Dabei befindet sich die Speiseröhre in direkter Nachbarschaft zu Luftröhre, Hauptschlagader und Herzen. Durch die Peristaltik der glatten Muskulatur k...
- MagenDer Magen ist ein schlauchförmiges Hohlorgan, das Ösophagus und Dünndarm miteinander verbindet. Er liegt unterhalb des Zwerchfells im linken Oberbauch. Durch seinen Aufbau ist der Magen dehnbar und kann sich, je nach Füllungszustand, im Bauchraum auf ein Volumen von bis zu 1,5 Litern ausdehnen. ...
- Dünndarm Der Dünndarm ist ein 5–6 m langes Hohlorgan, das vom Magenausgang bis zum Dickdarm reicht. Er dient vor allem der Nährstoffverdauung sowie der Resorption der Nährstoffe und des Wassers und hat somit eine überlebenswichtige Funktion. Von allen Verdauungsorganen ist der Dünndarm das einzige Org...
- Prinzip der OberflächenvergrößerungVielleicht hast du auch schon einmal gehört, dass die Oberfläche des Dünndarms etwa 400-500 qm2 groß ist. Wie dies bei einem 5 bis 6 m langen Hohlorgan möglich ist und welche Funktion diese Oberflächenvergrößerung hat, erklären wir im Folgenden. An der Oberfläche des Dünndarms findet die ...
- DickdarmDer Dickdarm ist der terminale Abschnitt des Verdauungstraktes und reicht vom Ende des Dünndarms bis zum Anus. Dabei weist er eine Länge von 1,5 m auf. Der Dickdarm entzieht den nicht resorbierten Speisebreiresten aus dem Dünndarm Wasser und Elektrolyte und dickt diese entsprechend ein. Zudem wir...
- Leber und GallenblaseDie Leber ist das wichtigste Stoffwechselorgan des Menschen. Sie befindet sich im rechten Oberbauch direkt unter dem Zwerchfell und erhält über Blutgefäße die Nährstoffe, die durch den Darm absorbiert wurden. Die Leber kann in acht Segmente unterteilt werden, die aufgrund ihrer Blutversorgung i...
- Bauchspeicheldrüse (Pankreas)Die Bauchspeicheldrüse ist ein 12 bis 15 cm langes Organ, das quer im Oberbauch liegt und von Magen und querverlaufendem Dickdarmabschnitt verdeckt wird. Anatomisch kann die Bauchspeicheldrüse in Kopf, Körper und Schwanz unterteilt werden. Die Bauchspeicheldrüse kann funktionell in einen endokri...
- Kohlenhydrate
- Funktion von KohlenhydratenKohlenhydrate werden auch Saccharide genannt und sind eine sehr große Naturstoffklasse. Sie bestehen hauptsächlich aus Kohlenstoff-, Wasserstoff- und Sauerstoffatomen. Aufgrund dieser Hauptbestandteile haben sie ihren Namen „Kohlenhydrat“ erhalten. Mengenmäßig sind sie der wichtigste Energie...
- AufbauKohlenhydrate bestehen aus den Elementen Kohlenstoff (C), Wasserstoff (H) und Sauerstoff (O). Allgemein wird ein Stoff als Kohlenhydrat bezeichnet, wenn er wenigstens drei Kohlenstoffatome enthält, mindestens eine Aldehyd- oder Ketogruppe sowie zwei Hydroxygruppen . ...
- Vorkommen von Kohlenhydraten in LebensmittelnKohlenhydrate sind in unterschiedlicher Menge in fast allen pflanzlichen Lebensmitteln enthalten. Einen besonders hohen Anteil an Kohlenhydraten weisen Getreide (z. B. Weizen, Roggen, Gerste, Hafer, Mais, Reis) sowie Getreideprodukte (Brot, Brötchen, Teigwaren, Müsli, Gebäck) auf. Einige Pseudoge...
- Verdauung und ResorptionWie bereits im vorherigen Kapitel erwähnt, gibt es sehr viele verschiedene Arten von Kohlenhydraten. In unserer Nahrung können diese Kohlenhydrate als Mono- oder Disaccharide, aber auch als Oligo- und Polysaccharide vorkommen. Um letztendlich all diese Formen aufnehmen zu können, ist es nötig, d...
- Regulation des BlutzuckerspiegelsAls Blutzucker bezeichnet man die Konzentration von Glukose im Blut. Bei einem gesunden Menschen liegt der Blutzuckerspiegel normalerweise in einem Bereich von 60–110 mg/dl. In diesem Bereich steht dem Organismus ausreichend schnell verfügbare Glukose zur Verfügung, sodass auch bei einer akuten ...
- Proteine
- FunktionProteine sind für den Körper von großer Wichtigkeit, da sie verschiedenste Funktionen erfüllen und als universelle Bausteine für jede Zelle dienen. Sie können aufgrund ihrer unterschiedlichen Funktionen in sieben Gruppen unterteilt werden: Strukturproteine geben unseren Zellen, Geweben und so...
- Aminosäuren und Peptide Aminosäuren sind die Grundbestandteile von Proteinen. Genauer gesagt, wird die Funktion von Proteinen durch die Reihenfolge der Aminosäuren bestimmt. Aber was sind Aminosäuren? Wie der Name schon vermuten lässt, ist eine Aminosäure ein Molekül mit einer Aminogruppe (NH3) und einer Säuregrup...
- Raumstruktur von ProteinenNach der Proteinbiosynthese liegt die Polypeptidkette im Zytoplasma vor. Bevor die Polypeptidkette jedoch als Protein funktionsbereit ist, müssen sogenannte Faltstrukturen ausgebildet werden, welche dem Protein seine dreidimensionale Struktur verleihen. Viele Proteine bilden diese Faltstrukturen vo...
- Vorkommen von Proteinen in LebensmittelnEin geringer Anteil an Proteinen ist in fast allen Lebensmitteln enthalten. Einige pflanzliche und tierische Lebensmittel weisen jedoch einen recht hohen Proteinanteil auf. Als pflanzliche Proteinquellen dienen vor allem Hülsenfrüchte wie Linsen oder Bohnen, Tofu aus Soja, verschiedene Getreides...
- Verdauung und Resorption von Eiweißen Haben wir eine eiweißhaltige Mahlzeit zu uns genommen, müssen diese Eiweiße, die aus langen miteinander verknüpften Aminosäureketten bestehen, zuerst in kleinere Einheiten gespalten werden, bevor sie von den Schleimhautzellen des Verdauungstraktes resorbiert werden können. Diese Spaltung wird ...
- Fette
- Funktion von FettenFette und Öle gehören zu den essenziellen Grundbausteinen des Körpers. Sie können von diesem nur teilweise selbst synthetisiert werden und müssen daher auch von außen mit der Nahrung zugeführt werden (sogenannte essenzielle Fettsäuren). Die im Körper vorhandenen Fette erfüllen verschiedene...
- Aufbau von Fetten Fette werden im Fachjargon als Triacylglyceride (TAG) oder Triglyceride (TG) bezeichnet. Diese Namen haben die Fette aufgrund ihres Grundgerüsts, welches aus einem Glycerin und drei Fettsäuren besteht (siehe Abbildung). Das Grundgerüst des Glycerins besteht aus drei Kohlenstoffatomen, die über ...
- Vorkommen von Fetten in LebensmittelnAuch Fette sind in einer Vielzahl von Lebensmitteln enthalten. Hierbei variiert der Gehalt von Fetten und somit auch die Kaloriendichte jedoch sehr stark. Fettreiche Lebensmittel sind vor allem Fette und Öle, die aus unterschiedlichen Nahrungsmitteln wie beispielsweise Oliven oder Raps gewonnen wer...
- Verdauung und Resorption von FettenDer Abbau von Fetten ist ein äußerst komplexer Vorgang. Der Grund dafür liegt in den Eigenschaften der Fette. Diese können nur als polare Fettsäuren, die sich mit anderen Substraten zu Mizellen zusammenlagern, die Membran der Verdauungsorgane passieren. Daher ist es nötig, dass die über die N...
- Ernährungsabhängige Erkrankungen
- Diabetes mellitus
- HäufigkeitAktuell leiden in Deutschland etwa 6,9 Millionen Menschen an Diabetes mellitus. Der Großteil (ca. 95%) dieser Erkrankungen ist auf den Diabetes Typ 2 zurückzuführen (die Daten auf die wir uns in diesem Kapitel beziehen, stammen aus dem "Deutscher Gesundheitsbericht Diabetes 2020"). Vor 100 Jahren...
- Diabetes-Typen Beim Diabetes mellitus Typ 1 kommt es durch erbliche Veranlagung und äußere Faktoren (z. B. bestimmte Virusinfektionen) zu einer Fehlsteuerung des Immunsystems. Dieses erkennt die insulinproduzierenden β-Zellen der Bauchspeicheldrüse als fremd und greifen diese an. Durch den Untergang der β-Zel...
- DiagnostikDie Diagnose eines Diabetes mellitus ist anhand verschiedener Parameter möglich, die eine Auskunft über die Regulation des Blutzuckerspiegels ermöglichen. Anhand der Werte kann eine Unterteilung in gesund, Prädiabetes und Diabetes mellitus erfolgen. Als Prädiabetes wird die Vorstufe des Diabete...
- Folgen der DiabeteserkrankungZu Beginn der Erkrankung merken die Betroffen meist keine bis geringe Symptome. Die ersten Symptome sind häufiger Durst und ein erhöhter Harndrang. Dieser entsteht durch den zu hohen Blutzuckerspiegel, der dazu führt, dass die Glukose in der Niere nicht vollständig resorbiert werden kann und dah...
- Möglichkeiten der Prävention Primärprävention: Primäre Präventionsmaßnahmen dienen dazu, das Neuauftreten von Krankheiten zu verhindern. Im Falle der Diabetesprävention sollte Normalgewicht mit einem BMI zwischen 18,5 und 25 kg/m2 angestrebt werden. Besonders schädlich wirkt sich ein erhöhter Bauchumfang aus. Geeignete...
- Ernährungsabhängige ErkrankungenErnährungsabhängige Erkrankungen sind Erkrankungen, die durch Mangel- oder Fehlernährung entstehen bzw. beeinflusst werden können. In Europa und Nordamerika ist die häufigste Form der Fehlernährung die Überernährung. Hierbei wird dem Körper mehr Energie zugeführt als verbraucht wird. Durc...
- Diabetes mellitus
- Grundlagen einer vollwertigen Ernährung
- Herz als Druck-Saugpumpe
- Lage und Aufbau des HerzensDie Zellen unseres Körpers sind auf eine permanente Zufuhr von Sauerstoff und Nährstoffen sowie einen permanenten Abtransport von Kohlendioxid und Abbauprodukten angewiesen. Für diese Zufuhr sowie den Abtransport ist es wesentlich, dass die Zellen in engem Kontakt mit Blutgefäßen, das Blut als ...
- Die Herzklappen und die Ventilebene Die vier Herzklappen dienen als Rückstoßventil und sorgen für einen geregelten Blutfluss. Sie verhindern, dass Blut während der Kontraktion zurück in die Vorhöfe bzw. in die Ventrikel fließt. Zwischen den Vorhöfen und den Hauptkammern liegen die sogenannten Segelklappen, auch Atrioventrik...
- Der Ventilebenenmechanismus Als Ventilebene bezeichnet man die Klappenebene des Herzens. Dies ist eine sehr feste Bindegewebsplatte innerhalb des Herzskeletts, in die alle vier Klappen eingebettet sind. Sie können sich je nach Kontraktionszustand des Herzens verschieben, da die Herzspitze (Apex cordis) am Zwerchfell befestig...
- Aufbau der Herzwand Die Herzwand ist von innen nach außen aus den folgenden drei Schichten aufgebaut (Abbildung): Endokard (Herzinnenhaut), Myokard (Herzmuskulatur), Epikard (Herzaußenhaut). Das Endokard (Herzinnenhaut) ist die innerste Schicht der Herzwand. Sie wird durch ein spezielles Epithel, das Endothel,...
- Die Herzkranzgefäße Die Herzkranzgefäße sind die Blutgefäße, die das Herz kranzartig umgeben und das Myokard mit Blut versorgen. Sie entspringen als Koronararterien (Aa. coronariae) aus der Aorta in Höhe der Aortenklappe und das rechte Herz durch die rechte Koronararterie (A. coronaria dextra) und das linke Herz ...
- Der Herzzyklus: Systole und DiastoleDas Herz eines erwachsenen Menschen schlägt im Durchschnitt 60- bis 80-mal pro Minute (Herzfrequenz) und wirft bei jedem Schlag etwa 70 mL Blut aus (Herzschlagvolumen). Bei einer Herzfrequenz von 80 Schlägen pro Minute macht das 5,6 L Blut pro Minute (Herzzeitvolumen). Damit das Blut gepumpt werde...
- Druck-Volumen-Diagramm Wie zuvor beschrieben, ist eine koordinierte Organisation der Druck- und Volumenverhältnisse der Ventrikel maßgeblich für den Ablauf von Blutfüllung und -austreibung. Aus dieser organisierten bzw. organisierten Beziehung lässt sich ein Druck-Volumen-Diagramm. Wiggers-Diagramm (benannt nach dem...
- Der Frank-Starling-MechanismusDer Frank-Starling-Mechanismus wurde unabhängig von den beiden Wissenschaftlern Otto Frank und Ernest Starling entdeckt und bestimmte die autonome Anpassung der Herztätigkeit bei erhöhtem Füllvolumen oder erhöhtem Aortendruck, ohne dass das autonome Nervensystem eingreift. Er ist ein moderner...
- Die Herztöne Während der normalen Herztätigkeit treten zwei Herztöne auf. Der erste Ton ist sehr dumpf und tief, wohingegen der zweite Ton recht hoch und laut ist. Wie kommen aber diese beiden Töne zustande? Der erste Herzton entsteht während der Anspannungsphase, auch im Druck-Volumen-Diagramm zwischen ...
- Erregungsbildungs- und Erregungsleitungssystem Der Impuls, der den Herzschlag und somit auch die Systole und Diastole anregt, kommt vom Herzen selbst und ist unabhängig vom Nervensystem. Dies sieht man auch schon im Labor, wo isolierte Herzmuskelzellen selbstständig und ohne Stimulation zucken. Im Herzen existieren spezialisierte Herzmuskel...
- Aktionspotenziale der HerzmuskulaturPrinzipiell gibt es im Herzen also zwei Arten von Herzmuskelzellen: die Schrittmacherzellen, die die Erregung bilden und weiterleiten, und die Herzmuskelzellen des Arbeitsmyokards, die für die Kontraktion des Herzens zuständig sind. Dabei erzeugen die Schrittmacherzellen über die Ausbildung eines...
- Aktionspotenzialbildung im ArbeitsmyokardPrinzipiell gibt es im Herzen also zwei Arten von Herzmuskelzellen: die Schrittmacherzellen, die die Erregung bilden und weiterleiten, und die Herzmuskelzellen des Arbeitsmyokards, die für die Kontraktion des Herzens zuständig sind. Dabei erzeugen die Schrittmacherzellen über die Ausbildung eines...
- Aktionspotenzialbildung in SchrittmacherzellenDie Aktionspotenzialbildung in den Schrittmacherzellen läuft im Wesentlichen wie beim Arbeitsmyokard ab. Auch hier beruht die Erregungsbildung auf wechselnde Ionenströme, die zeitlich koordiniert sind. Anders als beim Arbeitsmyokard, ist jedoch das Ruhepotenzial der Schrittmacherzellen sehr insta...
- Das Elektrokardiogramm (EKG)Durch die zeitliche Abfolge der Aktionspotenziale aller Herzmuskelzellen ändert sich die Oberflächenladung des Herzens in einem regelmäßigen Muster. Diese Ladungsänderungen dringen bis zur Körperoberfläche (bis zur Haut) durch und lassen sich über Elektroden ableiten. Diese Ableitung der Her...
- Regulation der HerztätigkeitWie schon beschrieben ist das Herz in der Lage, autonom (selbstständig) zu schlagen. Dabei pumpt es bei jedem Schlag eine definierte Menge Blut, die man als Herzschlagvolumen bezeichnet. Sie ist definiert als Differenz des enddiastolischen und des endsystolischen Volumens. In Ruhe schlägt das Herz...
- Das Herz in Not – HerzerkrankungenDie Weltgesundheitsorganisation WHO stellt jedes Jahr eine Statistik über die weltweit häufigsten Todesursachen auf. Dabei ergab die letzte Statistik, dass im Jahr 2019 Herzkrankheiten mit etwa 16 % die weltweit häufigste Todesursache war. Nimmt man noch die Blutgefäßkrankheiten (Bluthochdruck,...
- Koronare Herzkrankheit (KHK)Die Weltgesundheitsorganisation WHO stellt jedes Jahr eine Statistik über die weltweit häufigsten Todesursachen auf. Dabei ergab die letzte Statistik, dass im Jahr 2019 Herzkrankheiten mit etwa 16 % die weltweit häufigste Todesursache war. Nimmt man noch die Blutgefäßkrankheiten (Bluthochdruck,...
- HerzinfarktDer Herzinfarkt (Myokardinfarkt) ist in Deutschland eine der Haupttodesursachen, wobei jährlich ca. 300 Infarkte pro 100.000 Einwohner gezählt werden. Bei einem Herzinfarkt ist die Mangeldurchblutung des Herzmuskelgewebes so weit vorangeschritten, dass Teile des Gewebes absterben (Nekrose). Auch h...
- HerzinsuffizienzBei der Herzinsuffizienz (Herzschwäche) handelt es sich um eine Herzerkrankung, bei der das Herz nicht mehr so leistungsfähig wie ein gesundes Herz ist. Das erkrankte Herz ist dabei nicht mehr in der Lage den Körper ausreichend mit Blut und Sauerstoff zu versorgen, was sich auch bei den Patienten...
- Hormonsystem
- Aufgaben des HormonsystemsAnders als primitive Einzeller müssen im mehrzelligen Organismus die vielen spezialisierten Zellen, Gewebe und Organe sinnvoll integriert und koordiniert werden. So dienen dem Menschen besonders das Nerven- und das Hormonsystem als Integrationssysteme. Für die Pathogenabwehr (Abwehr von Krankheits...
- Bildungsorte der HormoneHormone können anhand verschiedener Eigenschaften wie beispielsweise ihrer chemischen Struktur, Funktion, aber auch gemäß ihres Bildungsortes eingeteilt werden. Die meisten Hormone im menschlichen Körper sind glanduläre Hormone (Glandula = Drüse), also Drüsenhormone. Sie werden von spezialisi...
- Einteilung und Funktion der HormoneHormone können anhand verschiedener Eigenschaften wie beispielsweise ihrer chemischen Struktur, Funktion, aber auch gemäß ihres Bildungsortes eingeteilt werden....
- Chemische Struktur der HormoneHormone können anhand verschiedener Eigenschaften wie beispielsweise ihrer chemischen Struktur, Funktion, aber auch gemäß ihres Bildungsortes eingeteilt werden. Gemäß ihrer chemischen Struktur und somit ihrer Biosynthese lassen sich Hormone insbesondere in die folgenden Gruppen einteilen: P...
- Transport von Hormonen im BlutWährend die hydrophilen Hormone (z. B. Peptidhormone) frei im wässrigen Blut vorliegen, sind die hydrophoben Hormone während des Transports im Blut an sogenannte Transportproteine (oder Carrier) gebunden. Dies gilt vor allem für die lipophilen Steroidhormone und die Hormone T3 und T4 der Schildd...
- Wirkungsmechanismen von Hormonen Die Spezifikation des Hormonsystems kommt nicht wie beim Nervensystem über definierte Zell-Kontakte-Zustände, sondern über spezifische Hormonrezeptoren, die von den jeweiligen Zielzellen gebildet werden. Je nachdem, ob das Hormon hydrophil oder lipophil ist, können die Rezeptoren an der Plasmam...
- Hemmungsarten von Hormonrezeptoren Ganz ähnlich wie manche Nervengifte (Nikotin, Koffein etc.), die postsynaptischen Rezeptoren über ihre Strukturähnlichkeit blockieren oder aktivieren, können auch Substanzen, wie körpereigene Faktoren, Gifte oder Medikamente, Hormonrezeptoren hemmen. Dies macht man sich auch in der Medizin z...
- Hierarchie der Hormone Die Bildung und Sekretion von Hormonen ist ein sehr komplexer und wichtiger Prozess. Daher unterliegt die Sekretion bestimmter Hormone einer strengen Hierarchie. Das ermöglicht das Verarbeiten zahlreicher Informationen sowie eine genaue Regulation der jeweiligen Hormonabgabe. Da sich die Hormone d...
- Kybernetische Regelkreise Wie wir zuvor gesehen haben, werden die endokrinen Drüsen und Gewebe durch eine starke Hierarchie gesteuert. Dabei können hormonelle Signale über die Hypothalamus-Hypophysen-Achse die Freisetzung peripherer Hormone steuern. Sensoren messen in den inneren Organen, aber auch in der Muskulatur, die...
- Die Hypothalamus-Hypophysen-Achse Wie bereits erwähnt, wird ein Großteil der peripheren Hormone durch die Hypothalamus-Hypophysen-Achse reguliert. Diese Achse bzw. diese beiden Areale des unteren Zwischenhirns bilden als übergeordnete Hormondrüsen eine funktionelle Einheit, die aufgrund ihrer anatomischen Lage häufig gemeinsam...
- Die Hormone der Hypothalamus-Hypophysen-Achse Zu den Releasing-Hormonen gehören das Thyreotropin-Releasing-Hormon (TRH), das die Ausschüttung des thyreoideastimulierenden Hormons (TSH) aus der Adenohypophyse stimuliert; das Corticotropin-Releasing-Hormon (CRH), das die Ausschüttung des adrenocorticotropen Hormons (ACTH) aus der Adenohypo...
- Hormonelle Einflüsse im Lebenszyklus
- Aufbau und Funktion der GeschlechtsorganeDie männlichen und weiblichen Geschlechtsorgane dienen der Fortpflanzung (Reproduktion) des Menschen. Sie entwickeln sich entsprechend der jeweiligen Geschlechtschromosomen (XX und XY) aus den zunächst embryonal zweigeschlechtlich angelegten Keimanlagen in die primären, sekundären und tertiären...
- Die männlichen GeschlechtsorganePrinzipiell unterscheidet man die inneren und äußeren Geschlechtsorgane. Zu den inneren Geschlechtsorganen des Mannes gehören die Hoden (Testis), Nebenhoden (Epididymis), Samenleiter (Ductus deferens), Vorsteherdrüse (Prostata), Samenbläschen (Vesiculae seminales) und die Cowper-Drüsen. Das Gl...
- Die SpermatogeneseAls Spermatogenese (griechisch: sperma = Samen und genesis = entstehen) bezeichnet man die Bildung befruchtungsfähiger Spermien aus den Vorläuferzellen in den Hodenkanälchen. Dieser Vorgang dauert beim Menschen etwa 64 Tage und beschreibt die „Wanderung“ der sich entwickelnden Keimzellen von ...
- Hormonelle Steuerung der männlichen GeschlechtsfunktionMit dem Eintreten der Pubertät schüttet der Hypothalamus Gonadotropin-Releasing-Hormon (GnRH) aus. Diese regen in der Adenohypophyse die Bildung und Ausschüttung des follikelstimulierenden Hormons (FSH) und des luteinisierenden Hormons (LH) an. Während FSH hauptsächlich die Spermienreifung übe...
- Die weiblichen GeschlechtsorganeWie auch beim Mann, unterscheidet man bei der Frau zwischen den inneren und äußeren Geschlechtsorganen.Während die äußeren Geschlechtsorgane durch die kleinen und großen Schamlippen (Labia minora und Labia majora), den Kitzler (Klitoris) und den Scheidenvorhof (Vestibulum vaginae) gebildet wer...
- Die Eierstöcke und Eileiter Die paarig angelegten Eierstöcke liegen jeweils seitlich im Becken der Frau (Abbildung). Sie produzieren jeden Monat eine befruchtungsfähige Eizelle ( Oozyte ) und bilden die weiblichen Sexualhormone der Gruppe der Östrogene (Östradiol, Östron, Östriol) und das Progesteron . Die erste v...
- Der Uterus Die Gebärmutter (Uterus) ist ein birnenförmiges Organ, das mit einer Schleimhaut, dem Endometrium ausgekleidet ist (Abb. "Innere Geschlechtsorgane der Frau"). Sie besteht im Deklarierten aus dem Gebärmutterkörper (Corpus uteri), der über den Gebärmutterhals (Zervix) und dessen unterer Öffnu...
- Die Oogenese Als Oogenese (auch Ovogenese) bezeichnet man die Bildung einer befruchtungsfähigen Eizelle (Oozyte) aus den Keimbahnzellen der Frau. Dieser Prozess ist sehr empfindlich und läuft in mehreren Phasen ab. Die Oogenese beginnt mit den Oogonien, die mitotisch aus den Urkeimzellen hervorgehen. Einige O...
- Hormonelle Steuerung der weiblichen Geschlechtsfunktion Die Pubertät der Frau setzt etwa mit dem 13. Lebensjahr, mit der vermehrten Sekretion des GnRH aus dem Hyperthalamus, ein. GnRH regt seinerseits die Adenohypophyse zur Bildung des follikelstimulierenden Hormons und des luteinisierenden Hormons an. Beides sind Sexualhormone, die während de...
- Der Menstruationszyklus Mit knapp 36 Jahren haben Frauen eine lange Reproduktionsdauer. Sie beginnt zwischen 8 und 13 Lebensjahren mit der ersten Regelblutung (Menarche) und endet mit etwa 50 Lebensjahren mit der Menopause, der mindestens ein Jahr ohne ovarielle Regelblutung folgt. Anschließend beginnt die Postmenopause....
- Hormonelle und nicht-hormonelle KontrazeptivaAls Kontrazeptiva bezeichnet man Methoden, die der Empfängnisverhütung, also der Verhinderung einer ungewollten Schwangerschaft, dienen. Dabei können Paare auf verschiedenste Möglichkeiten zurückgreifen. Es sei allerdings gesagt, dass das ideale Verhütungsmittel nicht existiert. Die Wahl kann ...
- Hormonelle Kontrazeptiva Die Grundidee der hormonellen Kontrazeption basiert darauf, über künstliche Geschlechtshormone einen Eisprung zu verhindern. Man bezeichnet sie daher auch als Ovulationshemmer. Häufig enthalten die jeweiligen Präparate künstliche Formen des Östrogens Östradiol (z. B. Ethinylestradiol) und Ge...
- Die Anti-Baby-Pille Die wohl bekannteste hormonelle Verhütungsmethode ist die Pille (auch oraler Ovulationshemmer genannt). Diese wurde bereits in den 1960er Jahren in den USA entwickelt und war gesellschaftlich und politisch zunächst wenig akzeptiert. Noch bis Ende der 1960er Jahre wurde sie in der Bundesrepublik D...
- Die HormonspiraleDie Hormonspirale, auch intrauterines Implantat oder Intrauterinsystem (IUS), ist ein T-förmiges Kunststoffimplantat, das durch den Frauenarzt in die Gebärmutter eingelegt wird. Sie gibt kontinuierlich niedrigdosiertes Gestagen ab und setzt, wie die Minipille auch, auf die lokale Gestagen-Wirkung....
- Die DreimonatsspritzeWer etwaigen Anwendungsfehler entgegenwirken will oder andere Verhütungsmethoden nicht verträgt, kann auf die Dreimonatsspritze zurückgreifen. Hierbei wird durch den Frauenarzt alle drei Monate Gestagen in den großen Gesäßmuskel oder in den Oberarm injiziert. Auch hierbei wird die Wirkung nich...
- Nicht-hormonelle (mechanische) Kontrazeptiva Für die meisten Frauen ist die Pille das Verhütungsmittel der Wahl. Allerdings verträgt nicht jede Frau die Hormonpräparate gleich gut. Als Alternative dienen nicht-hormonelle Methoden, die eine Befruchtung entweder mechanisch oder chemisch verhindern. Im Folgenden werden diverse nicht-hormonel...
- Kreislauf und Blutdruckregulation
- Anatomie der BlutgefäßeDie Blutgefäße beider Teilkreisläufe lassen sich funktionell (gemäß der Gefäßfunktion) und morphologisch (gemäß ihres „Aussehens“) in unterschiedliche Gefäßabschnitte unterteilen (Abbildung). Jeder Teilkreislauf beginnt mit den Arterien, die Blut vom Herzen weg transportieren. Diese t...
- Aufbau von Arterien und VenenDie Gefäßwand von Arterien und Venen ist im Wesentlichen recht ähnlich aufgebaut und besteht aus drei Wandschichten, deren Art und Beschaffenheit je nach Funktion variieren kann (Abbildung): Tunica interna: Die innerste Schicht bildet die Tunica interna. Sie besteht aus einer speziellen Epithels...
- Arterien und das HochdrucksystemArterien (auch Schlagadern) sind der Teil des Blutgefäßsystems, der stets Blut vom Herzen wegtransportiert. Dabei benennt man die Arterien meist gemäß der Region, die sie versorgen. Beispielsweise versorgt die Arteria femoralis (A. femoralis) den Oberschenkel (Femur) mit Blut. Die größte Arter...
- Venen und das NiederdrucksystemVenen sind der Teil des Blutgefäßsystems, der das Blut zum Herzen zurücktransportiert. Dabei sammeln kleinere Venolen zunächst das Blut, das durch die Kapillaren fließt, und vereinigen sich zu immer größer werdenden Venen. Die größte Vene ist die Hohlvene, die als obere Hohlvene (V. cava su...
- Venen und das NiederdrucksystemVenen sind der Teil des Blutgefäßsystems, der das Blut zum Herzen zurücktransportiert. Dabei sammeln kleinere Venolen zunächst das Blut, das durch die Kapillaren fließt, und vereinigen sich zu immer größer werdenden Venen. Die größte Vene ist die Hohlvene, die als obere Hohlvene (V. cava su...
- KrampfadernDie Aufgabe der Venen ist es, das Blut aus den Organen zu sammeln und zum Herzen zu transportieren. Staut sich jedoch das Blut vor allem in den Beinvenen, steigt die Wandspannung der Venenwand. Dies kann auf Dauer zur Weitung der Venen führen. Dadurch kann es zu einem Entfernen der Ränder der Vene...
- Die Kapillargefäße Das arterielle und das venöse Blutgefäßsystem sind über kleine Haargefäße, sogenannte Kapillaren, miteinander verbunden. Sie bilden den eigentlichen Ort, in dem der Stoffaustausch stattfindet. Ihre Gefäßwand ist nicht aus drei Schichten aufgebaut, sondern besteht im Wesentlichen aus der Tuni...
- StoffaustauschDer Stoffaustausch erfolgt über die Gefäßwand der Kapillare und hängt von zwei Parametern ab: dem effektiven Filtrationsdruck und dem kolloidosmotischen Druck. Was heißt das aber? Fließt das Blut von der Aorta über die Arterien bis in die stark verzweigten Arteriolen, nimmt der Blutdruck kon...
- Die LymphgefäßeLymphgefäße sind in ihrem Aufbau den Blutgefäßen sehr ähnlich. Sie transportieren allerdings kein Blut, sondern sammeln das überschüssige Gewebswasser, das von den Kapillaren nicht aufgenommen wurde. Diese Flüssigkeit, die man als Lymphe bezeichnet, wird dann im Anschluss dem venösen System...
- Der PfortaderkreislaufDer Pfortaderkreislauf ist ein venöser Blutkreislauf und Teil des Körperkreislaufes. In ihm wird Blut aus Magen, Darm, Milz und der Bauchspeicheldrüse über eine Pfortader, Vena portae, zunächst zur Leber und weiter zur unteren Hohlvene geleitet. Der Zweck des Pfortaderkreislaufes ist es, Nä...
- Der fetale KreislaufDer Blutkreislauf eines ungeborenen Kindes (Fetus) unterscheidet sich maßgeblich vom erwachsenen Blutkreislauf. Da der Fetus im Mutterleib nicht atmen kann, sind die Lungen noch nicht entfaltet und können den kleinen Körper des Fetus noch nicht mit Sauerstoff versorgen. Gleiches gilt für das Pfo...
- Der postnatale KreislaufMit dem ersten Schrei entfalten sich die Lungen direkt nach der Geburt (postnatal). Der Widerstand in den Lungenarterien sinkt stark und das Blut aus dem rechten Ventrikel gelangt vollständig in den Lungenkreislauf. Danach gelangt das sauerstoffreiche Blut in den linken Vorhof, dessen Druck nun hö...
- Hämodynamik und BlutdruckregulationDie Gewebe des Körpers bedürfen zu jeder Tageszeit und in jeder Lage einer permanenten Versorgung mit Sauerstoff und Nährstoffen. Dies wird durch einen kontinuierlichen Blutfluss bewerkstelligt, der mit einem bestimmten Druck und mit einer bestimmten Fließgeschwindigkeit durch die Blutgefäße s...
- Kurzfristige BlutdruckregulationDer Blutdruck ist ein relativ empfindliches System und kann schon durch kleine Veränderungen gestört werden. Dies ist z. B. der Fall, wenn man kurzfristig schnell läuft bzw. rennt oder aus dem Bett aufsteht (Orthostasereaktion). Steht man von dem Bett oder dem Sofa auf, versackt schlagartig Blut ...
- Mittelfristige BlutdruckregulationReicht die kurzfristige Blutdruckregulation nicht mehr aus, setzt nach wenigen Minuten bis Stunden die mittelfristige Blutdruckregulation ein. Diese Regulation erfolgt hauptsächlich über die des Gefäßwiderstandes. Fällt der Blutdruck langfristiger ab, sinkt auch die Durchblutung der Glomeruli i...
- Krankhaft veränderter Blutdruck: BluthochdruckDer Blutdruck untersteht einer permanenten Kontrolle und wird ständig an die sich ändernden Situationen angepasst. Daher sind temporäre und größere Abweichungen (z. B. Sport) vom Idealblutdruck von 120/80 mmHg durchaus üblich. Ist der Blutdruck allerdings permanent zu hoch oder zu niedrig, kö...
- Krankhaft veränderter Blutdruck: BlutniederdruckIm Gegensatz zum Bluthochdruck, ist beim Blutniederdruck (Hypotonie) der Blutdruck zu gering. Dies ist der Fall, wenn der Druck unter 100/60 mmHg fällt. Allerdings sind die Grenzen zum normalen Blutdruck fließend und es gibt keine klar definierte Grenze wie bei der Hypertonie. Interessanterweise g...
- Neurologie
- Die Nervenzelle
- Aufbau des NervensystemsDas Nervensystem dient der Wahrnehmung, Verarbeitung und Weiterleitung von Informationen im menschlichen Körper. Zu diesem Zweck haben sich verschiedene Zellarten entwickelt: Nervenzellen (Neuronen) dienen der Informationsübertragung und Stützzellen (Gliazellen) der Versorgung der Neuronen. Grund...
- Zelltypen des NervensystemsDas Nervensystem bzw. das Nervengewebe besteht im Wesentlichen aus zwei Zelltypen: den Neuronen, die Informationen aufnehmen, verarbeiten und weiterleiten und den Gliazellen, die unterstützende Aufgaben im Nervengewebe übernehmen....
- Aufbau der NervenzelleDas Neuron (Abbildung) besitzt zwei verschiede Arten von Fortsätzen, die der Interaktion mit anderen Neuronen dienen. Einer dieser Fortsätze ist der Dendrit. An ihm werden Reize von anderen Neuronen aufgenommen und zum Zellkörper, dem Soma (auch als Perikaryon bekannt), weitergeleitet. Im Soma b...
- Das AxonDas Axon ist ein langer zylinderartiger Zellausläufer eines Neurons. Der Name rührt von dem griechischen Wort für Achse (ho axōn) und wird auch als Neuraxon bezeichnet. Das Axon ist die zentrale Bahn, auf der die Reizleitung von einem auf das nächste Neuron abläuft. Die elektrischen Impulse (A...
- Exkurs: Schädigung der MyelinscheideIm Rahmen verschiedener Erkrankungen kann es zu Schädigungen der Myelinscheide kommen. Ein Beispiel ist das Guillain-Barré-Syndrom. Hierbei kommt es unter anderem nach einer Infektion mit bestimmten Bakterien oder Viren zu einer Bildung von Antikörpern, die auch gegen Myelin oder Membranbestandte...
- Das Ruhepotenzial der NervenzelleAls Ruhepotenzial (RP, VRP) oder Ruhemembranpotenzial bezeichnet man in der Physiologie den Spannungsunterschied zwischen der Außen- und Innenseite der Zellmembran von erregbaren Zellen (Neuronen oder Muskelzellen) in Ruhe. Vereinbarungsgemäß wird dabei das Potenzial des Extrazellularraums als Nu...
- Das Aktionspotenzial der NervenzelleEine kurzfristige Abweichung vom RP stellt das sogenannte Aktionspotenzial (AP) dar, also der elektrische Impuls, der über das Axon weitergeleitet wird. Es ist die Frequenz der APs, die letzten Endes die zu überbringende Information kodiert. Dies bedeutet, dass APs nicht einfach stumpf durch das A...
- Die Synapse
- Interzelluläre Signalübertragung: die SynapseIn den vorangegangenen Abschnitten haben wir gesehen, wie Neuronen Aktionspotenziale aufbauen und diese entlang des Axons leiten. Damit aber nun Signale über eine längere Distanz geführt werden können, müssen die Signale von einer auf die nächste Nervenzelle übertragen werden. Um dies zu tun,...
- Exzitatorische und inhibitorische postsynaptische PotenzialeDurch das Binden von Neurotransmittern an (postsynaptische) Rezeptoren, werden Ionenströme ausgelöst, die das Potenzial der postsynaptischen Membran verschieben. Wie zuvor beschrieben, bezeichnet man diese Potenzialänderung als postsynaptisches Potenzial (PSP). Je nach Synapsentyp können jedoch ...
- Einteilung von NeurotransmitternÜblicherweise werden auch die Transmitter je nach ihrer Wirkung in exzitatorische (Glutamat, ACh, Noradrenalin etc.) und inhibitorische Neurotransmitter (γ-Aminobuttersäure) eingeteilt. Allerdings gibt es auch Neurotransmitter, die sowohl exzitatorisch als auch inhibitorisch wirken können. Beisp...
- Beeinflussung der Synapse durch Medikamente, Gifte und Drogen Eine Vielzahl von Medikamenten, Drogen und Giften entfalten ihre Wirkung an Synapsen. Dazu binden sie meist an Rezeptoren der Prä- oder Postsynapse oder hemmen wichtige Enzyme und führen somit zu einer Veränderung der Abläufe an der Synapse. Da Neuronen komplex miteinander verschaltet sind, füh...
- Die SuchtAls Sucht bezeichnet man in der Medizin einen krankhaften Zustand der Abhängigkeit von einer Droge, einem Genussmittel oder einem Verhalten. Die süchtige Person leidet dabei unter dem ständigen Zwang, sich das Suchtmittel oder das süchtige Verhalten in steigender Dosis zuführen zu müssen. Auch...
- Das zentrale Nervensystem
- Das zentrale NervensystemDas zentrale Nervensystem (ZNS) umfasst das Gehirn und das Rückenmark. Es steuert und reguliert über das periphere Nervensyste m (PNS) und vegetative Nervensystem die Funktion der Organe und ermöglicht einen koordinierten Bewegungsablauf der Skelettmuskulatur....
- Der Cortex und seine RindenfelderDie Großhirnrinde (Cortex) enthält mit Abstand den Großteil der Neuronen im Gehirn. Diese können funktionell in sogenannten Rindenfeldern zusammengefasst werden (Abb. 1A). Man unterscheidet die motorischen Rindenfelder, die die Skelettmuskulatur versorgen, die sensorischen Rindenfelder, die Sinn...
- Anatomie und Funktion der inneren HirnstrukturenBislang haben wir uns fast ausschließlich mit der äußeren Anatomie und Funktion des Großhirns befasst. Das Großhirn ist allerdings nur eines von sechs Teilen des Gehirns. Grob wird das Gehirn in das Großhirn (Abb.4.22: 1), Zwischenhirn (Abb.: 4–7), Mittelhirn (Abb.: 8), die Brücke (Abb.: 9)...
- ReflexeReflexe sind unwillkürliche Reaktionen des Nervensystems auf bestimmte Reize, die wir willentlich nicht beeinflussen können. Das grundsätzliche Reflexschema sieht dabei immer gleich aus: Ein Reiz wird von Rezeptoren auf Sinneszellen aufgenommen (Reizaufnahme). Die Sinneszelle wandelt den Reiz in...
- Exkurs: Der SchlaganfallEin Schlaganfall (Apoplexie oder apoplektischer Insult) ist eine schlagartig auftretende Erkrankung des Gehirns, bei der es zu einer kompletten oder teilweisen Nährstoffunterversorgung eines Teils des Gehirns kommt. Grund dafür ist meist eine kardiovaskuläre Grunderkrankung, wie Arteriosklerose, ...
- Exkurs: Das periphere NervensystemDas periphere Nervensystem (PNS) umfasst alle Bereiche, die nicht dem zentralen Nervensystem (ZNS) zugeschrieben werden. Obwohl eine funktionelle Abgrenzung beider Systeme nicht sinnvoll ist, zählt man zu dem PNS die Spinalnerven, die die entsprechenden Körperregionen versorgen, alle Rezeptoren, d...
- Die Nervenzelle
- Niere – ein vielseitiges Organ
- Das AusscheidungssystemÜber den Tag hinweg produziert unser Organismus diverse Stoffwechselprodukte, die entweder für den Körper nützlich (Glykogen, Hormone etc.) oder schädlich sind (giftige Abbauprodukte). So werden beispielsweise beim Proteinabbau Aminogruppen (NH2) frei, die entweder für den Aufbau neuer Protein...
- Die Anatomie des AusscheidungssystemsDas Ausscheidungssystem des Menschen besteht im Wesentlichen aus den paarigen Nieren und den ableitenden Harnwegen (Harnleiter, Harnblase und Harnröhre) (Abb.). Die bohnenförmigen Nieren (lateinisch Ren; altgriechisch νεφρός Nephrós) erfüllen verschiedene Aufgaben und sind das Zentrum des ...
- Die Anatomie der NiereDie Niere erfüllt eine Reihe verschiedener Funktionen und weist eine entsprechend komplexe Anatomie auf. Diese mag auf den ersten Blick recht kompliziert wirken, wird jedoch nach genauerer Beschreibung der ablaufenden Vorgänge verständlicher. Die paarigen Nieren (Ren bzw. Nephros) sind etwa 150 g...
- Anatomie des NephronsDie funktionelle Einheit der Niere bildet das Nephron, von dem etwa 1 bis 1,5 Millionen pro Niere anzutreffen sind. Man unterscheidet zwei Typen von Nephronen: die in der Rinde liegenden corticalen Nephrone und die juxtamedullären Nephrone, die von der Rinde bis tief ins Mark ziehen. Das Nephron be...
- Aufgaben des NephronsWie eingangs beschrieben ist das Ausscheidungssystem der zentrale Regulator für den Elektrolyt- und Wasserhaushalt. Beide Haushalte sind für den Körper absolut lebensnotwendig. Während Elektrolyte an wichtigen Zellprozessen wie der Aufrechterhaltung des Ruhepotenzials, der Bildung des Aktionspot...
- Die glomeruläre Filtration: Bildung des PrimärharnsDer Primärharn wird im Nierenkörperchen gebildet. Dabei wird das Blut, das durch den Glomerulus fließt, gefiltert und das Filtrat (der Primärharn) in der Bowman-Kapsel aufgefangen. Die Filtration beruht dabei auf der Druckdifferenz zwischen dem Blutdruck und dem hydrostatischen Druck der Bowman-...
- Abläufe im Tubulussystem: Bildung des SekundärharnsWürde der Primärharn einfach ungehindert ausgeschieden werden, würde der Körper jede Menge Wasser, aber auch viele nützliche Substanzen wie Glukose, Salze oder Puffer (Karbonate) verlieren. Man müsste permanent trinken und essen, um diesen Verlust wieder auszugleichen. Damit dies nicht passier...
- Abläufe im proximalen TubulusDer proximale Tubulus ist der erste Abschnitt der Harnkonzentrierung. Hier findet eine Massenresorption von Wasser, Salzen und Subtraten statt. Tatsächlich werden hier pro Tag fast 100 L Wasser und fast 1 kg Kochsalz resorbiert. Charakteristisch für den proximalen Tubulus sind die Na+-gekoppelten ...
- Die Henle-Schleife und das GegenstromprinzipDa im proximalen Tubulus rund Dreiviertel des Primärharns resorbiert werden, erreicht lediglich ein Viertel den absteigenden Ast der Henle-Schleife. Der hier ankommende Harn hat wegen der isoosmotischen Transporter im proximalen Tubulus, genauso wie der Primärharn im Nierenkörperchen auch, eine O...
- Abläufe im distalen TubulusNach der Passage durch die Henle-Schleife wurden bereits etwa 90 % des Primärharns resorbiert, sodass im distalen Tubulus nun die Feinjustierung erfolgt. Über Natrium-Kalium-Pumpen werden weiter Na+-Ionen aus dem Tubulussystem resorbiert. Dieser Vorgang kann hormonell über Aldosteron und Kortisol...
- Das SammelrohrDas Sammelrohr schließt sich dem distalen Tubulus an und zieht parallel zur Henle-Schleife bis zum Nierenbecken, in dem der Sekundärharn (Endharn) gesammelt wird. Das Sammelrohr ist aber nicht einfach nur eine bloße Leitung für den Sekundärharn, sondern dient auch der finalen Aufkonzentrierung ...
- Der juxtaglomeruläre Apparat und die Autoregulation der NiereFür eine normale Nierenfunktion bedarf es einer Balance zwischen der glomerulären Filtration im Nierenkörperchen und der Resorption bzw. Sekretion im Tubulussystem. Dies geschieht über einen Rückkopplungsmechanismus, bei dem dem Glomerulus die aktuelle Tubulusfunktion übermittelt wird. Hierfü...
- Exkurs: ACE und Covid19Das ACE besitzt eine zweite Isoform, das ACE2, das ebenfalls am RAAS beteiligt ist. ACE2 ist der Gegenspieler zum ACE und zersetzt Angiotensin I und II in kleine Fragmente. Diese wirken nicht gefäßverengend, sondern gefäßerweiternd und senken so den Blutdruck. ACE2 ist aber nicht nur ein Enzym, ...
- Die ableitenden HarnwegeAb dem Nierenkelch, wenn der Harn aus dem Nephron ins Nierenbecken fließt, beginnen die ableitenden Harnwege. Das Nierenbecken verengt sich nach unten hin und mündet in die Harnleiter, die etwa 30 cm lang sind und ebenfalls retroperitoneal liegen. Diese münden schließlich in die Harnblase (Vesic...
- Säure-Basen-RegulationZur Regulation des pH-Wertes des Blutes und des Interstitiums stehen dem Körper unterschiedliche Systeme zur Verfügung: Eines dieser Systeme ist das Bicarbonatpuffersystem. Hierbei stehen die Lungen und die Nieren in engem Zusammenhang, indem sie entweder CO2 abatmen oder Protonen sezernieren bzw....
- Stickstoffhaltige AbfallprodukteAmmoniak (NH3) enthält nur ein Stickstoffatom und ist sehr gut wasserlöslich, aber auch toxisch. Es wird zunächst in die Tubuli (das „Kanalsystem“) der Niere ausgeschieden, wo es zum ebenfalls giftigen Ammoniumion (NH4+) protoniert wird. Durch die Protonierung wird das Ammoniak nicht mehr mem...
- Endokrine Funktion der NiereDie Nieren sind auch endokrin aktiv und sind sowohl ein Bildungsort, als auch ein Wirkungsort für Hormone (Abb.). Die Nieren können folgende Hormone bilden:Renin: Wie bereits beschrieben, kann im juxtaglomerulären Apparat der Niere Renin gebildet werden, wenn der Blutdruck bzw. die glomeruläre D...
- NierendiagnostikAm Anfang einer jeden Diagnostik steht die Anamnese. Hier wird im Aufklärungsgespräch der Patient befragt, wie seine oder ihre Krankengeschichte aussieht und ob und welche Beschwerden vorliegen. Schmerzen beim Wasserlassen, eine Verfärbung des Urins oder Flankenschmerzen können auf eine Erkranku...
- ÖdemeIst die Nierenfunktion verringert, wird auch weniger Wasser ausgeschieden. Das Wasser verschwindet allerdings nicht einfach, sondern sammelt sich stattdessen im Gewebe an (Ödem). Da das Wasser der Schwerkraft folgt, bilden sich solche Ödeme besonders gerne in den Beinen. Neben der Niereninsuffizie...
- BluthochdruckWie bereits beschrieben, sind die Nieren ein zentrales Steuerorgan für die Blutdruckregulation. Erkrankungen, die die Nierendurchblutung vermindern (z. B. Verengung der Nierenarterie, Entzündung des Glomerulus im Zuge einer Glomerulonephritis), führen zur Aktivierung des RAAS und so zur Blutdruck...
- DiabetesDie Niere kann auch an verschiedenen Diabeteserkrankungen beteiligt sein. Dies kann sich dann in einer vermehrten Urinausscheidung (Polyurie) bemerkbar machen....
- HarninkontinenzBei einer Harninkontinenz (Blasenschwäche) kommt es unwillkürlich zum Harnverlust. Sie tritt auf, wenn die nervale Kontrolle über die Harnblase und deren Schließmuskeln gar nicht oder nur noch eingeschränkt funktioniert. Die Ursachen und Formen können vielfältig sein.Eine der häufigsten Form...
- NierensteineNierensteine (Nephrolithiasis) sind kleine Kristalle (Konkremente), die aus verschiedenen Urinbestandteilen entstehen können (Kalzium, Harnsäure, Magnesium, Ammonium, Phosphat etc.). Sie bilden sich bevorzugt an den drei Engstellen innerhalb der Harnleiter (Austrittsstelle am Nierenbecken, Kreuzun...
- NiereninsuffizienzUnter einer Niereninsuffizienz (Nierenschwäche) versteht man eine eingeschränkte Nierenfunktion. Man unterscheidet dabei die akute von der chronische Niereninsuffizienz.Von einer akuten Niereninsuffizienz spricht man, wenn die GFR plötzlich abfällt und das kritische Harnvolumen unter 0,5 L pro T...
- Therapie der Niereninsuffizienz und DialyseGrundsätzlich sieht die Therapie der Niereninsuffizienz vor, die Ursachen zu behandeln. Dabei sind die Behandlungsmöglichkeiten ebenso divers wie die Ursachen selbst. Sind Nierensteine die Ursache, die eine Harnstauung bedingen, werden diese zunächst entfernt. Bakterielle Entzündungen werden mit...
- NierentransplantationBei vollständigem Nierenversagen und Dialysepflicht besteht die Möglichkeit einer Nierentransplantation. Hierbei wird die Niere einer lebenden (Lebendspende) oder verstorbenen Person (postmortale Spende) dem Empfänger implantiert. Dies ist in Deutschland eine etablierte Methode, bei der die Spend...
- Immunsystem
- Grundlagen für die Arbeit des Immunsystems
- Grundlagen für die Arbeit des ImmunsystemsIm menschlichen Körper müssen die vielen spezialisierten Zellen, Gewebe und Organe sinnvoll integriert und koordiniert werden. So stehen dem Körper besonders das Nerven- und das Hormonsystem als Integrationssysteme zur Verfügung. Für die Pathogenabwehr (Abwehr von Krankheitserregern) und die Au...
- Das BlutSchon Goethe wusste, dass „Blut ein ganz besonderer Saft“ ist. Damit hatte er tatsächlich auch nicht ganz unrecht, denn Blut ist nicht nur ein zentraler Pfeiler der (langen veralteten) Humoralmedizin, sondern erfüllt auch im modernen medizinischen Verständnis wichtige Aufgaben. Zu den lebensw...
- Das BlutplasmaAls Blutplasma bezeichnet man den flüssigen Bestandteil des Blutes, der rund 50-55 % des Blutvolumens ausmacht. Das Plasma ist klar gelblich und besteht zum Großteil aus Wasser (ca. 90 %). Den Rest machen Proteine (ca. 7 %), Elektrolyte (ca. 1 %) und gelöste Substanzen wie Nährstoffe oder Stoffw...
- Exkurs: Elektrolytstörung und ElektrophoreseDie im Ionogramm dargestellte Elektrolytverteilung ist essenziell für die Funktion vieler Organe wie das Herz, die Nieren oder das Nervensystem. Eine Störung des Gleichgewichts kann zu vielfältigen Störungen in diesen Organen führen und weitreichende Folgen haben. Im Folgenden werden einige Ele...
- Der Hämatokrit und die BlutzellenAls Hämatokrit bezeichnet man den Anteil aller festen Bestandteile im Blut. Dies sind die Blutzellen, zu denen die Erythrozyten (roten Blutkörperchen), Leukozyten (weißen Blutkörperchen) und die Blutplättchen (Thrombozyten) gehören. Der Hämatokrit ist ein wichtiger Laborwert und liegt im Norm...
- Erythrozyten – die roten BlutkörperchenDie Erythrozyten (rote Blutkörperchen) stellen die größte Zellpopulation im Blut dar. Bei einer gesunden Frau befinden sich in einem Mikroliter Blut rund 4,8 Millionen Erythrozyten, während es beim gesunden Mann rund 5,4 Millionen sind. Erythrozyten sind kleine (7,8 µm Durchmesser) scheibenför...
- Exkurs: Kohlenstoffmonoxidvergiftung Kohlenstoffmonoxid ist ein farb- und geruchloses Gas, das bei Verbrennungen ohne ausreichende Sauerstoffzufuhr entsteht. Das Gas gelangt ähnlich wie Sauerstoff über die Lunge in das Blut, besetzt am Hämoglobin die Bindungsstelle des Sauerstoffes und verhindert somit dessen Bindung. Da Kohlenstoff...
- Erythropoese – Bildung der roten BlutkörperchenDie Bildung der Erythrozyten (Erythropoese) erfolgt im roten Knochenmark. Dabei wird ihre Synthese durch das Hormon Erythropoetin angestoßen, das bei Sauerstoffmangel vermehrt durch die Nieren, aber auch von der Leber gebildet wird. Es aktiviert pluripotente Stammzellen im roten Knochenmark, die si...
- Exkurs: Antigene und Antikörper Als Antigene (griechisch: anti = gegen; gennao = erzeugen) werden alle Strukturen bezeichnet, die von dem Immunsystem als fremd erkannt und gegen die Antikörper gebildet werden. Diese Antigene kommen auf der Oberfläche von Bakterien, Pilzen und Viren, aber auch auf Zellen anderer Menschen sowie Ti...
- Die Blutgruppen und das AB0-SystemAls Antigene (griechisch: anti = gegen; gennao = erzeugen) werden alle Strukturen bezeichnet, die von dem Immunsystem als fremd erkannt und gegen die Antikörper gebildet werden. Diese Antigene kommen auf der Oberfläche von Bakterien, Pilzen und Viren, aber auch auf Zellen anderer Menschen sowie Ti...
- Die Blutgruppen und der Rhesus- Faktor Neben dem AB0-System gibt es noch weitere Blutgruppensysteme, bei denen Antikörper gegen Oberflächenantigene gebildet werden. Zu diesen gehören unter anderem das Kell-System und das Rhesus-System. Das Rhesus-System (Rh) wurde bei Studien an Rhesusaffen entdeckt und ist klinisch bedeutsamer als...
- Leukozyten – die weißen BlutkörperchenAls Leukozyten (griechisch: leukos = weiß; kýtos = Zelle) bezeichnet man die weißen Blutkörperchen, also alle Blutzellen, die noch ihren Zellkern und Organellen besitzen und der Immunabwehr dienen. Sie sind mit einem Durchmesser von bis zu 20 µm größer als Erythrozyten und werden ebenfalls ü...
- Unterteilung der LeukozytenGranulozyten machen 45 – 75 % aller Leukozyten im Blut aus. Sie gehören zur angeborenen unspezifischen Abwehr und bilden die erste „Verteidigungsfront“. Ihr Zytoplasma ist vollgepackt mit kleinen Körnchen, sogenannten Granula, wodurch sie auch ihren Namen tragen. Sie sind an der Abwehr von B...
- Thrombozyten – die Blutplättchen Thrombozyten sind mit einem Durchmesser von etwa 3µm die kleinsten Blutkörperchen. Sie werden im roten Knochenmark aus Megakaryozyten (auch Knochenmarksriesenzellen) gebildet (Thrombopoese) und sind im Endeffekt „Zelltrümmer“, die aus diesen Vorläuferzellen abgeteilt werden. Thrombozyten sin...
- Blutstillung und Blutgerinnung Die Blutstillung und Blutgerinnung ist für das Abitur 2021/2022 kein abiturrelevantes Thema, wird an dieser Stelle jedoch aufgrund seiner Relevanz für viele Krankheitsbilder behandelt. Beim Lernen kann es für das Krankheitsverständnis helfen. Auswendiglernen ist hier jedoch höchstwahrscheinlich...
- FibrinolyseWurde der endgültige Thrombus gebildet, zieht sich das Fibrinnetz zusammen und nähert so die Wundränder an; die Wunde schließt sich allmählich. Fibroblasten (Bindegewebszellen) wachsen nun in das dichte Fibrinnetz ein, bauen den Thrombus um und verschließen die Wunde endgültig. Nach der Heilu...
- Exkurs: Thrombolyse Medikamentös kann die Fibrinolyse ebenfalls aktiviert werden, indem man Streptokinase oder rekombinantes tPA (r-tPA) verabreicht. Diese Medikamente dienen der Thrombolyse (kurz: Lyse), also dem Auflösen von Thromben, und werden bei bedrohlichen Gefäßverschlüssen (Herzinfarkt, Schlaganfall etc.)...
- Thrombosen und EmbolienZur Ausbildung eines Thrombus kann es jedoch auch unabhängig von der Wundheilung kommen. Dabei kommt es spontan und meist ohne Verletzung innerhalb eines Gefäßes zu einer Blutgerinnung, die zur Bildung eines Blutgerinnsels führt. Dieses kann zum lokalen Verschluss des Blutgefäßes führen und d...
- Die Blutbildung – Hämatopoese Der Verbrauch an Blutzellen ist wirklich enorm! Daher müssen jede Sekunde etwa 2 Millionen Blutzellen neugebildet werden. Dies geschieht während der sogenannten Hämatopoese, also der Blutzellbildung bzw. Blutbildung. Alle Blutzellen entstehen im roten Knochenmark und gehen auf gemeinsame pluripo...
- Das lymphatische System und die lymphatischen OrganeDas lymphatische System dient der Immunabwehr und setzt sich aus den lymphatischen Organen und dem Lymphgefäßsystem zusammen. ...
- Primäre lymphatische OrganeAls primäre lymphatische Organe bezeichnet man die Organe, die direkt an der Bildung und Reifung von Immunzellen beteiligt sind. Ziel ist die Bildung reifer Lymphozyten, die in der Lage sind, Antigene zu erkennen und eine Immunantwort einzuleiten. Die primären lymphatischen Organe nehmen eine übe...
- Sekundäre lymphatische OrganeAls sekundäre lymphatische Organe bezeichnet man diejenigen Organe und Gewebe, in denen reife B- und T-Lymphozyten nach Antigenen (also nach immunwirksamen Strukturen) suchen, nachdem sie das Knochenmark bzw. den Thymus verlassen haben. In ihnen findet die Antigenpräsentation und -erkennung und di...
- KrankheitserregerWenn man vom Immunsystem spricht, spricht man auch unweigerlich von der Abwehr von Krankheitserregern. Das Wort Krankheitserreger ist aber ein sehr allgemeiner Begriff und gibt nur unzureichend die Vielfalt und Diversität von Erregern wieder. Krankheitserreger, so wie wir sie meistens meinen, sind...
- VirenViren (Einzahl: Virus, aus dem Lateinischen virus = Gift) sind kleine, bis zu 400 nm große, meist runde Partikel, die tierische, menschliche und pflanzliche Zellen infizieren können. Die infizierte Zelle wird als Wirtszelle oder kurz Wirt bezeichnet und die Viruspartikel, die außerhalb der Wirtze...
- BakterienBakterien bilden neben den Archaeen und Eukaryoten eine der drei großen grundlegenden Domänen, in die alle Lebewesen eingeteilt werden. Sie sind einzellige Organismen und gehören zu den Prokaryoten, was bedeutet, dass sie keinen echten Zellkern haben, sondern nur eine definierte Region, in der da...
- Exkurs: Weitere KrankheitserregerProtozoen („Urtierchen“) sind einzellige Organismen und gehören zu den Eukaryoten. Sie teilen viele Ähnlichkeiten mit tierischen Zellen und besitzen einen echten Zellkern, Mitochondrien und andere Organellen (Abbildung 1). Protozoen pflanzen sich durch Zellteilung fort und können als Parasite...
- Unspezifische und spezifische Immunreaktion
- Das Immunsystem Der menschliche Körper steht im ständigen Kontakt mit der Umwelt und ist daher auch permanent äußeren Bedrohungen (Krankheitserreger, Gifte, Strahlungen etc.) ausgesetzt. Aber auch von innen heraus kann der Körper gefährdet werden. Zum Beispiel können entartete Zellen sich zu Tumoren entwic...
- Die Teilsysteme des ImmunsystemsDer menschliche Körper steht im ständigen Kontakt mit der Umwelt und ist daher auch permanent äußeren Bedrohungen (Krankheitserreger, Gifte, Strahlungen etc.) ausgesetzt. Aber auch von innen heraus kann der Körper gefährdet werden. Zum Beispiel können entartete Zellen sich zu Tumoren entwic...
- Die Zellen des ImmunsystemsDie Zellen des Immunsystems werden durch die Leukozyten dargestellt, die alle während der Leukopoese im Knochenmark aus pluripotenten Stammzellen gebildet werden. Dabei gehen die Phagozyten (Granulozyten und die aus den Monozyten hervorgehenden Makrophagen) aus myeloischen Vorläuferzellen hervor u...
- Die Botenstoffe des ImmunsystemsDem Immunsystem stehen unterschiedliche Botenstoffe zur Verfügung, die der Kommunikation zwischen Immunzellen dienen. Dies geschieht über hormonartige Botenstoffe, die sogenannten Zytokine, zu denen die Interleukine, Interferone und Tumornekrosefaktoren gehören. Sie aktivieren Immunzellen, könne...
- Das unspezifische ImmunsystemWie bereits beschrieben, ist das unspezifische Immunsystem direkt nach der Geburt einsatzbereit und dient der nicht-selektiven Abwehr von potenziellen Krankheitserregern, wie Bakterien, Pilzen, Viren oder Parasiten. Es besteht aus: den Schutzbarrieren des Körpers, die das Eindringen von Erregern ve...
- Die Schutzbarrieren des KörpersUm das Eindringen von äußeren Krankheitserregern zu verhindern, hat der Körper verschiedene Schutzbarrieren entwickelt, die auf physikalischem und chemischem Wege wirken. So dienen die Haut und die Schleimhäute als mechanische Barrieren. Sie verhindern allerdings nicht nur physikalisch das bloß...
- Exkurs: Schädigung des Mikrobioms des Darms durch AntibiotikaWährend oder nach einer Antibiotika-Behandlung kommt es gehäuft zu Beschwerden des Verdauungstraktes wie Durchfall, Übelkeit oder Bauchschmerzen. Der Grund für diese Symptome ist häufig in der Schädigung des Mikrobioms durch die eingenommenen Antibiotika zu finden. Diese schädigen nicht nur u...
- Die Zellen des unspezifischen ImmunsystemsGelangen dennoch Mikroorganismen in den Körper, werden sie von Phagozyten erkannt und vernichtet (Abbildung 1). Phagozyten, auch „Fresszellen“ (griechisch: phagein = fressen) genannt, sind Leukozyten, die körperfremde Partikel (z. B. Erreger) und Zelltrümmer aufnehmen und verdauen können (Ph...
- Die humoralen Faktoren des unspezifischen ImmunsystemsDas Komplementsystem ist einer der Hauptpfeiler der humoralen unspezifischen Immunabwehr und besteht aus neun im Plasma gelösten Proteinen, die als Komplementfaktoren C1 bis C9 bezeichnet werden. Es reagiert vor allem auf Bakterien und körperfremde Zellen und fördert Entzündungsreaktionen. Dabei...
- Die EntzündungsreaktionDie Entzündungsreaktion ist eine akute Abwehrreaktion des Körpers und gehört vornehmlich zum unspezifischen Immunsystem. Sie tritt ein, wenn es zu Zell- oder Gewebsschäden kommt, oder wenn Mikroorganismen eindringen. Das Ziel ist stets, den Gewebsschaden zu begrenzen und die Ursache zu beseitig...
- Thermoregulation und FieberFieber (Pyrexie) ist aber keineswegs nur eine bloße Begleiterscheinung bei Entzündungsreaktionen. Es erfüllt auch durchaus spezifische Rollen im Immunsystem. Um nun aber zu verstehen, wie Fieber entsteht, muss man wissen, wie die Körpertemperatur reguliert wird (Thermoregulation). Als Führungs...
- Das spezifische Immunsystem Anders als das unspezifische Immunsystem, ist das spezifische Immunsystem nicht ab der Geburt verfügbar, sondern muss sich erst im Laufe der Lebenszeit entwickeln, weshalb man es auch als erworbenes Immunsystem bezeichnet. Es dient vorranging der spezifischen Abwehr von infizierten oder entarteten ...
- Der MHC-KomplexDas spezifische Immunsystem unterscheidet körpereigene Zellen von körperfremden, infizierten oder entarteten Zellen über die sogenannten MHC-Moleküle (MHC steht für major histocompatibility complex). Diese sind Oberflächenproteine, die von praktisch allen kernhaltigen Zellen gebildet werden un...
- Exkurs: AutoimmunerkrankungenWie bereits erwähnt, differenzieren sich T-Zellen im Thymus, in dem sie auch lernen, zwischen körpereigen und körperfremd zu unterscheiden (Selbsttoleranz). Die T-Zellen, die körpereigene Strukturen erkennen und dagegen vorgehen (autoimmune T-Zellen), werden dabei „aussortiert“ und eliminier...
- Abläufe einer T-Zell-vermittelten ImmunreaktionWie aber werden die verschiedenen T-Zell-Gruppen genau koordiniert und was passiert, wenn ein Virus den Körper befällt? Diese Fragen sollen im Folgenden Schritt für Schritt geklärt werden (Abbildung). Im ersten Schritt nimmt ein Phagozyt (Makrophage, dendritsche Zelle etc.) virale Partikel auf, ...
- Die Zellen des spezifischen Immunsystems: B-ZellenNeben den T-Zellen existiert noch eine weitere Zellgruppe, die für die spezifische Immunität verantwortlich ist: die B-Zellen (B-Lymphozyten). Diese entstehen ebenfalls während der Leukopoese im Knochen, reifen aber, anders als die T-Zellen, im Knochenmark heran. Da Knochenmark im Englischen bone...
- Abläufe einer B-Zell-vermittelten ImmunreaktionKommt es zu einer Infektion (Abbildung), können B-Zellen Antigene über ihren B-Zell-Rezeptor erkennen. Dabei nehmen sie den Erreger auf, verdauen diesen und präsentieren das entsprechende Antigen auf ihrem MHC-II-Molekül. Wie auch bei der schon beschriebenen T-Zell-vermittelten Immunantwort, neh...
- Die humoralen Faktoren des spezifischen ImmunsystemsEbenso wie das unspezifische Immunsystem, nutzt auch das spezifische Immunsystem Zytokine zur Kommunikation. Dabei kommen hauptsächlich Interleukine, Interferone und Tumor-Nekrose-Faktoren zum Einsatz....
- AntikörperklassenAlle im Blut und im Extrazellularraum vorkommende Antikörper lassen sich fünf Grundstrukturen einteilen, die man als Antikörperklassen bezeichnet:...
- Exkurs: LeihimmunitätDie Leihimmunität (Nestschutz) stellt eine frühe Form der Immunisierung von ungeborenen Kindern dar. Dabei passieren IgG-Antikörper, die von der Mutter gebildet werden, die Plazentaschranke und schützen so den Fötus. Dieser Schutz hält jedoch nur temporär an, da die IgG-Antikörper in den ers...
- Primäre und sekundäre ImmunantwortAls primäre Immunantwort beschreibt man den Erstkontakt (Erstinfektion) mit einem Antigen, z. B. einem Erreger. Hierbei wird zunächst das unspezifische Immunsystem aktiv, das sehr schnell damit anfängt, die Antigene zu beseitigen. Reicht dies nicht aus, springt das spezifische Immunsystem an. Hie...
- Organtransplantation Quittiert ein lebenswichtiges Organ oder Gewebe seinen Dienst, besteht die Möglichkeit, dieses zu ersetzen. Dabei wird ein Organ von einem Spender in einen Empfänger verpflanzt. Die erste langfristige Organtransplantation erfolgte 1954, als der US-amerikanische Chirurg Joseph Edward Murray am Pete...
- ImmunisierungAls Immunisierung beschreibt man das künstliche Herbeiführen einer Immunität (Unempfindlichkeit gegenüber einem Erreger). Man spricht in diesem Zusammenhang auch von einer Schutzimpfung (kurz: Impfung). Eine Immunisierung kann aber auch auf natürlichem Wege entstehen, wenn eine Erstinfektion er...
- Exkurs: Die Geschichte des ImpfensDer medizinische Fachbegriff für die Impfung lautet Vakzination. Dieser Begriff geht auf die erste Impfung der europäischen Geschichte zurück. Im späten 18. Jahrhundert wurde Europa von einer schweren Pocken-Epidemie heimgesucht, der viele Menschen, darunter besonders Neugeborene, zum Opfer fi...
- Grundlagen für die Arbeit des Immunsystems
- Grundlagen
- Mathe
- Q1 - Analysis
- Grundlagen der Differenzialrechnung
- AbleitungsregelnDie Ableitung f'(x) einer Funktion f(x) gibt die Steigung des Graphen von f(x) an der Stelle x an. Die Anzahl der Apostrophe (') gibt den Grad der Ableitung an. Demnach gibt f''(x) die Steigung des Graphen von f'(x) an.Im Folgenden werden einige Regeln zum Ableiten von Funktionen vorgestellt (Poten...
- Kurvendiskussion
- Allgemeiner Aufbau von KurvendiskussionenEine vollständige Kurvendiskussion besteht aus neun Schritten: dem Bestimmen der Ableitungen, des Definitionsbereichs, der Symmetrie, der Nullstellen, der Extrem- und Wendepunktstellen, der Monotonie und Krümmung sowie des Grenzverhaltens. Zuletzt werden diese markanten Punkte in ein geeignetes Ko...
- DefinitionsbereichIm Definitionsbereich liegen alle Zahlen, die für x eingesetzt werden dürfen, damit der Funktionsterm ein Ergebnis liefert. Im Normalfall handelt es sich hierbei um alle reellen Zahlen (R ). Jedoch gibt es auch hier einige Ausnahmen: Wurzeln: Steht im Funktionsterm die Variable unter einer Wurzel...
- Symmetrieeigenschaften Um die Symmetrieeigenschaften einer Funktion rechnerisch zu ermitteln, ersetzt man in der Ausgangsfunktion "x" durch "-x" und vergleicht die Funktion mit der Ausgangsfunktion. Es kommen drei Ergebnisse in Frage....
- NullstellenUm die Nullstellen zu bestimmen, wird die Funktion gleich 0 gesetzt, um die zugehörigen x-Werte zu bestimmen: f(x) = 0Die Ermittlung der x-Werte kann nach dem Nullsetzen auf verschiedenen Wegen stattfinden und ist auch auf die Berechnung von Extrem- und Wendestellen übertragbar. Grob lässt sich d...
- ExtrempunkteExtrempunkte sind die Punkte im Graph, an denen der Funktionswert maximal (Hochpunkte) oder minimal (Tiefpunkte) wird. Um diese nachzuweisen, werden zwei Bedingungen geprüfen und anschließend die genaue Koordinate berechnet: Zuerst muss die notwendige Bedingung geprüft werden. Finde hierfür all...
- WendepunkteWendepunkte sind Punkte, an denen sich das Krümmungsverhalten eines Graphs ändert. "Angenommen man fährt mit einem Auto den Graph entlang ist die Krümmung die Richtung, in die man das Lenkrad einschlägt. An dem Punkt, an dem sich die Richtung des Einschlags verändert, liegt der Wendepunkt." E...
- GrenzverhaltenDas Grenzverhalten beschreibt den Verlauf des Graphen, wenn man ihn in Richtung ∞ & -∞ (∞ steht für unendlich) laufen lässt. Man schreibt das Grenzverhalten mit Hilfe des sogenannten Limes auf. Entscheidend ist dabei jeweils der höchste Exponent der Funktion. Ausschließlich dieser wird bet...
- ZeichnungFür die Zeichnung wird zunächst ein passender Maßstab gesucht. Hierfür schaut man sich die bereits bestimmten Punkte (Nullstellen, Extrema und Wendepunkte) an und beschriftet anschließend die x- und y-Achse entsprechend. Durch das zuvor bestimmte Grenzverhalten muss zusätzlich noch das Verhalt...
- WertebereichDer letzte Schritt der Kurvendiskussion ist das Ablesen des Wertebereichs. Dieser Bereich gibt alle möglichen Funktionswerte (y-Werte) des Graphen an. Sollte der Graph also von ∞ bis -∞ verlaufen, so ist W = R . Sollte der Graph stattdessen beispielsweise in beide Richtungen gegen ∞ laufen un...
- Kurvendiskussion einer ganzrationalen Funktionen 1. Vorarbeit Ableitungen: f(x) = -2x² + x f‘(x) = -4x + 1 f‘‘(x) = -4 f‘‘‘(x) = 0 2. Definitionsbereich: D = R 3. Symmetrie: Die Funktion besitzt keine Symmetrie, da f(x) = -2x² + x f(-x) = -2 · (-x)² + (-x) = -2x² -x -f(x) = 2x² - x f(x) ≠ f(-x) f(-x) ≠ -f(x) 4. Nulls...
- e-Funktion
- Kurvendiskussion einer e-FunktionDas e in der e-Funktion steht für die Eulersche Zahl, welche gerundet dem Wert 2,71828 entspricht. Die Besonderheit der e-Funktion ist, dass sie die einzige Funktion ist, welche sich beim Auf- und Ableiten nicht verändert.Es gilt daher:f(x) = exf'(x) = exF(x) = ex...
- Beispiel einer Kurvendiskussion einer e-Funktion1. Vorarbeit: f(x) = (x + 1) · e-x f‘(x) = 1 · e-x + (x + 1) · e-x · (-1) f‘(x) = e-x - (x + 1) · e-x f‘(x) = (1 - x - 1) · e-x f‘(x) = -x · e-x f‘‘(x) = (-1) · e-x + (-x) · e-x · (-1) f‘‘(x) = -e-x + x · e-x f‘‘(x) = ...
- Vertiefung der Differenzialrechnung
- Tangente und OrthogonaleDas Wort Tangente leitet sich von dem lateinischen Wort "tangere" ab, welches "berühren" bedeutet. Eine Tangente ist demnach eine Gerade, die den Graphen einer Funktion an einer Stelle x0 berührt, aber nicht schneidet....
- Rekonstruktion einer FunktionManchmal wird in der Aufgabenstellung nicht die Funktion direkt gegeben, sondern Punkte oder Informationen einer Funktion, mithilfe derer die Funktion dann rekonstruiert werden soll. Um möglichst leicht eine Funktion rekonstruieren zu rekonstruieren, gibt es folgende Schritte: Allgemeine Funktions...
- Kurvendiskussion einer KurvenscharBei der Kurvendiskussion einer Kurvenschar ist neben dem x-Wert noch ein weiterer Parameter vorhanden. Wichtig ist, dass man den zweiten Buchstaben bei der Rechnung wie eine Zahl behandelt, daher kann diese Variable bei Rechnungen und auch Lösungen einfach stehen bleiben. Der Rechenweg selbst änd...
- Beispiel einer Kurvenschar einer e-Funktion1. Vorarbeit: fa(x) = (x + a) · ex-a fa‘(x) = 1 · ex-a + (x + a) · ex-a fa‘(x) = (x + a + 1) · ex-a fa‘‘(x) = 1 · ex-a + (x + a + 1) · ex-a fa‘‘(x) = (x + a + 2) · ex-a fa‘‘‘(x) = 1 · ex-a + (x + a + 2) · ex-a fa‘‘‘(x...
- Ortskurve einer KurvenscharPunkte einer Kurvenschar, die eine gewisse Eigenschaft erfüllen (beispielsweise Nullstellen, Extrema oder auch Wendepunkte), lassen sich in einer sogenannten Ortskurve darstellen. Auf der Ortskurve eines Hochpunktes einer Kurvenschar liegen alle Hochpunkte für die unterschiedlichen Werte der Varia...
- Integralrechnung
- Integralrechnung mit Ober- und UntersummeDie Integralrechnung dient der Bestimmung einer Fläche zwischen einem Graphen und der x-Achse. Um dies zunächst zu vereinfachen, gibt es die Überlegung Rechtecke zwischen der Funktion und der x-Achse zu zeichnen. Die Breite dieser Rechtecke wird ∆x genannt und im Vornerein angegeben. Die Höhe ...
- Bilden der StammfunktionMeistens ist es leichter, mit einem Integral die Fläche zwischen einem Graph und der x-Achse zu berechnen. Um mit einem Integral arbeiten zu können, müssen wir zunächst die Stammfunktion bilden. Dies ist jene Funktion, welche abgeleitet zu unserer Ausgangsfunktion führt. Um eine Stammfunktion ...
- Ermitteln der Stammfunktion durch KoeffizientenvergleichDas „Ermitteln einer Stammfunktion durch Koeffizientenvergleich“ klingt zunächst kompliziert, ist aber deutlich einfacher als du vielleicht denkst. Das Vorgehen erklären wir im Folgenden und zeigen es anhand eines Beispiels: Bei dieser Art von Aufgaben sind häufig die Ausgangsfunktion f(x) un...
- Den Wert eines Integrals berechnen Um den Wert eines Integrals zu berechnen, werden eine Ausgangsfunktion, ihre Stammfunktion sowie ein Intervall, über welches integriert wird, benötigt. Der Wert des Integrals berechnet sich anschließend mit folgender Formel:...
- Flächenberechnung zwischen der x-Achse und einem Graphen Um die Fläche zwischen der x-Achse und dem Graphen in einem bestimmten Intervall berechnen zu können, muss folgende Überlegung angestellt werden: Es ist möglich, dass Abschnitte des Graphen in dem vorgegebenen Intervall unter- und oberhalb der x-Achse liegen. Diese werden durch eine oder mehrere...
- Durch Parallelen begrenzte IntegraleDie Berechnung der Fläche zwischen einem Graphen und einer Parallelen der x-Achse stellt eine abgewandelte Aufgabe der Berechnung der Fläche zwischen einem Graphen und der x-Achse dar. Bei dieser Aufgabenart muss die Funktion f(x) entsprechend dem Faktor, um den die Parallele von der x-Achse abwei...
- Berechnen der Fläche zwischen zwei GraphenAuch bei diesen Aufgaben bleibt die Herangehensweise der vorherigen Aufgaben sehr ähnlich. Um die Fläche zwischen zwei Graphen zu berechnen, benötigen wir die Differenzfunktion der beiden Funktionen. Die Differenzfunktion erhalten wir, indem wir die eine Funktion von der anderen abziehen. Rechens...
- Uneigentliche IntegraleBei der Integralrechnung gibt es Aufgaben, bei denen die Funktion keine Nullstellen besitzt. Bei solchen nähert sich der Graph der x-Achse zwar stetig an, schneidet diese jedoch nie. In solchen Fällen lässt sich mit Hilfe des uneigentlichen Integrals dennoch eine endliche Fläche berechnen. Auch ...
- Integralaufgaben mit ParameterIn einigen Aufgaben kommt in der Funktion eine Variable vor. Meist ist zu dieser Variablen schon die Größe der Fläche, welche der Graph einschließen soll, in der Aufgabenstellung angegeben. Mithilfe dieser Angabe soll dann die Variable bestimmt werden. Um die Variable zu ermitteln, muss entspre...
- Winkel einer Funktion bestimmenFunktionen können in gewissen Winkeln in andere Funktionen übergehen oder in den „Boden“ münden. Der Boden verläuft in Aufgaben zumeist waagerecht und kann demnach also mit der x-Achse gleichgesetzt werden. Rechenweg: Der Winkel einer Funktion lässt sich berechnen, indem der x-Wert der ge...
- Exponentielles WachstumExponentielles Wachstum liegt vor, wenn sich eine Funktion innerhalb eines Zeitschritts immer um denselben Faktor erhöht oder verkleinert. Ein Beispiel hierfür wäre eine Funktion, die alle 2s um 50% wächst. In einer Tabelle ist diese Eigenschaft daran erkennbar, dass f(t+1)/f(t) konstant ist. Kl...
- Rotation um die x-AchseUnter einem Rotationskörper versteht man einen Graphen, der um die x-Achse rotiert wird. Dadurch entsteht ein dreidimensionaler Körper, dessen Volumen mit folgender Formel berechnet werden kann:...
- Grundlagen der Differenzialrechnung
- Q2 - Lineare Algebra
- Gleichungssysteme
- Aufbau von GleichungssystemenInnerhalb der linearen Algebra kommt es immer wieder vor, dass verschiedenste Gleichungssysteme gelöst werden sollen. Jedes Gleichungssystem besteht aus einer bestimmten Anzahl verschiedener Gleichungen. Diese Gleichungen setzen unbekannte Variablen in eine bestimmte Abhängigkeit zueinander. Unte...
- Verfahren zum Lösen von GleichungssystemenZiel der Verfahren ist es, nach der Verrechnung zweier Zeilen eine Variable weniger zu haben als vorher. Diesen Vorgang wiederholt man so lange bis in einer Gleichung nur noch eine Variable übrig bleibt. Diese kann dann bestimmt werden. Die bekannte Variable kann anschließend in die anderen Gleich...
- Arten von GleichungssystemenBei einem gewöhnlichen Gleichungssystem gibt es genauso viele Gleichungen wie Variablen. Daher können zum Bestimmen der Variablen die oberen Verfahren so lange angewandt werden, bis alle Variablen bestimmt sind.Beispiel:I 2 = 1s -2rII -4 = -2s – 4rSubtraktionsverfahren anwenden: 2۰I – II 4 = ...
- Grundlagen der lineare Algebra
- Einführung VektorenEin Vektor hat eine Richtung und eine Länge. Es handelt sich um eine Angabe, wie weit man in eine bestimmte Richtung zu gehen hat. Ein Vektor beschreibt demnach, wie man von einem Punkt im Koordinatensystem zu einem anderen kommt. Jedem Punkt im Raum lässt sich eindeutig ein Ortsvektor zuordnen....
- Länge eines dreidimensionalen VektorsEin dreidimensionaler Vektor verläuft durch alle drei Dimensionen des Raums und hat ebenfalls immer eine bestimmte Länge und Richtung. Die Länge eines Vektors wird auch "Betrag des Vektors" genannt und lässt sich mit dem räumlichen Pythagoras bestimmen. Bei der Formel des Pythagoras werden alle...
- Skalarmultiplikation eines VektorsUnter der skalaren Multiplikation versteht man die Multiplikation eines Vektors mit einer Zahl. Rechnerisch bedeutet dies, dass man jede einzelne Koordinate, also Zeile des Vektors mit dem Faktor multipliziert. Anschaulich heißt es, dass sich nicht die Richtung, sondern nur die Länge des Vektors v...
- Rechnen mit VektorenUm zwei Vektoren zu addieren, werden Werte derselben Zeile addiert. Anschaulich beschrieben läuft man zuerst den ersten Vektor entlang, um anschließend dem zweiten zu folgen. Das Ergebnis ist der direkte Weg zwischen dem Start und dem Ziel. Beispiel:...
- Lineare Abhängigkeit bzw. UnabhängigkeitBei der linearen Abhängigkeit bzw. Unabhängigkeit wird untersuchen, ob zwei Vektoren kollinear zueinander sind. Zwei oder mehr Vektoren sind kollinear, wenn sie in dieselbe oder genau entgegengesetzte Richtung zeigen, also parallel sind. Rechnerisch bedeutet dies, dass sie Vielfache voneinander si...
- Das SkalarproduktDas Skalarprodukt wird in einigen Formeln der linearen Algebra verwendet. Die wichtigste Anwendung dieser Rechnung findet sich bei der Berechnung von Winkeln zwischen zwei Vektoren. Unter dem Skalarprodukt versteht man die Multiplikation von Vektoren....
- Geraden
- Konstruieren einer Geradengleichung aus zwei PunktenEine Gerade wird in der linearen Algebra folgendermaßen beschrieben: Man startet bei einem Punkt, von dem man weiß, dass er auf der Geraden liegt. Dieser Punkt wird unser Ortsvektor. Von diesem Punkt aus geht man dann in eine bestimmte Richtung. Diese Richtung wird durch den sogenannten Richtungsv...
- Punktprobe bei GeradenHäufig wird gefragt, ob ein dritter Punkt auf einer Geraden liegt. Um dies zu überprüfen, wurde die sogenannte Punktprobe entwickelt. Rechenweg: Wenn ein Punkt auf einer Gerade liegt, muss es möglich sein, für den Parameter r einen Wert einzusetzen, der von dem Stützvektor aus zu dem gegebenen...
- Lagebeziehung von GeradenZwei Geraden können in einem Raum in verschiedenen Lagebeziehungen zueinander stehen. Diese Lagebeziehungen können mithilfe verschiedener Rechenwege ermittelt werden. Hierbei unterscheidet man vier verschiedene Möglichkeiten: Die Geraden sind parallel zueinander, liegen aber nicht aufeinander. D...
- Schnittwinkel von GeradenDer Schnittwinkel zwischen Geraden lässt sich nur bestimmen, wenn diese einen Schnittpunkt besitzen. Sollte dies der Fall sein, benutzt man ihre Richtungsvektoren und verwendet die Winkelformel. Es gilt daher:...
- Ebenen
- Aufstellen der Ebenengleichung in der Parameterform Wie bereits bei der Konstruktion von Geraden benötigt man auch bei der Ebenenkonstruktion einen Punkt, welcher in der Ebene liegt. Dieser wird auch hier zu unserem Stützvektor. Auch der Richtungsvektor bleibt uns erhalten, wird jedoch durch einen zusätzlichen zweiten Richtungsvektor ergänzt. Dab...
- NormalenvektorDer Normalenvektor ist ein Vektor, der senkrecht auf zwei anderen Vektoren steht. Bildet man den Normalenvektor, der senkrecht zu den beiden Richtungsvektoren einer Ebene steht, so steht dieser auch senkrecht zur Ebene und zu jedem Punkt der Ebene. Jener Normalenvektor wird für viele weitere Rechnu...
- Koordinatenform der EbeneDie Koordinatenform der Ebene ist die wohl praktischste Form für Rechnungen mit Ebenen. Man kann sie sowohl für Punktproben, Lagebeziehungen oder Winkelberechnungen verwenden. Aufstellen der Koordinatenform: Zuerst wird der Normalenvektor der Ebene herausgeschrieben oder berechnet. Durch den Norm...
- Lagebeziehung Ebene und GeradeÄhnlich wie zwei Geraden können auch eine Ebene und eine Gerade ein bestimmtes Lageverhältnis einnehmen. Dieser Aufgabentyp kann ebenfalls sehr gut mit einem Algorithmus gelöst werden....
- Schnittwinkel von Ebene und GeradeÄhnlich wie zwischen zwei Geraden kann auch zwischen einer Ebene und einer Gerade ein Schnittwinkel berechnet werden. Wer noch die Formel für den Schnittwinkel zwischen zwei Geraden im Kopf hat, wird es auch bei diesem Aufgabentyp leicht haben....
- Lagebeziehung zwischen EbenenDas Thema Lagebeziehung zwischen Ebenen ist kein Pflichtstoff des aktuellen Kerncurriculums, wurde von uns jedoch aus Gründen der Vollständigkeit im Skript beibehalten. Lagebeziehungen: Für die Lage zwischen zwei Ebenen gibt es wieder drei verschiedenen Varianten: Die beiden Ebenen können echt ...
- Schnittwinkel von EbenenAuch für den Schnittwinkel von Ebenen ist erforderlich, dass sie eine Schnittgerade besitzen. Trifft dies zu, wird ebenfalls mit dem Normalenvektor gearbeitet. Da dieser auf beiden Ebenen senkrecht steht, ist die Differenz von 90 Grad zu vernachlässigen. Diese Differenz gleicht sich aus und man ka...
- LotfußpunktverfahrenDer Lotfußpunkt ist jener Punkt auf einer Ebene, welcher den geringsten Abstand der Ebene zu einem anderen Punkt aufweist. Das Lotfußpunktverfahren findet also Anwendung bei Aufgaben, bei denen der geringste Abstand zwischen einem Punkt und einer Ebene gesucht wird. Die Verbindungsgerade des Lotfu...
- Abstand Punkt und EbeneFür den Abstand von einem Punkt und einer Ebene bildet man zunächst - wie beschrieben - den Lotfußpunkt. Dies ist dann der Punkt der Ebene, der den geringsten Abstand zum Punkt besitzt. Nun kann man den Verbindungsvektor zwischen dem Punkt P und dem Lotfußpunkt aufstellen und dessen Betrag besti...
- Gleichungssysteme
- Q3 - Stochastik
- Grundlage
- Allgemeines und BegriffserklärungenIn der Stochastik beschäftigt man sich mit Prozessen, deren Ausgänge nicht eindeutig vorhersehbar sind. Man spricht hierbei von Zufallsexperimenten. Innerhalb dieser Zufallsexperimente gibt es einige Grundbegriffe, welche hier zunächst erklärt werden. Der Ergebnisraum bzw. die Ergebnismenge bild...
- Laplace-WahrscheinlichkeitDefinition: Von einem Laplace-Experiment spricht man, wenn alle Ausgangsmöglichkeiten eines Zufallsexperimentes gleich wahrscheinlich sind. Hier gilt:...
- Empirisches Gesetz der Großen ZahlenNeben dem Laplace-Experiment solltest du auch das Empirische Gesetz der Großen Zahlen kennen. Spezielle Aufgaben hierzu gab es im Abitur zwar eher selten, jedoch wäre es wichtig zu wissen, wovon die Rede ist, sollte dieser Begriff in einer Aufgabenstellung auftauchen. Spätestens in der mündliche...
- Vereinigungs- und Schnittmenge & GegenereignisBetrachtet man zwei Ereignisse gleichzeitig, so spricht man oft auch von einer Vereinigungs- oder einer Schnittmenge. Die Vereinigungsmenge verwendet man, wenn mindestens eines der beiden Ereignisse E1 bzw. E2 eintritt. Von einer Schnittmenge hingegen spricht man, wenn sowohl E1 als auch E2 eintrit...
- Berechnung von Wahrscheinlichkeiten
- KombinatorikDie Kombinatorik erlaubt es uns, auf relativ einfache Weise eine Anzahl von Möglichkeiten zu berechnen. Bei den meisten Aufgaben kann die Anzahl der Möglichkeiten mithilfe des Urnenmodells berechnet werden. Hierbei ist n die Anzahl der Kugeln, die aus einer Urne entnommen werden, und k die Anzahl ...
- „Mindestens“-AufgabenAnwendung findet das Gegenereignis oft in „mindestens“-Aufgaben. Hier ist es meistens leichter das Gegenereignis aufzustellen und dessen Wahrscheinlichkeit zu berechnen als die des eigentlichen Ereignisses. Hierfür wird die Formel umgestellt zu:...
- BaumdiagrammeBaumdiagramme werden angewandt, um ein mehrstufiges Zufallsexperiment übersichtlich abzubilden. Dadurch kann man auch einfache Zufallsexperimente, welche öfter hintereinander durchgeführt werden, darstellen....
- Dreimal "Mindestens"-AufgabenBei diesen Aufgabentypen wird die Anzahl von Versuchen berechnet, die man mindestens braucht, damit eine Mindestanzahl von Ereignissen zu mindestens x Prozent eintritt (die Prozent sind dabei immer angegeben). Wie die Überschrift schon verrät, steht in den meisten solcher Aufgaben dreimal das Wort...
- Prüfungsanalyse: Dreimal „Mindestens"-AufgabenDie Dreimal "Mindestens"-Aufgaben kommen im Abitur nicht sehr häufig dran. Wenn sie sich doch einmal einschleichen, sind sie jedoch kein Hexenwerk. Du musst sie lediglich anhand der Aufgabenstellung erkennen und dir merken, dass sie immer durch das selbe Vorgehen gelöst werden können. Dadurch has...
- Bedingte und Totale WahrscheinlichkeitenZunächst stellt sich hier die Frage: Was sind bedingte Wahrscheinlichkeiten? Die Wahrscheinlichkeit eines Ereignisses ist eine relative Größe. Sie kann durch zusätzliche Informationen beeinflusst werden. Schauen wir uns als Beispiel das abgebildete Glücksrad an. Die Wahrscheinlichkeit, dass bei...
- Prüfungsanalyse: Bedingte WahrscheinlichkeitenAufgaben zu bedingten Wahrscheinlichkeiten sind gelegentlich Bestandteil des Abiturs und können meist mit einem Baumdiagramm gelöst werden. Dabei sollte vor allem darauf geachtet werden, dass sich die Wahrscheinlichkeiten auf den Ästen je nach Situation verändern können....
- Inverses BaumdiagrammTeilweise lassen sich gesuchte bedingte Wahrscheinlichkeiten nicht, wie bei dem letzten Beispiel, direkt aus den Textinformationen ablesen. Stattdessen benötigt man als Zwischenschritt ein Inverses Baumdiagramm. In diesem werden die Stufen des Ausgangsdiagramms umgekehrt. Wenn zunächst in der erst...
- Satz von BayesDer Satz von Bayes vereinfacht es, bestimmte bedingte Wahrscheinlichkeiten zu ermitteln. Wir nutzen das Wissen, dass die Wahrscheinlichkeit für P(A∩B) sich nicht verändert, egal ob erst A oder erst B eintritt. Mit diesem Wissen können wir dann eine Gleichung bilden, die wir nach der bedingten W...
- Vier-Felder-TafelEine andere Darstellungsweise neben den Baumdiagrammen bilden die Vier-Felder-Tafeln. Diese sind häufig übersichtlicher in der Darstellung und einfacher in der Handhabung.Für die zwei Ereignisse A und B sieht die Tafel folgendermaßen aus:...
- Unabhängigkeit von EreignissenIm Folgenden soll es um die Unabhängigkeit von Ereignissen gehen. Ereignisse sind dann unabhängig voneinander, wenn sich die Wahrscheinlichkeit des einen nicht verändert, auch wenn das andere bereits eingetreten ist....
- Wahrscheinlichkeitsverteilungen
- Zufallsgrößen
- WahrscheinlichkeitsverteilungBei vielen Experimenten können die verschiedenen Ereignisse mit unterschiedlicher Häufigkeit eintreten. Die Wahrscheinlichkeitsverteilung soll angeben, wie wahrscheinlich der Eintritt eines Ereignisses ist....
- ErwartungswertDefinition: Der Erwartungswert einer Zufallsvariable ist der Durchschnittswert, den die Zufallsvariable annimmt. Vergleichen lässt sich dies mit der Durchschnittsnote einer Klassenarbeit. Diese Durchschnittsnote spiegelt den Durchschnitt aller erreichten Noten wider. Auch beim Erwartungswert kann e...
- Prüfungsanalyse: ErwartungswertImmer mal wieder findet eine Aufgabe den Weg ins Abitur, bei der es sich um ein Gewinnspiel handelt, für welches bestimmt werden muss, ob es sich um ein faires Spiel handelt oder nicht. Hier hilft die bekannte Tabelle, welche den Gewinn und die Wahrscheinlichkeit für diesen aufführt. Auch wenn ni...
- Varianz und StandardabweichungEinleitung: Der Erwartungswert allein reicht nicht vollkommen aus, um eine Zufallsvariable ausreichend zu beschreiben. Eine weitere hilfreiche Angabe zur Beschreibung von Zufallsvariablen ist die Streuung der Variablen um den Mittelwert, die sogenannte Varianz. Um diesen Sachverhalt näher zu beleu...
- Binomialverteilung
- BinomialverteilungDie Binomialverteilung beschreibt eine der wichtigsten Verteilungen von Wahrscheinlichkeiten in der Stochastik. Wenn sie gilt, ist es möglich, Formeln zu verwenden, die das Bestimmen des Erwartungswerts, der Varianz und der Standardabweichung erleichtert. Sie findet beispielsweise bei Bernoulli-Exp...
- Die kumulierte BinomialverteilungDie Binomialverteilung ist sehr praktisch, um punktuelle Wahrscheinlichkeiten auszurechnen. Lautet die Frage: „Wie hoch ist die Wahrscheinlichkeit, dass in zehn Würfen mit einer Münze sechs-mal Kopf geworfen wird?“, kann diese Aufgabe mithilfe der Bernoulli-Formel leicht gelöst werden. Wenn m...
- Prüfungsanalyse: Binomialverteilung Bernoulli-Aufgaben fehlen in kaum einem Vorschlag des Aufgabentyps C. Hier ist es wichtig die beiden Bedingungen, welche es uns erlauben mit den Formeln zu arbeiten, vor Augen zu haben. Diese Bedingungen sind, dass es (1.) genau zwei Ausgangsmöglichkeiten gibt, deren (2.) Wahrscheinlichkeit sich n...
- Die Sigma-UmgebungDie σ-Umgebung (gesprochen: sigma-Umgebung) hilft uns, mithilfe des Erwartungswertes eine Aussage zu treffen, wie wahrscheinlich der Ausgang eines Experiments in einem bestimmten Bereich liegt. Bei allen Binomialverteilungen wird die Wahrscheinlichkeit der σ-Umgebung für eine häufig durchgeführ...
- NormalverteilungDie Normal- oder Gaußverteilung beschreibt ein bestimmtes Modell in der Statistik. Es zeichnet sich dadurch aus, dass ca. zweidrittel aller Messwerte innerhalb einer Standartabweichung um den Mittelwert liegen. Bei der graphischen Darstellung ähneln normalverteilte Daten einer Glocke, weshalb die ...
- Zufallsgrößen
- Hypothesentests
- Einleitung zu HypothesentestsBei unserem letzten Thema handelt es sich um die Hypothesentests. Für viele stellen diese ein Buch mit sieben Siegeln dar. Da Hypothesentests jedoch leicht verdiente Punkte sein können, sobald man sie einmal durchschaut hat, soll ihr Zweck nun erstmal durch eine Geschichte erläutert werden....
- Vorgehen und Beispiele bei HypothesentestsBei Hypothesentests gibt es zwei verschiedene Fragestellungen: Der α-Fehler ist gesucht und die Entscheidungsregel ist gegeben. Im Falle unserer Geschichte ist dies die Wahrscheinlichkeit, dass der Narr trotz fairem Würfel (HO) hingerichtet wird (Ergebnis von H1). Die Entscheidungsregel ist gesuc...
- Prüfungsanalyse: HypothesentestHypothesentests haben in den letzten Jahren ihren Platz im Vorschlagstyp C gefestigt. Sie bilden nun meistens den Abschluss dieses Vorschlags und somit auch den Abschluss des Matheabiturs generell. Es geht hier nur noch ein letztes Mal darum, die Aufgabe ordentlich zu lesen, die gegebenen Informati...
- Grundlage
- Q1 - Analysis
- Sport
- Grundlagen sportlicher Leistungsfähigkeit
- Definition Sport und TrainingBevor wir genauer auf die einzelnen Bereiche eingehen, werden wir in den folgenden Absätzen die Frage klären, was Sport überhaupt ist. Diese Frage ist jedoch nicht eindeutig zu beantworten, da es nicht die eine Definition von Sport gibt. So definiert der Duden beispielsweise Sport als eine „nac...
- Faktoren der sportlichen LeistungsfähigkeitSportliche Leistungsfähigkeit wird bedingt durch: Kondition: Konditionelle Fähigkeiten umfassen die grundlegenden körperlichen Fähigkeiten eines Sportlers und werden in die vier Komponenten Ausdauer, Kraft, Beweglichkeit und Schnelligkeit aufgeteilt. Technik/Koordination: Im Sport spielen mo...
- Motorische GrundeigenschaftenDie motorischen Grundeigenschaften stellen die Grundlage jeder sportlichen Tätigkeit dar. Sie können in zwei, sich gegenseitig beeinflussende Bereiche unterschieden werden: Die konditionellen Fähigkeiten bündeln die zugrunde liegenden energetischen Prozesse. Die koordinativen Fähigkeiten umfa...
- Beanspruchung, Belastung und körperliche AnpassungJeder Sportler strebt in einem unterschiedlich großen Maße eine Leistungssteigerung an. Grundvoraussetzung für diese Steigerung sind Trainingseinheiten mit einer geeigneten Belastung. Unter Belastung kann die Summe, der von außen an einen Sportler gestellten Anforderungen verstanden werden. Die...
- Prinzip der Homöostase und SuperkompensationDer menschliche Körper steht ständig unter dem Einfluss seiner Umwelt. Wird der Körper durch eine Belastung - beispielsweise im Rahmen einer Trainingseinheit - beansprucht, so erfolgt im Rahmen dieser Belastung immer auch eine Anpassungsreaktion. Diese hat das Ziel, auf zukünftige Belastungen di...
- Trainingsprinzipien Trainingsprinzipien dienen als Richtlinien für die zielgerichtete Gestaltung des Trainings. Dabei sollten diese Prinzipien keinesfalls als gesetzt, sondern vielmehr als übergeordnete Orientierungsgrundlage verstanden werden. Prinzip der trainingswirksamen Belastungen: Dieses Prinzip beruht auf d...
- Trainingsplanung, -steuerung und -diagnostikDie Trainingssteuerung kann als zielgerichteter und strukturierter Prozess zur Planung, Durchführung und Auswertung des Trainings angesehen werden. Bei diesem Prozess müssen die Trainingsziele mit den Grundvoraussetzungen des Sportlers sowie den Trainingsprinzipien abgestimmt werden. Zu Beginn der...
- AufwärmenVor einer sportlichen Belastung sollte ein adäquates Aufwärmen stattfinden. Im Folgenden werden wir auf die Funktionen sowie Grundsätze und Formen des Aufwärmens eingehen. Funktion: Physiologische Vorbereitung: Das Aufwärmen bereitet die körperlichen Systeme auf das Abrufen sportlicher Leist...
- Aktiver Bewegungsapparat
- Muskelaufbau und -kontraktionUm eine Bewegung auszuführen, sind die meisten Skelettmuskeln des menschlichen Körpers über Sehnen mit Knochen verbunden. Durch die aktive Verkürzung des Muskels werden die Ansatzpunkte der Muskeln einander angenähert und es kommt zu einer Bewegung in einem oder mehreren Gelenken. Um genau zu v...
- Arbeitsweisen und Kontraktionsformen der Skelettmuskulatur und muskuläre DysbalancenEs können jeweils drei Arbeitsweisen und Kontraktionsformen unterschieden werden. Diese werden im Folgenden gemeinsam erläutert: Positiv dynamische Arbeitsweise – konzentrische Kontraktion: Zu Beginn eines Klimmzuges hängt der Sportler mit gestreckten Armen an einer waagerechten Stange. Nu...
- Hauptmuskelgruppen der Skelettmuskulatur Die „Hauptmuskelgruppen der Skelettmuskulatur“ sind seit kurzem neuer Bestandteil des Kernkurrikulums. Wichtig ist dabei diejenigen Muskeln zu kennen, die bei einer Belastung entscheidend beansprucht werden. So komplex dieses Thema auf den ersten Blick auch wirken mag, brauchst du dir hierbei k...
- Energiebereitstellung und Leistungsschwellen Bei der Muskelkontraktion ist ATP (Adenosintriphosphat) der einzig verwertbare Energielieferant. ATP löst in diesem Zusammenhang die Verbindung von Aktin und Myosin, um eine erneute Bindung möglich zu machen. Man spricht in diesem Zusammenhang auch von der „Weichmacherfunktion“. Ist zu wenig A...
- Beispielaufgabe EnergiebereitstellungDa in der Vergangenheit im Abitur bereits des Öfteren die Energiebereitstellung anhand eines vorgegebenen Beispiels erklärt werden sollte, werden wir im Folgenden eine Beispielaufgabe anführen und diese anschließend beantworten. ...
- Exkurs: Analyse von LaktatkurvenIn den vergangenen Jahren wurden im Material häufig Laktatkurven von Sportlern dargestellt, welche es anschließend zu analysieren galt. Diese Analyse mag im ersten Moment zwar abschrecken, ist jedoch, wenn man auf einige Eckpunkte achtet, einfach zu meistern und kann ein guter Weg sein, um Punkte ...
- Ausdauer
- Strukturmodell Ausdauer Ausdauer kann als psychische und physische Ermüdungswiderstandsfähigkeit im Rahmen einer sportlichen Belastung beschrieben werden. Sie schließt auch die Erholungsfähigkeit nach Beendigung der Belastung mit ein. Im Rahmen des Strukturmodells können verschiedene Komponenten unterschieden werden:...
- GrundlagenausdauerDie Grundlagenausdauer (GLA) bezeichnet die Fähigkeit des Körpers, Beanspruchung im aeroben Bereich über einen möglichst langen Zeitraum aufrecht zu erhalten und anschließend schnell regenerieren zu können. Ein gewisses Maß an Grundlagenausdauer ist für jeden Sportler, vom Gewichtheber bis z...
- Physiologische Anpassung des Körpers an das AusdauertrainingIm Folgenden wird näher auf die Anpassungsprozesse des Körpers im Rahmen von Ausdauertraining eingegangen. ...
- Trainingsmethoden
- Einleitung Trainingsmethoden Je nach Ziel eines Athleten müssen die Belastungsmerkmale des Trainings ausgelegt werden. Diese Belastungsmerkmale (Reizstärke, -dauer, -umfang und -dichte) bedingen sich gegenseitig und sollten möglichst nahe an den Belastungsmerkmalen des Sports selbst angelehnt sein. Bei der Kombination der Be...
- DauermethodeDie Dauermethode kann in eine extensive und intensive Dauermethode unterteilt werden und dient primär der Verbesserung der aeroben Leistungsfähigkeit....
- IntervallmethodeDie Intervallmethode wird, wie auch die Dauermethode, in intensive und extensive Intervallmethode unterteilt. Charakteristisch für die Intervallmethode sind zwei verschiedene Kriterien: Geplanter Wechsel von Belastungs- und Pausenintervallen → keine kontinuierliche Belastung wie bei der Dauermet...
- Wiederholungsmethode und Wettkampfmethode Durchführung: Dem Prinzip der Wiederholungsmethode liegt zu Grunde, dass der Sportler eine Strecke mit maximaler Geschwindigkeit/Intensität durchläuft und nach jeder Belastung eine vollständige (=echte) Erholungspause erfolgt. Die Distanz und Wiederholungsanzahl werden gezielt niedrig gehalten,...
- Ausdauertests Wie bereits im Kapitel „Trainingssteuerung“ dargestellt, sind Tests zur Messung der sportlichen Leistungsfähigkeit wichtig, um den Trainingsfortschritt eines Sportlers zu beurteilen. Im Ausdauerbereich gibt es eine Reihe von Tests wie den Cooper-Test, den Conconi-Stufentest, den Laktatstufente...
- Exkurs: Trainingsplanung Im Abitur soll gelegentlich ein Trainingsplan für eine Sportler einer bestimmten Sportart erstellt werden. Auch hier gibt es wieder verschiedene Wege zum Ziel. Einen möglichen Weg bzw. ein hilfreiches Konzept zum Erstellen eines Trainingsplans wollen wir dir hier vorstellen: Informationen herausa...
- Kraft
- Grundlagen KrafttrainingKraft bezeichnet die Fähigkeit des Muskel-Nerven-Systems durch Muskelkontraktion Widerstände zu überwinden, ihnen entgegenzuwirken oder sie zu halten. Dabei kann das Thema Kraft in unterschiedliche Kraftarten unterteilt werden (Maximalkraft, Kraftausdauer, Schnellkraft und Reaktivkraft)....
- Ziele und des Wirkung KrafttrainingsMithilfe des Krafttrainings können verschiedene Ziele erreicht werden. Je nach Motiv des Sportlers stehen dabei einzelne Ziele im Vordergrund: Leistungssteigerung: Durch Krafttraining kann die Leistung in der jeweiligen Sportart gesteigert werden. Dabei kann die verbesserte Kraftfähigkeit Vorauss...
- Trainingsarten - Maximalkraft Jedes Krafttraining muss für einen Sportler genau auf die Anforderung seiner Sportart, Position und körperliche Konstitution angepasst sein. Daher muss bei der Erstellung eines Trainingsplans immer darauf geachtet werden, welche Muskelgruppe und Kraftarten – Schnellkraft, Maximalkraft, Kraftausd...
- Trainingsarten - Kraftausdauer & SchnellkraftDie Kraftausdauer setzt sich aus den beiden konditionellen Fähigkeiten Kraft und Ausdauer zusammen. Folglich wird eine gute Kraftausdauer vor allem in Sportarten mit Ausdauercharakter und vielen Belastungsspitzen benötigt. Bei der Tour de France zum Beispiel steigt an jedem Anstieg die Belastung a...
- Exkurs Rehatraining & Theorie des MuskelaufbausNach einer Verletzung oder Operation eines Sportlers muss dieser stufenweise an das ursprüngliche Training herangeführt werden. Für die verschiedenen Regenerationsphasen bieten sich verschiedene Trainingsmethoden an. Werden diese adäquat eingesetzt, kann der Sportler eine optimale Genesung erfah...
- Organisationsformen des KrafttrainingsBeim Stationstraining gibt es, ähnlich wie beim Zirkeltraining, verschiedene Stationen, an denen unterschiedliche Übungen (Bankdrücken, Klimmzüge, Kniebeuge, Boxsprünge, Schulterdrücken u.a.) absolviert und somit verschiedene Muskelgruppen beansprucht werden. Der große Unterschied zum Zirkel...
- Koordination
- Modell koordinativer FähigkeitenKoordination beschreibt das harmonische Zusammenwirken verschiedener Muskeln mit unterschiedlichen Sinnesorganen und dem ZNS als oberste Steuerinstanz. Die koordinativen Fähigkeiten bewirken, dass die Impulse aufeinander abgestimmt werden und die entsprechenden Muskeln erreichen....
- AnalysatorenAnalysatoren sind für die Wahrnehmungsprozesse zuständig. Es sind Funktionseinheiten von Sinnessystemen bzw. -organen, die verschiedene Informationen aus der Umwelt und dem Körperinneren als Afferenzen zur Verrechnung an das ZNS weiterleiten. Im Zusammenhang mit Bewegung spielen fünf Analysatore...
- Struktur sportlicher Bewegungen
- BewegungsmerkmaleZur Beschreibung und Verbesserung von Bewegungen können sowohl qualitative als auch quantitative Bewegungsmerkmale herangezogen werden....
- Funktionale AnalyseSportliche Bewegungen können als zyklische oder azyklische Bewegungen vorliegen. Zyklische Bewegung sind jene Bewegungen, bei denen sich gleichartige Teilbewegungen (z.B. beim Laufen oder Rudern) wiederholen. Bei azyklischen Bewegungen wird das Bewegungsziel durch eine einmalige Aktion erreicht. Ei...
- Biomechanische Merkmale translatorischer und rotatorischer BewegungenJede Bewegung kann unter dem Gesichtspunkt der biomechanischen Merkmale Translation und Rotation analysiert werden. Manche Bewegungen weisen nur translatorische oder nur rotatorische Bewegungsaspekte auf, wobei die meisten komplexeren Bewegungen aus einer Mischung der beiden Merkmale bestehen....
- Biomechanische PrinzipienWie der Name schon verrät handelt es sich bei diesem Prinzip um den optimalen Beschleunigungsweg einer Bewegung. Ein optimaler Beschleunigungsweg spielt besonders bei Sportarten mit möglichst großen Stoß-, Wurf- und Sprungweiten oder –höhen eine zentrale Rolle. Bei diesen Bewegungen kann eine...
- Exkurs: Analyse eines BewegungsablaufesDa die Bewegungsanalyse das beliebteste Abiturthema ist, wird im Folgenden eine Bewegung exemplarisch analysieren. Analysieren Sie die Bewegung der „flüchtigen Flugrolle“ nach Meinel und Schnabel oder Göhner. Benennen Sie außerdem die Knotenpunkte der Bewegung und analysieren Sie die der Bewe...
- Motive sportlichen Handelns
- Motive sportlichen HandelnsIn Deutschland haben im Jahr 2017 ca. 40 Millionen Menschen angegeben Sport zu treiben. Davon absolvieren 37 Prozent mehrere Einheiten pro Monat und 28 Prozent sogar mehrere Einheiten pro Woche. All diese Menschen haben verschiedene Motive Sport zu treiben, die im Folgenden kurz aufgegriffen und erk...
- GesundheitskonzepteDas Verständnis von Gesundheit oder einem gesunden Leben ist von Person zu Person verschieden. Eine allgemein gültige Definition ist schwierig zu finden, jedoch gibt es einige Eckpunkte, die als Orientierung dienen können. Die WHO definiert Gesundheit als einen Zustand völligen psychischen, phys...
- SalutogenesemodellSalutogenesemodell (lat. salus = Gesundheit, Glück und griech. génesis = Entstehung) Das Modell der Salutogenese befasst sich mit der Frage, was Gesundheit ist und wie sie entsteht. Es ist demnach ein positiver Ansatz zur Erklärung, wie die Gesundheit verbessert, aber auch durch welche Faktoren s...
- RisikofaktorenmodellDas Risikofaktorenmodell beschäftigt sich - im Gegensatz zum Salutogenesemodell - nicht mit der Gesundheitsentstehung, sondern mit Faktoren, die Krankheiten begünstigen bzw. entstehen lassen können. Ein Risikofaktor ist eine körperliche, psychische oder umweltassoziierte Gegebenheit, die eine Kr...
- GesundheitssportDer Gesundheitsbegriff gewinnt in unserer heutigen Zeit immer mehr an Bedeutung. Durch unsere hochtechnologisierte Welt bewegen wir uns immer weniger und leiden immer mehr an den Folgen dieses Bewegungsmangels und an muskulären Dysbalancen. Eine gesunde Ernährung wird in Zeiten von Fastfood immer ...
- Doping
- Was ist DopingDoping kann als die unerlaubte Einnahme, Injektion oder Verabreichung von verbotenen Substanzen, welche dem Sportler zu einer Leistungssteigerung verhelfen, definiert werden. Welche Substanzen verboten sind, wird jährlich von der WADA („World Anti-Doping Agency“) festgelegt. Bei diesen Wirkstof...
- Substanzen
- Anabole SteroideDiese Gruppe stellt die am häufigsten im Doping eingesetzten Substanzen dar. Anabole Steroide sind Abkömmlinge des männlichen Geschlechtshormons Testosteron und haben daher vor allem eine anabole und androgene Wirkung. Die anabole Wirkung zeichnet sich durch einen verstärkten Muskelaufbau aus, ...
- Beta-BlockerDiese Substanzen setzen an den Beta-Rezeptoren des Herzens an und blockieren diese kompetitiv (=reversibel, nicht permanent). Dadurch kommt es zur Senkung der Herzaktivität und zu einem Abfall des Blutdrucks. Sie haben dadurch keine leistungssteigernde, sondern eine beruhigende Wirkung. ...
- DiuretikaDiuretika sind Substanzen, die an den Nieren eine verstärkte Flüssigkeitsausscheidung bewirken. Die Motivation hinter der Einnahme kann zum einen die Verschleierung anderer Dopingmittel sein, die über den Urin nachgewiesen werden können. Zum anderen führt ein großer Wasserverlust auch zu ...
- Peptid- und GlykoproteinhormoneIm Zusammenhang mit Doping wird aus dieser Gruppe vor allem Erythropoetin (EPO) und hGH (= human Growth Hormone) verwendet. ...
- StimulanzienStimulanzien sind Stoffe, die auf das zentrale Nervensystem wirken und dadurch eine höhere körperliche und geistige Aktivität bewirken. Dadurch wird die motorische Leistungsfähigkeit erhöht, die Risikobereitschaft und Wachsamkeit gesteigert und der Körper kann auf Energiereserven zur...
- Motive des DopingsEs gibt sehr viele Gründe und Motive zu dopen. Diese können sehr verschieden und vielseitig sein. Grob können die Gründe und Motive in zwei Gruppen unterteilen: Interne Gründe: Diese Gruppe umfasst alle Gründe, die von dem Sportler selbst ausgehen. Externe Gründe: Diese Gruppe umfasst alle F...
- Vor- und Nachteile einer Legalisierung leistungssteigender Substanzen im SportDie Debatte, ob leistungssteigender Substanzen im (Leistungs-)Sport generell legalisiert werden sollten, wird in den Medien sowie im Abitur von Zeit zu Zeit aufgegriffen, sodass wir auch hier kurz die Argumente, die für oder gegen eine Legalisierung sprechen, aufgreifen werden. Dabei gibt es nicht ...
- Lernen sportlicher Bewegungen
- BewegungshandlungEine Bewegungshandlung ist im Sport ein bewusster und zielgerichteter Prozess. Bevor diese Bewegungshandlung jedoch sichtbar ausgeführt wird, laufen verschiedene Prozesse auf der emotionalen und kognitiven Ebene ab. Zudem erfolgt eine ständige Antizipation des Handlungsergebnisses sowie situations...
- RegelkreislaufmodellJede Bewegungshandlung ist aus unterschiedlichen Komponenten aufgebaut. Wie im vorherigen Kapitel besprochen, reichen diese vom Antriebs- bis zum Ergebnisteil. Die sensomotorische Ausführung ist durch vielfältige Steuerungs- und Regelungsprozesse gekennzeichnet. Aus diesem Grund wird das Regelkrei...
- BewegungsantizipationDas Wort Antizipation stammt aus dem Lateinischen. „Anticipatio“ bedeutet so viel wie Vorwegnahme. Als Antizipation wird im Sport die mentale Vorwegnahme eines künftigen Bewegungsablaufes bezeichnet. Einfacher ausgedrückt bedeutet Antizipation, dass aufgrund von Erfahrung und aktueller Wahrne...
- Phasen sportlichen LernensUm das Lernen sportlicher Bewegungen zu verstehen, wurde von Meinel und Schnabel das Dreiphasenmodell entwickelt. Dieses Lernmodell wird auch als „sensomotorische Regelungsvorgänge“ beschrieben. Das Dreiphasenmodell gliedert sich in die Phase der Grobkoordination, der Feinkoordination und der F...
- Kooperation und Konkurrenz im Sportspiel
- Organisation von Sportspielen mit anderen für andereBei der Organisation von Sportspielen handelt es sich um ein eher wage formuliertes Überthema, das auf verschiedene Weisen behandelt werden kann. Dementsprechend vielfältig sind auch die Möglichkeiten eine Aufgabe zu lösen bzw. ein Sportspiel zu planen. Im folgenden Text werden wir dir dazu eini...
- Organisation von Sportspielen durch Verbände Die Organisation von Sportspielen hat in Deutschland eine lange Geschichte und große Wichtigkeit. Im Jahr 2019 existierten in Deutschland knapp 90.000 Sportvereine mit rund 27,4 Millionen Mitgliedern. Dies macht den Deutschen Olympischen Sportbund (kurz DOSB) zur weltweit größten „Non-governmen...
- Kooperation und Konkurrenz im SportspielDas Themenfeld „Kooperation und Konkurrenz im Sportspiel“ ist ein breites Gebiet, welches aus verschiedenen Perspektiven beleuchtet werden kann. Im Folgenden werden wir einige dieser Aspekte aufgreifen. ...
- Fair PlayFair Play ist ein sehr weitreichendes und teilweise auch uneindeutiges Thema, bei dem die Meinungen sehr weit auseinandergehen. Diese Gegebenheit macht es als Thema für eine Abituraufgabe umso lukrativer. Nach dem sportwissenschaftlichen Lexikon lässt sich Fairplay als „eine ethische Grundhaltu...
- Wechselwirkungen zwischen Wirtschaft, Politik, Medien und Sport
- Wechselwirkungen zwischen Wirtschaft, Politik, Medien und Sport Jedes Jahr wird im Sportabitur mindestens eine Aufgabe zu dem gesellschaftlichen Aspekt von Sport gestellt. Diese Aufgaben sind meist mit reichlich Material unterlegt und behandeln aktuelle sportliche Phänomene, wie die Wirkung von Massenevents (z.B. Olympische Spiele) auf die Bevölkerung oder die...
- Mediale Vermarktung von SportartenAuch für Randsportarten ist eine gezielte mediale Vermarktung von Bedeutung, um den Bekanntheitsgrad zu steigern und das Interesse der Gesellschaft für die jeweilige Sportart zu wecken. Ein gutes Beispiel für den Effekt einer guten medialen Vermarktung ist der Verlauf der Sportart „Crossfit“ ...
- Die Schattenseite der WechselwirkungDiese Beziehung von Sport, Medien und Wirtschaft ist aber nicht in jeder Hinsicht förderlich und hat auch destruktive Seiten. So können die finanziellen Mittel, die zwischen den drei Parteien fließen, Sportler unter Druck setzen. Vor allem junge Athleten, die zur Weltspitze in ihrer Sportart ge...
- TrendsportartenZuletzt sollten auch die Trendsportarten nicht unerwähnt bleiben. Diese Gruppe von Sportarten genießt von Zeit zu Zeit ein großes Aufsehen in den Medien und könnte auch im Abitur aufgegriffen werden. Eine Trendsportart hast du mit Crossfit schon kennengelernt. Was genau macht eine Trendsport au...
- DopingDoping ist in der Sportwelt ein weitverbreitetes Problem. Die WADA (Welt-Anti-Doping-Agentur) bezeichnet Doping als den Versuch der Leistungssteigerung bei gleichzeitiger Gesundheitsgefährdung durch die Anwendung von Substanzen der verbotenen Wirkstoffgruppen oder durch die Anwendung verbotener Met...
- Grundlagen sportlicher Leistungsfähigkeit
- Keine Treffer gefunden
Gentherapie
Die Gentherapie ist ein medizinisches Verfahren, bei dem defekte oder fehlende Gene in den Zellen eines Patienten repariert, ersetzt oder ergänzt werden. Ziel ist es, genetisch bedingte Erkrankungen auf molekularer Ebene zu behandeln oder im Idealfall zu heilen. Im Gegensatz zur klassischen Pharmakotherapie, die meist nur Symptome lindert, setzt die Gentherapie direkt an der Ursache der Erkrankung an – dem defekten Gen.
Grundvoraussetzung für eine Gentherapie ist, dass die genetische Ursache der Krankheit bekannt ist und das betroffene Gen identifiziert wurde. Besonders geeignet sind monogene Erkrankungen, also Krankheiten, die durch den Defekt eines einzigen Gens verursacht werden (z. B. Mukoviszidose, Sichelzellanämie, SCID).
In der Gentherapie unterscheidet man zwei grundsätzliche Ansätze:
- Somatische Gentherapie: Hierbei werden ausschließlich Körperzellen (somatische Zellen) des Patienten genetisch verändert. Die Veränderungen betreffen nur den behandelten Patienten und werden nicht an Nachkommen weitergegeben. Diese Form der Gentherapie ist ethisch weitgehend akzeptiert und wird bereits in der klinischen Praxis angewendet.
- Keimbahntherapie: Bei der Keimbahntherapie werden Keimzellen (Ei- oder Samenzellen) oder frühe Embryonalzellen genetisch verändert. Die Veränderungen werden an alle nachfolgenden Generationen vererbt. Die Keimbahntherapie ist in Deutschland und den meisten Ländern verboten, da die langfristigen Folgen nicht absehbar sind und schwerwiegende ethische Bedenken bestehen.
Abitur-Tipp: In Klausuren wird häufig nach dem Unterschied zwischen somatischer Gentherapie und Keimbahntherapie gefragt. Der entscheidende Unterschied liegt in der Vererbbarkeit: Somatische Gentherapie betrifft nur den Patienten selbst, Keimbahntherapie auch dessen Nachkommen. Merke dir außerdem, dass die Keimbahntherapie in Deutschland durch das Embryonenschutzgesetz verboten ist.
Um ein therapeutisches Gen in die Zielzellen einzubringen, benötigt man einen Vektor (Genfähre). Die häufigsten Vektoren sind modifizierte Viren, da diese von Natur aus in der Lage sind, ihr genetisches Material in Wirtszellen einzuschleusen. Die viralen Gene, die für die Vermehrung und Pathogenität verantwortlich sind, werden entfernt und durch das therapeutische Gen ersetzt.
- Retroviren: Retroviren integrieren ihr Genom dauerhaft in das Wirtsgenom. Vorteil: langfristige Expression des therapeutischen Gens. Nachteil: Die Integration erfolgt zufällig und kann zu Insertionsmutagenese führen, wenn das Transgen in der Nähe eines Onkogens oder Tumorsuppressorgens eingebaut wird.
- Adenoviren: Adenoviren integrieren ihr Genom nicht in die Wirts-DNA, sondern verbleiben als Episom im Zellkern. Vorteil: kein Risiko der Insertionsmutagenese. Nachteil: Die Genexpression ist vorübergehend, da das Episom bei Zellteilungen verloren gehen kann. Zudem können Adenoviren starke Immunreaktionen auslösen.
- Adeno-assoziierte Viren (AAV): AAV sind kleine, nicht-pathogene Viren, die sowohl sich teilende als auch ruhende Zellen infizieren können. Sie integrieren sich nur selten ins Wirtsgenom und lösen kaum Immunreaktionen aus. AAV gelten derzeit als die sichersten und vielseitigsten viralen Vektoren und werden in vielen klinischen Studien eingesetzt.
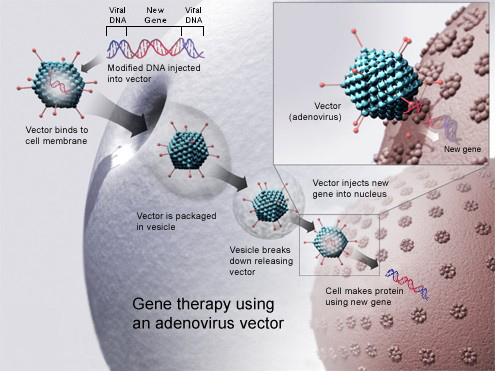
Gentherapie mit viralem Vektor
Ein viraler Vektor transportiert das therapeutische Gen in die Zielzelle. Je nach Vektortyp (Retrovirus, Adenovirus, AAV) wird das Gen integriert oder liegt als Episom vor.
Neben viralen Vektoren gibt es auch nicht-virale Methoden zur Übertragung von Genen:
- Lipofektion: Das therapeutische Gen wird in Liposomen (künstliche Lipidvesikel) verpackt, die mit der Zellmembran verschmelzen und das Gen in die Zelle einschleusen.
- Elektroporation: Durch kurze elektrische Impulse werden vorübergehend Poren in der Zellmembran erzeugt, durch die DNA in die Zelle gelangen kann.
- Genkanone (Biolistik): DNA-beschichtete Goldpartikel werden mit hoher Geschwindigkeit in die Zellen geschossen. Diese Methode wird vor allem bei Pflanzenzellen eingesetzt.
Nicht-virale Methoden sind in der Regel sicherer, da sie kein Risiko einer Insertionsmutagenese oder viraler Immunreaktionen bergen. Allerdings ist ihre Effizienz meist geringer als die viraler Vektoren.
Je nach Durchführung unterscheidet man zwei Strategien:
- In-vivo Gentherapie: Der Vektor mit dem therapeutischen Gen wird direkt in den Körper des Patienten eingebracht (z. B. durch Injektion oder Inhalation). Die Transfektion der Zielzellen erfolgt im lebenden Organismus. Diese Methode wird eingesetzt, wenn die Zielzellen nicht leicht entnommen werden können (z. B. Nervenzellen, Leberzellen).
- Ex-vivo Gentherapie: Dem Patienten werden zunächst Zellen entnommen, außerhalb des Körpers (in vitro) genetisch verändert und anschließend zurücktransplantiert. Vorteil: Die Transfektion kann unter kontrollierten Bedingungen überprüft werden, bevor die Zellen reinfundiert werden. Diese Methode eignet sich besonders gut für Blutstammzellen.
Das CRISPR/Cas9-System (Clustered Regularly Interspaced Short Palindromic Repeats) hat die Gentherapie revolutionär verändert. Es stammt ursprünglich aus dem Immunsystem von Bakterien, die damit virale DNA erkennen und zerstören.
Das System besteht aus zwei Komponenten:
- Guide-RNA (gRNA): Eine kurze RNA-Sequenz, die komplementär zur Zielsequenz im Genom ist und das Cas9-Enzym zur gewünschten Stelle navigiert.
- Cas9-Endonuklease: Ein Enzym, das an der durch die gRNA definierten Stelle einen Doppelstrangbruch in der DNA erzeugt.
Nach dem Doppelstrangbruch gibt es zwei Reparaturwege:
- NHEJ (Non-Homologous End Joining): Die Bruchenden werden direkt wieder verknüpft. Dabei können Insertionen oder Deletionen entstehen, die ein Gen gezielt ausschalten können (Gene Knockout).
- HDR (Homology-Directed Repair): Wird eine DNA-Vorlage (Reparaturmatrix) mitgeliefert, kann die Zelle die Bruchstelle präzise nach dieser Vorlage reparieren. So können defekte Gene gezielt korrigiert oder neue Sequenzen eingefügt werden.
Die Vorteile von CRISPR/Cas9 gegenüber älteren Methoden sind die hohe Präzision, Effizienz, einfache Handhabung und geringe Kosten. Eine Herausforderung bleiben mögliche Off-Target-Effekte, also unbeabsichtigte Schnitte an ähnlichen, aber nicht identischen DNA-Sequenzen.
Abitur-Tipp: CRISPR/Cas9 ist eines der wichtigsten Themen in der modernen Genetik und wird regelmäßig im Abitur abgefragt. Du solltest den Mechanismus (gRNA + Cas9 → Doppelstrangbruch → NHEJ oder HDR) sicher erklären können und wissen, worin sich CRISPR/Cas9 von klassischen Gentherapie-Methoden unterscheidet. Auch der Vergleich mit Restriktionsenzymen wird gerne geprüft: Während Restriktionsenzyme nur bestimmte kurze Erkennungssequenzen schneiden, kann CRISPR/Cas9 durch die frei wählbare gRNA jede beliebige Sequenz im Genom ansteuern.
Die folgenden Erkrankungen sind wichtige Beispiele für die Anwendung der Gentherapie:
- SCID (Severe Combined Immunodeficiency): Eine schwere Immunschwäche, bei der ein Defekt im ADA-Gen (Adenosindesaminase) oder im IL2RG-Gen die Entwicklung funktionsfähiger Lymphozyten verhindert. Betroffene Kinder müssen in sterilen Umgebungen leben („Bubble Babies“). Die ex-vivo Gentherapie mit retroviralen Vektoren war einer der ersten klinischen Erfolge der Gentherapie (bereits in den 1990er-Jahren). Allerdings entwickelten einige Patienten durch Insertionsmutagenese Leukämie, was die Risiken der Methode verdeutlichte.
- Mukoviszidose (Cystische Fibrose): Eine autosomal-rezessiv vererbte Erkrankung, die durch Mutationen im CFTR-Gen verursacht wird. Das defekte CFTR-Protein führt zu zähem Schleim in Lunge und anderen Organen. Gentherapeutische Ansätze zielen darauf ab, das funktionstüchtige CFTR-Gen mittels viraler Vektoren oder Liposomen in die Lungenepithelzellen einzubringen.
- Sichelzellanämie: Eine Mutation im β-Globin-Gen führt zu fehlgeformten Erythrozyten. Mit CRISPR/Cas9-basierten Therapien (z. B. Casgevy) können die Blutstammzellen des Patienten so verändert werden, dass sie wieder funktionstüchtiges Hämoglobin produzieren. Casgevy wurde 2023 als erste CRISPR-basierte Therapie zugelassen.
Trotz großer Fortschritte birgt die Gentherapie verschiedene Risiken:
- Insertionsmutagenese: Bei der Verwendung integrierender Vektoren (z. B. Retroviren) kann das therapeutische Gen an einer ungünstigen Stelle im Genom eingebaut werden. Wird dadurch ein Onkogen aktiviert oder ein Tumorsuppressorgen inaktiviert, kann dies zur Entstehung von Krebs führen. Dies trat bei SCID-Patienten auf, die nach erfolgreicher Gentherapie Leukämie entwickelten.
- Immunreaktionen: Der Körper kann den viralen Vektor als Fremdstoff erkennen und eine Immunantwort auslösen. Im schlimmsten Fall kann dies zu schweren Entzündungsreaktionen oder einem anaphylaktischen Schock führen. Der Fall von Jesse Gelsinger (1999), der nach einer Adenovirus-basierten Gentherapie an einer überschießenden Immunreaktion starb, verdeutlichte dieses Risiko.
- Off-Target-Effekte (bei CRISPR/Cas9): Die Cas9-Endonuklease kann an Stellen schneiden, die der Zielsequenz ähnlich, aber nicht identisch sind. Solche unbeabsichtigten Mutationen können schädliche Auswirkungen haben.
- Unzureichende oder übermäßige Expression: Das therapeutische Gen wird möglicherweise nicht in ausreichender Menge oder zu stark exprimiert, was zu unerwarteten Nebenwirkungen führen kann.
Die Gentherapie wirft zahlreiche ethische Fragen auf, insbesondere im Zusammenhang mit der Keimbahntherapie:
- Pro somatische Gentherapie: Sie kann schwere Leiden lindern oder heilen, betrifft nur den einzelnen Patienten und ist mit anderen medizinischen Eingriffen vergleichbar.
- Pro Keimbahntherapie: Sie könnte genetische Erkrankungen dauerhaft aus einer Familie eliminieren und zukünftigen Generationen Leid ersparen.
- Contra Keimbahntherapie: Die langfristigen Folgen für nachfolgende Generationen sind nicht absehbar. Es besteht die Gefahr des Enhancement (genetische Verbesserung über das Therapieziel hinaus), das zu einer „Zweiklassengesellschaft“ führen könnte. Zudem können zukünftige Generationen nicht in den Eingriff einwilligen (fehlende Einwilligung).
- Rechtliche Lage in Deutschland: Die somatische Gentherapie ist unter strengen Auflagen erlaubt. Die Keimbahntherapie ist durch das Embryonenschutzgesetz (ESchG, 1990) verboten. International gibt es unterschiedliche Regelungen – der Fall des chinesischen Forschers He Jiankui, der 2018 die ersten geneditierten Babys erzeugte, löste weltweit Empörung aus und führte zu verschärften Regulierungen.
Abitur-Tipp: Ethische Erörterungen zur Gentherapie sind ein typisches Klausurformat. Verwende dafür am besten eine Pro-Contra-Struktur und berücksichtige verschiedene Perspektiven (Patient, Gesellschaft, zukünftige Generationen). Wichtige Argumente sind: Linderung von Leid vs. unabsehbare Folgen, individuelle Freiheit vs. gesellschaftliche Verantwortung, Therapie vs. Enhancement. Vergiss nicht, die rechtliche Lage in Deutschland zu erwähnen (Embryonenschutzgesetz).
Die Gentherapie hat in den letzten Jahren bemerkenswerte Fortschritte erzielt:
- Zugelassene Gentherapeutika: Mehrere Gentherapien sind inzwischen zugelassen, darunter Luxturna (gegen erbliche Netzhautdystrophie, RPE65-Mutation), Zolgensma (gegen spinale Muskelatrophie, SMN1-Gen) und Casgevy (CRISPR-basiert gegen Sichelzellanämie und β-Thalassämie).
- CAR-T-Zelltherapie: Eine Sonderform der ex-vivo Gentherapie, bei der körpereigene T-Zellen genetisch so verändert werden, dass sie einen chimären Antigenrezeptor (CAR) tragen und gezielt Krebszellen erkennen und zerstören können. Diese Therapie zeigt beeindruckende Erfolge bei bestimmten Blutkrebs-Formen.
- Base Editing und Prime Editing: Weiterentwicklungen von CRISPR/Cas9, die einzelne Basen gezielt austauschen können, ohne einen Doppelstrangbruch zu erzeugen. Diese Methoden sind präziser und bergen ein geringeres Risiko für Off-Target-Effekte.
- Zukunftsperspektiven: Die Gentherapie könnte in Zukunft auch bei polygenen Erkrankungen (z. B. Diabetes, Herz-Kreislauf-Erkrankungen) und bei neurodegenerativen Erkrankungen (z. B. Alzheimer, Parkinson) zum Einsatz kommen. Die stetige Verbesserung der Vektoren und Editierungswerkzeuge macht immer präzisere und sicherere Eingriffe möglich.
Abitur-Tipp: Für das Abitur solltest du die grundlegenden Methoden der Gentherapie (virale Vektoren, CRISPR/Cas9) und mindestens zwei konkrete Anwendungsbeispiele (z. B. SCID, Sichelzellanämie) nennen können. Besonders wichtig ist, dass du die Vorteile und Risiken differenziert darstellen kannst. Verknüpfe dein Wissen über Gentherapie mit anderen Themen wie Gentechnik, Mutationen und Proteinbiosynthese – solche Querverbindungen werden im Abitur gerne verlangt.