Bibliothek
Fach wählen
Themen
Bohrsches Atommodell
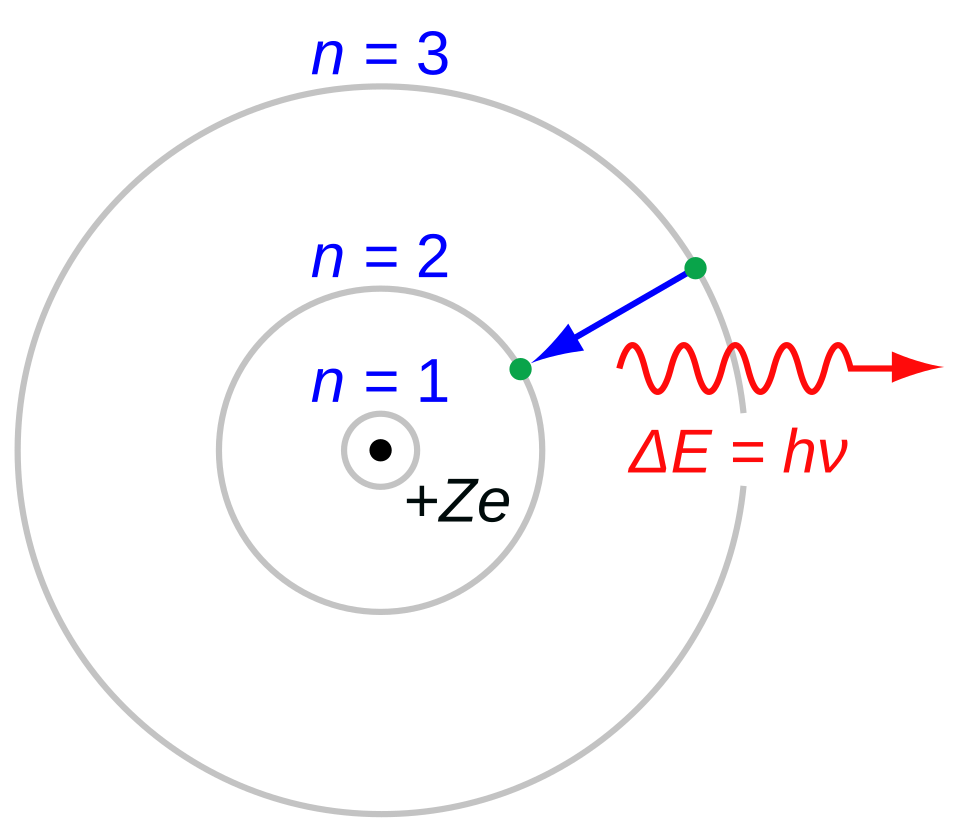
Nach Rutherfords Streuversuch (1909) war klar, daß Atome aus einem winzigen positiven Kern und einer Elektronenhülle bestehen. Klassisch hätten Elektronen jedoch durch Kreisbewegung ständig Energie abstrahlen und in den Kern stürzen müssen. Niels Bohr löste das Problem 1913 mit drei Postulaten.
1. Quantisierungspostulat: Elektronen bewegen sich strahlungsfrei nur auf bestimmten Bahnen, deren Bahndrehimpuls quantisiert ist:
\[ L = m_e\,v\,r = n\,\frac{h}{2\pi},\quad n = 1, 2, 3,\ldots \]
2. Frequenzbedingung: Beim Übergang zwischen zwei Bahnen wird ein Photon emittiert oder absorbiert:
\[ h\,f = E_n - E_m \]
3. Die Bewegung auf der Bahn folgt klassischen Gesetzen.
Aus Coulomb-Anziehung als Zentripetalkraft \( \dfrac{e^2}{4\pi\varepsilon_0\,r^2} = \dfrac{m_e\,v^2}{r} \) und Quantisierungsbedingung folgen die Bahnradien:
\[ r_n = n^2 \cdot a_0,\quad a_0 = \frac{\varepsilon_0 h^2}{\pi m_e e^2} \approx 5{,}29\cdot 10^{-11}\,\text{m} \]
und die Energieniveaus des Wasserstoffatoms:
\[ E_n = -\frac{13{,}6\,\text{eV}}{n^2} \]
Der Grundzustand liegt bei \( E_1 = -13{,}6\,\text{eV} \).
Beim Übergang \( n = 3 \to n = 2 \) wird ein Photon emittiert:
\[ \Delta E = E_3 - E_2 = -\frac{13{,}6}{9} + \frac{13{,}6}{4}\,\text{eV} \approx 1{,}89\,\text{eV} \]
Die Wellenlänge:
\[ \lambda = \frac{hc}{\Delta E} \approx 656\,\text{nm} \]
Das ist die rote Balmer-Linie Hα.
Das Bohrsche Modell beschreibt das Wasserstoffspektrum äußerst gut, scheitert aber bei Mehrelektronenatomen, der Linienfeinstruktur und der Erklärung chemischer Bindung. Diese Probleme löst erst die Quantenmechanik mit der Schrödinger-Gleichung.
Vergessen, daß \( E_n \) negativ ist (gebundene Zustände). Bei der Berechnung von Wellenlängen muß immer \( |\Delta E| \) eingesetzt werden.
Zusammenfassung: Bohr postuliert quantisierte Bahnen mit \( L = nh/(2\pi) \). Die Wasserstoff-Energieniveaus sind \( E_n = -13{,}6\,\text{eV}/n^2 \).
Abitur-Tipp: Präge dir \( E_n = -13{,}6\,\text{eV}/n^2 \) und die Frequenzbedingung \( hf = E_n - E_m \) ein. Damit lässt sich praktisch jede Aufgabe zur Wasserstoff-Spektroskopie lösen.